Giáo án điện tử chuyên đề Hoá học 10 cánh diều Bài 3: Năng lượng hoạt hoá của phản ứng hoá học
Tải giáo án điện tử Chuyên đề học tập Hoá học 10 cánh diều Bài 3: Năng lượng hoạt hoá của phản ứng hoá học. Bộ giáo án chuyên đề được thiết kế sinh động, đẹp mắt. Thao tác tải về đơn giản, dễ dàng sử dụng và chỉnh sửa. Thầy, cô kéo xuống để xem chi tiết.
Xem: => Giáo án hóa học 10 cánh diều (bản word)
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét







Xem toàn bộ: Giáo án điện tử chuyên đề Hoá học 10 cánh diều
NHIỆT LIỆT CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI!
BÀI 3: NĂNG LƯỢNG HOẠT HÓA CỦA PHẢN ỨNG HÓA HỌC
KHỞI ĐỘNG
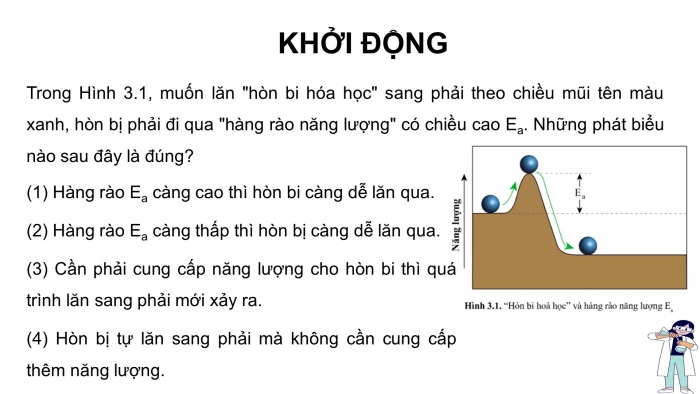
Trong Hình 3.1, muốn lăn "hòn bi hóa học" sang phải theo chiều mũi tên màu xanh, hòn bị phải đi qua "hàng rào năng lượng" có chiều cao Ea. Những phát biểu nào sau đây là đúng?
(1) Hàng rào Ea càng cao thì hòn bi càng dễ lăn qua.
(2) Hàng rào Ea càng thấp thì hòn bị càng dễ lăn qua.
(3) Cần phải cung cấp năng lượng cho hòn bi thì quá trình lăn sang phải mới xảy ra.
(4) Hòn bị tự lăn sang phải mà không cần cung cấp thêm năng lượng.
NỘI DUNG BÀI HỌC
I. Năng lượng hoạt hóa
II. Ảnh hưởng của năng lượng hoạt hóa và nhiệt độ tới tốc độ phản ứng qua phương trình Arrhenius
III. Vai trò của chất xúc tác
I. Năng lượng hoạt hóa
Thế nào là va chạm có hiệu quả?
> Va chạm có hiệu quả là những va chạm đúng hướng và đủ năng lượng để tạo ra sản phẩm
Nếu các chất không đủ năng lượng thì có xảy ra phản ứng hay không?
> Các chất không đủ năng lượng thì có không xảy ra phản ứng
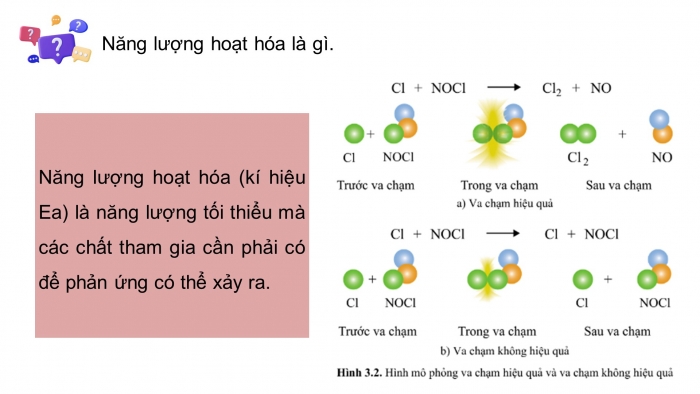
Năng lượng hoạt hóa là gì.
Năng lượng hoạt hóa (kí hiệu Ea) là năng lượng tối thiểu mà các chất tham gia cần phải có để phản ứng có thể xảy ra.
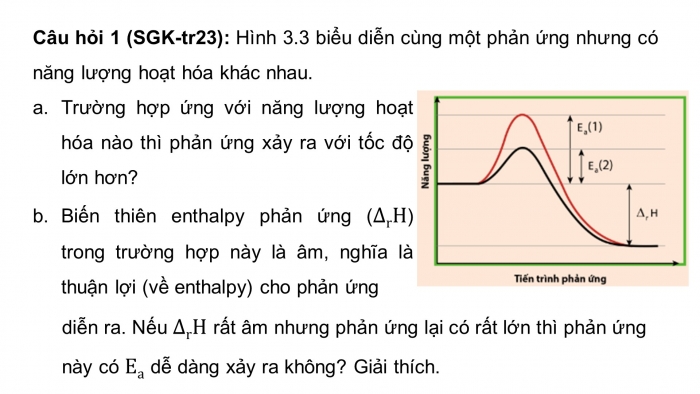
Câu hỏi 1 (SGK-tr23): Hình 3.3 biểu diễn cùng một phản ứng nhưng có năng lượng hoạt hóa khác nhau.
- Trường hợp ứng với năng lượng hoạt hóa nào thì phản ứng xảy ra với tốc độ lớn hơn?
- Biến thiên enthalpy phản ứng (∆rH) trong trường hợp này là âm, nghĩa là thuận lợi (về enthalpy) cho phản ứng diễn ra. Nếu ∆rH rất âm nhưng phản ứng lại có rất lớn thì phản ứng này có Ea dễ dàng xảy ra không? Giải thích.
Trả lời:
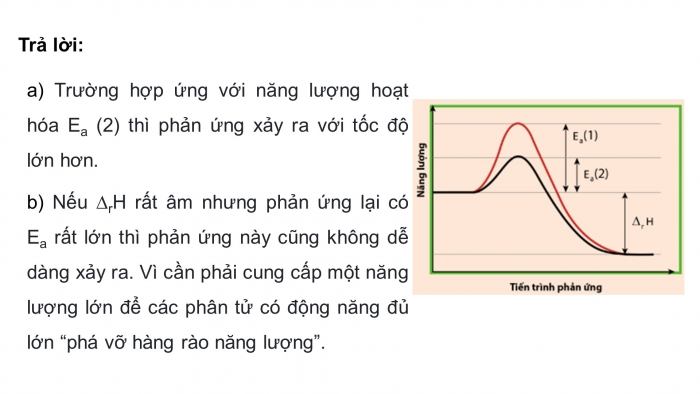
a) Trường hợp ứng với năng lượng hoạt hóa Ea (2) thì phản ứng xảy ra với tốc độ lớn hơn.
b) Nếu ∆rH rất âm nhưng phản ứng lại có Ea rất lớn thì phản ứng này cũng không dễ dàng xảy ra. Vì cần phải cung cấp một năng lượng lớn để các phân tử có động năng đủ lớn “phá vỡ hàng rào năng lượng”.
Vận dụng 1 (tr-20): Các phản ứng tạo gỉ kim loại có thể xảy ra ngay ở điều kiện nhiệt độ phòng mà không cần đun nóng. Hãy dự đoán năng lượng hoạt hóa của phản ứng là thấp hay cao.
Trả lời:
Các phản ứng tạo gỉ kim loại có thể xảy ra ngay ở điều kiện nhiệt độ phòng mà không cần đun nóng. Vì vậy, năng lượng hoạt hóa của phản ứng tạo gỉ kim loại là thấp.
KẾT LUẬN
- Năng lượng hoạt hóa càng thấp phản ứng càng dễ xảy ra.
- Năng lượng hoạt hóa càng lớn thì tốc độ phản ứng càng nhỏ và năng lượng hoạt hóa càng nhỏ, thì tốc độ phản ứng càng lớn.
II. ẢNH HƯỞNG CỦA NĂNG LƯỢNG HOẠT HÓA VÀ NHIỆT ĐỘ TỚI TỐC ĐỘ PHẢN ỨNG QUA PHƯƠNG TRÌNH ARRHENIUS
PHIẾU HỌC TẬP
(1) Viết biểu thức tốc độ phản ứng, nêu ý nghĩa của tứng kí hiệu trong biểu thức.
(2) Câu hỏi 2: Phát biểu định luật tác dụng khối lượng về tốc độ của phản ứng hóa học.
(3) Viết phương trình Arrhenius và cho biết ý nghĩa của các kí hiệu trong phương trình đó.
(4) Luyện tập 1: Nếu ở ví dụ 1, Ea (1) = 100 kJ mol-1 và
Ea (2) = 150 kJ mol-1 thì tốc độ phản ứng thay đổi như thế nào?
(5) Luyện tập 2: Nếu ở ví dụ 2, Ea = 50 kJ mol-1 thì tốc độ phản ứng thay đổi như thế nào?
Trả lời các câu Phiếu học tập:
(1) Xét phản ứng:
mM + nN ![]() sản phẩm
sản phẩm![]()
Biểu thức tốc độ phản ứng: ![]() .
.
trong đó:
- k là hằng số tốc độ phản ứng;
 lần lượt là nồng độ các chất M, N tham gia phản ứng.
lần lượt là nồng độ các chất M, N tham gia phản ứng.- m, n là hệ số của các chất M, N trong phản ứng.
(2) Định luật tác dụng khối lượng về tốc độ của phản ứng hóa học:
"Ở nhiệt độ không đổi, tốc độ phản ứng tỉ lệ với tích số nồng độ các chất tham gia phản ứng với số mũ thích hợp"
(3) Phương trình Arrhenius:
![]()
Trong đó:
- k là hằng số tốc độ phản ứng
- A là hằng số thực nghiệm Arrhenius
- e là cơ số của logarit tự nhiên, e = 2,7183
- Ea: năng lượng hoạt hóa (J/mol).
- R là hằng số lí tưởng, R =8,324 (J/mol.K)
- T là nhiệt độ theo thang Kelvin (K).
(4)
Ta có:
![]()
Như vậy trong trường hợp này, khi năng lượng hoạt hóa tăng 50 kJ mol-1
thì tốc độ phản ứng giảm đi khoảng 581 triệu lần.
(5) Ta có:

Vậy trong trường hợp Ea = 50 kJ mol-1 thì tốc độ phản ứng tăng xấp xỉ 1,93 lần.
Theo phương trình kinh nghiệm của Arrhenius, ta có: ![]() , trong cùng một phản ứng,
, trong cùng một phản ứng, ![]() không đổi, hằng số
không đổi, hằng số ![]() và
và ![]() không đổi, khi tăng nhiệt độ, dẫn đến hằng số tốc độ
không đổi, khi tăng nhiệt độ, dẫn đến hằng số tốc độ ![]() của phản ứng tăng, nên tốc độ phản ứng tăng.
của phản ứng tăng, nên tốc độ phản ứng tăng.
Dựa vào phương trình Arrhenius, tốc độ phản ứng thay đổi như thế nào khi tăng nhiệt độ của phản ứng?
> Tốc độ phản ứng tăng
Tốc độ phản ứng thay đổi như thế nào khi Ea càng lớn.
> Tốc độ phản ứng tăng
Vận dụng 2 (tr-25): Hãy liệt kê kết quả ở ví dụ 2 với hệ số Van’t Hof về sự thay đổi tốc độ phản ứng theo nhiệt độ
Trả lời:
Theo Van’t Hoff với đa số các phản ứng, khi nhiệt độ tăng 10oC thì tốc độ phản ứng tăng từ 2 đến 4 lần.
> Kết quả ở ví dụ 2 phù hợp với hệ số Van’t Hoff về sự thay đổi tốc độ phản ứng theo nhiệt độ.
III. VAI TRÒ CỦA CHẤT XÚC TÁC
Mô tả thí nghiệm và nêu vai trò của chất xúc tác.
Thí nghiệm phân hủy H2O2 trong dung dịch ở nhiệt độ thường, khi cho thêm MnO2 vào thì phản ứng xảy ra nhanh hơn có hiện tượng sủi bọt khí và ống thí nghiệm nóng lên.
Phương trình phản ứng:
![]() )
)
Thế nào là chất xúc tác.
Câu hỏi 3 (SGK-tr25): Một phản ứng diễn ra ở một nhiện độ không đối, khi them chất xúc tác, tốc độ phản ứng tăng lên do năng lượng hoạt hóa bị thay đổi. Vậy chất xúc tác làm tăng hay giảm năng lượng hoạt hóa của phản ứng?
--------------- Còn tiếp ---------------
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử chuyên đề Hoá học 10 cánh diều
