Giáo án điện tử KHTN 7 cánh diều – Phần hóa học bài 6: Hoá trị, công thức hoá học
Bài giảng điện tử KHTN 7 cánh diều – Phần hóa học. Giáo án powerpoint bài 6: Hoá trị, công thức hoá học. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt tạo hứng thú học tập cho học sinh. Thầy cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 7 cánh diều (bản word)
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét







Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hóa học 7 cánh diều
NHIỆT LIỆT CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC NÀY
KHỞI ĐỘNG
- Ghép hình và ghi kết quả ghép hình theo kí hiệu hoá học và các con số
BÀI 6: HOÁ TRỊ, CÔNG THỨC HOÁ HỌC
NỘI DUNG BÀI HỌC
HOÁ TRỊ
CÔNG THỨC HOÁ HỌC
- HOÁ TRỊ
- Khái niệm hoá trị
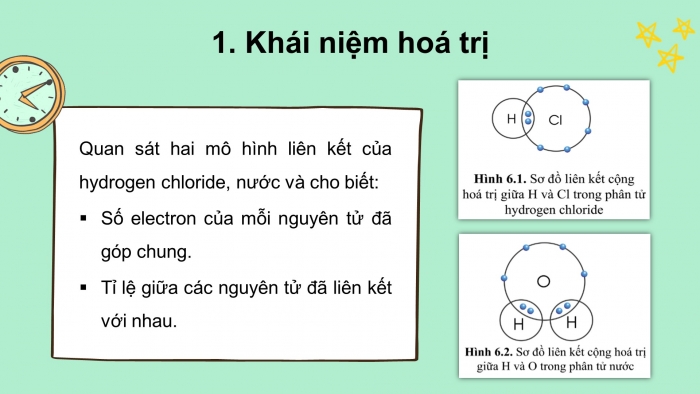
Quan sát hai mô hình liên kết của hydrogen chloride, nước và cho biết:
- Số electron của mỗi nguyên tử đã góp chung.
- Tỉ lệ giữa các nguyên tử đã liên kết với nhau.
- Khi tạo thành phân tử hydrogen chloride, mỗi nguyên tử H và Cl góp 1e.
- Đôi electron dùng chung giữa 2 nguyên tử.
- H và Cl có hoá trị I.
- Khi H kết hợp với O, mỗi nguyên tử H góp chung 1 electron, nguyên tử O góp chung 2 electron.
- H có hoá trị I, O có hoá trị II.
- Kết luận: Hoá trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác.
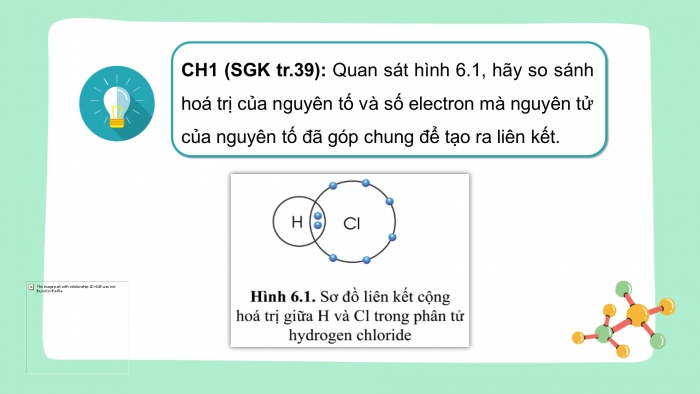
CH1 (SGK tr.39): Quan sát hình 6.1, hãy so sánh hoá trị của nguyên tố và số electron mà nguyên tử của nguyên tố đã góp chung để tạo ra liên kết.
Hoá trị của nguyên tố = số electron mà nguyên tử của nguyên tố đã góp chung để tạo ra liên kết.
Nhận xét về hoá trị của H và O trong các hợp chất?
Trong hợp chất, H luôn có hoá trị I, O luôn có hoá trị II.
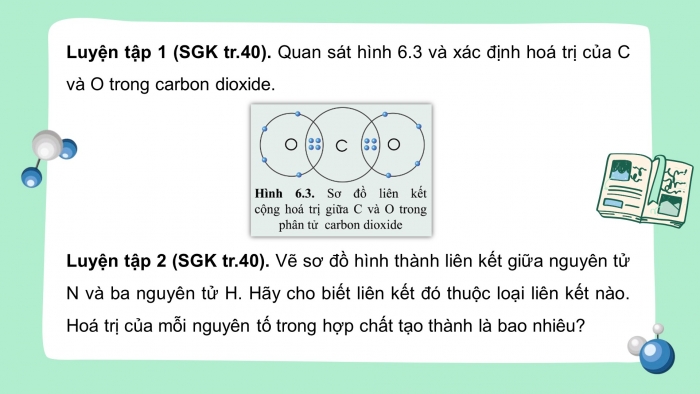
Luyện tập 1 (SGK tr.40). Quan sát hình 6.3 và xác định hoá trị của C và O trong carbon dioxide.
Luyện tập 2 (SGK tr.40). Vẽ sơ đồ hình thành liên kết giữa nguyên tử N và ba nguyên tử H. Hãy cho biết liên kết đó thuộc loại liên kết nào. Hoá trị của mỗi nguyên tố trong hợp chất tạo thành là bao nhiêu?
Luyện tập 1 (SGK tr.40)
Luyện tập 2 (SGK tr.40)
Nguyên tử N có 5e ở lớp ngoài cùng
Cần thêm 3e để đạt cấu hình electron của khí hiếm Ne
Nguyên tử H có 1e ở lớp ngoài cùng
Cần thêm 1e để đạt cấu hình electron của khí hiếm Ne
Liên kết giữa N và H được tạo thành bởi đôi electron dùng chung giữa hai nguyên tử.
- Nguyên tử N góp 3 electron.
- Nguyên tử H góp chung 1 electron.
- Quy tắc hoá trị
- Trong phân tử carbon dioxide, hoá trị và số nguyên tử tham gia liên kết của C và O như sau:
- Quy tắc cộng hoá trị: Khi các nguyên tử của hai nguyên tố A, B liên kết với nhau, tích giữa hoá trị và số nguyên tử của A bằng tích giữa hoá trị và số nguyên tử của B.
CH 2 (SGK tr.41). Cát được sử dụng nhiều trong xây dựng và là nguyên liệu chính để sản xuất thuỷ tinh. Silicon oxide là thành phần chính của cát. Phân tử silicon oxide gồm 1 nguyên tử Si liên kết với 2 nguyên tử O. Dựa vào hoá trị của các nguyên tố trong bảng 6.1, hãy tính tích hoá trị và số nguyên tử của mỗi nguyên tố trong phân tử silicon oxide. Nhận xét về tích đó.
Nhận xét: Tích của hoá trị và số nguyên tử tham gia liên kết của Si và O bằng nhau.
Luyện tập 3 (SGK tr.41). Dựa vào hoá trị của các nguyên tố trong bảng 6.1 và quy tắc hoá trị, hãy cho biết mỗi nguyên tử Mg có thể kết hợp với bao nhiêu nguyên tử Cl.
Luyện tập 4 (SGK tr.41). Nguyên tố A có hoá trị III, nguyên tố B có hoá trị II. Hãy tính tỉ lệ nguyên tử của A và B trong hợp chất tạo thành từ hai nguyên tố đó.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hóa học 7 cánh diều
GIÁO ÁN WORD LỚP 7 - SÁCH CÁNH DIỀU
Soạn giáo án Toán 7 cánh diều cả năm
Giáo án Ngữ văn 7 cánh diều cả năm
Soạn giáo án Thể dục 7 cánh diều theo công văn mới nhất
Soạn giáo án Công dân 7 cánh diều theo công văn mới nhất
Soạn giáo án Khoa học tự nhiên 7 cánh diều theo công văn mới nhất
Soạn giáo án Vật lí 7 cánh diều theo công văn mới nhất
Soạn giáo án Hoá học 7 cánh diều theo công văn mới nhất
Soạn giáo án Sinh học 7 cánh diều theo công văn mới nhất
Soạn giáo án Công nghệ 7 cánh diều theo công văn mới nhất
Soạn giáo án Tin học 7 cánh diều theo công văn mới nhất
Soạn giáo án Lịch sử 7 cánh diều theo công văn mới nhất
Soạn giáo án Địa lí 7 cánh diều theo công văn mới nhất
Soạn giáo án Mĩ thuật 7 cánh diều theo công văn mới nhất
Soạn giáo án Hoạt động trải nghiệm, hướng nghiệp 7 cánh diều theo công văn mới nhất
