Giáo án powerpoint hóa học 11
Giáo án powerpoint hay còn gọi là giáo án điện tử, bài giảng điện tử, giáo án trình chiếu. Dưới đây là bộ giáo án powerpoint hóa học 11. Giáo án được thiết kế theo phong cách hiện đại, đẹp mắt để tạo hứng thú học tập cho học sinh. Với tài liệu này, hi vọng việc dạy môn hóa học 11 của thầy cô sẽ nhẹ nhàng hơn.
Click vào ảnh dưới đây để xem giáo án rõ





Xem video về mẫu Giáo án powerpoint hóa học 11
Một số tài liệu quan tâm khác
Phần trình bày nội dung giáo án
1. GIÁO ÁN POWERPOINT BAO GỒM ĐỦ CÁC BÀI TRONG HÓA HỌC 11
Chương 1: Sự điện li
- Bài 1: Sự điện li
- Bài 2: Axit, bazơ và muối
- Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit-bazơ
- Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
- Bài 5: Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Bài 6: Bài thực hành 1: Tính axit-bazơ. Phản ứng trao đổi ion trong dung dịch các chất điện li
Chương 2: Nitơ - Photpho
- Bài 7 : Nitơ
- Bài 8 : Amoniac và muối amoni
- Bài 9: Axit nitric và muối nitrat
- Bài 10: Photpho
- Bài 11: Axit photphoric và muối photphat
- Bài 12: Phân bón hóa học
- Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng
- Bài 14: Bài thực hành 2: Tính chất của một số hợp chất nitơ, photpho
Chương 3: Cacbon - Silic
- Bài 15 : Cacbon
- Bài 16 : Hợp chất của cacbon
- Bài 17 : Silic và hợp chất của silic
- Bài 18 : Công nghiệp silicat
- Bài 19 : Luyện tập : Tính chất hóa học của cacbon, silic và các hợp chất của chúng
Chương 4: Đại cương về hóa học hữu cơ
- Bài 20 : Mở đầu về hóa học hữu cơ
- Bài 21 : Công thức phân tử hợp chất hữu cơ
- Bài 22 : Cấu trúc phân tử hợp chất hữu cơ
- Bài 23 : Phản ứng hữu cơ
- Bài 24 : Luyện tập : Hợp chất hữu cơ, công thức phân tử và công thức cấu tạo
Chương 5 : Hiđrocacbon no
- Bài 25 : Ankan
- Bài 26 : Xicloankan
- Bài 27 : Luyện tập : Ankan và xicloankan
- Bài 28 : Bài thực hành số 3 : Phân tích định tính nguyên tố. Điều chế và tính chất của metan
Chương 6 : Hiđrocacbon không no
- Bài 29 : Anken
- Bài 30 : Ankađien
- Bài 31 : Luyện tập : Anken và ankađien
- Bài 32 : Ankin
- Bài 33 : Luyện tập : Ankin
- Bài 34 : Bài thực hành 4 : Điều chế và tính chất của etilen và axetilen
Chương 7: Hiđrocacbon thơm. Nguồn hiđrocacbon thiên nhiên. Hệ thống hóa về hiđrocacbon
- Bài 35 : Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
- Bài 36 : Luyện tập : Hiđrocacbon thơm
- Bài 37 : Nguồn hiđrocacbon thiên nhiên
- Bài 38 : Hệ thống hóa về hiđrocacbon
Chương 8: Dẫn xuất halogen - Ancol - Phenol
- Bài 39 : Dẫn xuất halogen của hiđrocacbon
- Bài 40 : Ancol
- Bài 41 : Phenol
- Bài 42 : Luyện tập : Dẫn xuất halogen, ancol, phenol
- Bài 43 : Bài thực hành 5: Tính chất của etanol, glixerol và phenol
Chương 9: Anđehit - Xeton - Axit cacboxylic
- Bài 44 : Anđehit - Xeton
- Bài 45 : Axit cacboxylic
- Bài 46 : Luyện tập : Anđehit - Xeton- Axit cacboxylic
- Bài 47 : Bài thực hành 6 : Tính chất của anđehit và axit cacboxylic
2. GIÁO ÁN WORD BÀI
Ngày soạn:
Tiết 3: SỰ ĐIỆN LI
- MỤC TIÊU:
- Kiến thức:
HS Biết được:
- Khái niệm về sự điện li, chất điện li, chất điện li mạnh, chất điện li yếu, cân bằng điện li
- Quan sát thí nghiệm, rút ra được kết luận về tính dẫn điện của dung dịch chất điện li.
- Phân biệt được chất điện li, chất không điện li, chất điện li mạnh, chất điện li yếu.
- Viết được phương trình điện li của chất điện li mạnh, chất điện li yếu.
- Bản chất tính dẫn điện của chất điện li (nguyên nhân và cơ chế đơn giản)
- Viết phương trình điện li của một số chất.
- Năng lực
* Các năng lực chung
- Năng lực tự học
- Năng lực hợp tác
- Năng lực phát hiện và giải quyết vấn đề
- Năng lực giao tiếp
* Các năng lực chuyên biệt
- Năng lực sử dung ngôn ngữ
- Năng lực thực hành hóa học
- Năng lực tính toán
- Năng lực giải quyết vấn đề thông qua hóa học
- Năng lực vận dụng kiến thức hóa học vào cuộc sống
- Phẩm chất
Yêu gia đình, quê hương đất nước; Nhân ái khoan dung; Trung thực, tự trọng, chí công, vô tư; Tự lập, tự tin, tự chủ; Có trách nhiệm với bản thân, cộng đồng, đất nước, nhân loại; Nghĩa vụ công dân.
- THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- Giáo viên
- Dụng cụ và hoá chất thí nghiệm đo độ dẫn điện
- Học sinh
- Xem lại hiện tượng dẫn điện đã học trong chương trình vật lý lớp 7
III. TIẾN TRÌNH DẠY HỌC
- HOẠT ĐỘNG KHỞI ĐỘNG: (10 phút)
- a) Mục tiêu: Tạo tâm thế trước khi bắt đầu học bài mới.
- b) Nội dung: Giáo viên cho HS làm các thí nghiệm
- c) Sản phẩm: Học sinh làm thí nghiệm
- Tổ chức thực hiện:
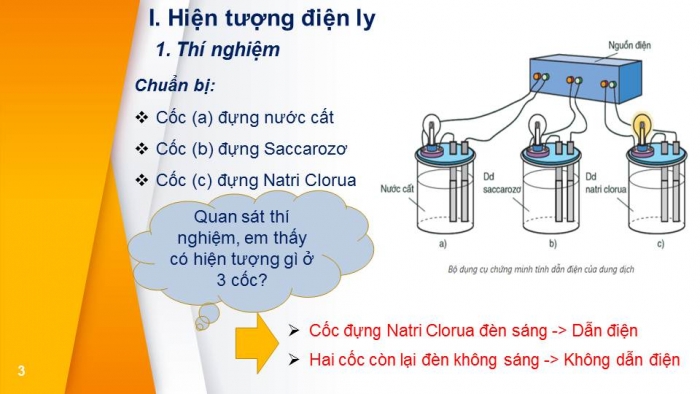
- GV tiến hành thí nghiệm hoặc chiếu phim hoặc xem hình ảnh về thí nghiệm tính dẫn điện:
- của nước cất
- dung dịch saccarozơ
- dung dịch HCl
- dung dịch NaOH
- dung dịch NaCl
Yêu cầu HS: quan sát thí nghiệm, nêu hiện tượng xảy ra? giải thích ?
Giáo viên đặt vấn đề: Tại sao dung dịch HCl, NaCl, NaOH dẫn điện, còn các chất còn lại không dẫn điện?
Giáo viên gợi ý: Vận dụng kiến thức đã học lớp dưới về khái niệm dòng điện để giải thích
- HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Tính dẫn điện
- a) Mục tiêu: Hiểu được nội dung bài học, các khái niệm, định nghĩa có liên quan.
- b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
- c) Sản phẩm: HS vận dụng kiến thức đã học để trả lời các câu hỏi và phiếu bài tập.
- d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH | SẢN PHẨM DỰ KIẾN |
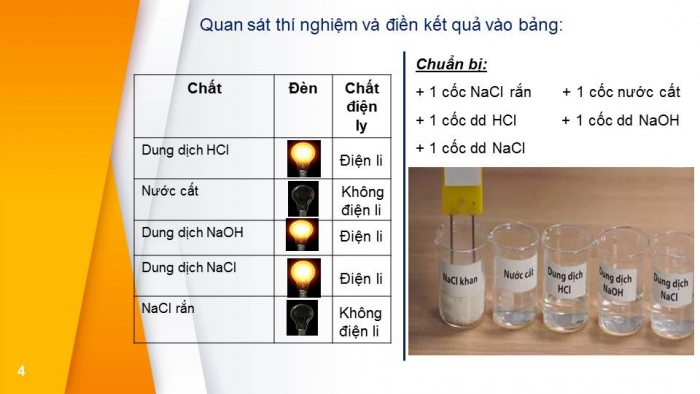
Bước 1: Chuyển giao nhiệm vụ: HS nghiên cứu sgk, thảo luận nhóm để hoàn thành phiếu học tập. Bước 2: Thực hiện nhiệm vụ: HS: Hoạt động nhóm hoàn thành phiếu học tập Bước 3: Báo cáo thảo luận - HĐ chung cả lớp: GV mời 4 nhóm báo cáo kết quả (mỗi nhóm 1 nội dung), các nhóm khác góp ý, bổ sung, phản biện. Bước 4: Kết luận, nhận định: GV chốt lại kiến thức. Kết luận: - Dung dịch axit, bazơ muối dẫn điện. Các chất rắn khan: NaCl, NaOH và một số dung dịch rượu đường không dẫn điện. | I. Hiện tượng điện li 1. Thí nghiệm: SGK
Kết luận: - Dung dịch axit, bazơ muối dẫn điện. Các chất rắn khan: NaCl, NaOH và một số dung dịch rượu đường không dẫn điện |
Hoạt động 2: Nguyên nhân tính dẫn điện của các dung dịch axit, bazơ, muối trong nước
- a) Mục tiêu: Hiểu được nội dung bài học, các khái niệm, định nghĩa có liên quan.
- b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
- c) Sản phẩm: HS vận dụng kiến thức đã học để trả lời các câu hỏi và phiếu bài tập.
- d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH | SẢN PHẨM DỰ KIẾN |
Bước 1: Chuyển giao nhiệm vụ: - Các chất rắn khan: NaCl, NaOH và các dung dịch rượu, đường do chúng tồn tại ở dạng phân tử nên không dẫn điện. - GV đưa ra một số axit bazơ, muối quen thuộc để học sinh biểu diễn sự phân li và gọi tên các ion tạo thành. Bước 2: Thực hiện nhiệm vụ: HS: Hoạt động nhóm hoàn thành phiếu học tập Bước 3: Báo cáo thảo luận - HĐ chung cả lớp: GV mời 4 nhóm báo cáo kết quả (mỗi nhóm 1 nội dung), các nhóm khác góp ý, bổ sung, phản biện. Bước 4: Kết luận, nhận định: GV chốt lại kiến thức. | - Các axit, bazơ, muối khi tan trong nước phân li ra các ion làm cho dung dịch của chúng dẫn điện. - Quá trình phân li các chất trong nước ra ion gọi là sự điện li. - Những chất tan trong nước phân li ra ion gọi là chất điện li. - Sự điện li được biểu diễn bằng phương trình điện li. Ví dụ NaCl → Na+ + Cl- HCl → H+ + Cl- NaOH → Na+ + OH- |
Phiếu học tập số 1
(Phiếu này được dùng để ghi nội dung bài học thay cho vở)
- Tại sao các dung dịch muối axit, bazơ muối dẫn được điện?
- Biểu diễn sự phân li của axit bazơ muối theo phương trình điện li. Hướng dẫn cách gọi tên một số ion.
Hoạt động 3: So sánh sự dẫn điện của các chất
- a) Mục tiêu: Hiểu được nội dung bài học, các khái niệm, định nghĩa có liên quan.
- b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
- c) Sản phẩm: HS vận dụng kiến thức đã học để trả lời các câu hỏi và phiếu bài tập.
- d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH | SẢN PHẨM DỰ KIẾN |
Bước 1: Chuyển giao nhiệm vụ: - GV làm thí nghiệm 2 của dung dịch HCl và CH3COOH ở SGK cho HS nhận xét và rút ra kết luận. Bước 2: Thực hiện nhiệm vụ: HS: Hoạt động nhóm hoàn thành phiếu học tập Bước 3: Báo cáo thảo luận - HĐ chung cả lớp: GV mời 4 nhóm báo cáo kết quả (mỗi nhóm 1 nội dung), các nhóm khác góp ý, bổ sung, phản biện. Bước 4: Kết luận, nhận định: GV chốt lại kiến thức. | - Nhận xét ở cùng nồng độ thì HCl dẫn điện nhiều hơn CH3COOH.
|
Hoạt động 4: Chất điện li mạnh
- a) Mục tiêu: Hiểu được nội dung bài học, các khái niệm, định nghĩa có liên quan.
- b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
- c) Sản phẩm: HS vận dụng kiến thức đã học để trả lời các câu hỏi và phiếu bài tập.
- d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH | SẢN PHẨM DỰ KIẾN |
Bước 1: Chuyển giao nhiệm vụ: GV gợi ý để HS rút ra các khái niệm chất điện li mạnh. GV nhắc lại đặc điểm cấu tạo của tinh thể NaCl là tinh thể ion, các ion âm và dương phân bố đều đặn tại các nút mạng. GV khi cho tinh thể NaCl vào nước thì có hiện tượng gì xảy ra? GV kết luận dưới tác dụng của các phân tử nước phân cực. Các ion Na+ và ion Cl- tách ra khỏi tinh thể đi vào dung dịch. Bước 2: Thực hiện nhiệm vụ: HS: Hoạt động nhóm hoàn thành phiếu học tập Bước 3: Báo cáo thảo luận - HĐ chung cả lớp: GV mời 4 nhóm báo cáo kết quả (mỗi nhóm 1 nội dung), các nhóm khác góp ý, bổ sung, phản biện. Bước 4: Kết luận, nhận định: GV chốt lại kiến thức. | a. Chất điện li mạnh - Chất điện li mạnh là chất khi tan trong nước các phân tử hoà tan đều phân li ra ion.
NaCl → Na+ + Cl- Chất điện li mạnh bao gồm Các axit mạnh như HNO3, H2SO4, HClO4, HClO3, HCl, HBr, HI, HMnO4... Các bazơ mạnh như NaOH, Ba(OH)2... Hầu hết các muối.
|
Hoạt động 5: Chất điện li yếu
- a) Mục tiêu: Hiểu được nội dung bài học, các khái niệm, định nghĩa có liên quan.
- b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
- c) Sản phẩm: HS vận dụng kiến thức đã học để trả lời các câu hỏi và phiếu bài tập.
- d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH | SẢN PHẨM DỰ KIẾN |
Bước 1: Chuyển giao nhiệm vụ: GV lấy Ví dụ CH3COOH để phân tích rồi giúp HS rút ra định nghĩa, đồng thời giáo viên cũng cung cấp cho HS cách biểu diễn trong phương trình điện li của chất điện li yếu Đặc điểm của quá trình điện li yếu? Chúng cũng tuân theo nguyên lí chuyển dịch cân bằng. Bước 2: Thực hiện nhiệm vụ: HS: Hoạt động nhóm hoàn thành phiếu học tập Bước 3: Báo cáo thảo luận - HĐ chung cả lớp: GV mời 4 nhóm báo cáo kết quả (mỗi nhóm 1 nội dung), các nhóm khác góp ý, bổ sung, phản biện. Bước 4: Kết luận, nhận định: GV chốt lại kiến thức. | b. Chất điện li yếu - Chất điện li yếu là chất khi tan trong nước chỉ có một phần phân li ra ion, phần còn lại tồn tại ở dạng phân tử trong dung dịch. Ví dụ CH3COOH D CH3COO- + H+ - Chất điện li yếu gồm axit có độ mạnh trung bình và yếu: CH3COOH, HCN, H2S, HClO, HNO2, H3PO4... bazơ yếu Mg(OH)2, Bi(OH)3... Một số muối của thuỷ ngân như Hg(CN)2, HgCl2...
|
- HOẠT ĐỘNG LUYỆN TẬP
- Mục tiêu: Củng cố, luyện tập kiến thức vừa học.
- Nội dung: Hoàn thành các câu hỏi trong phiếu bài tập.
- Sản phẩm: HS vận dụng các kiến thức vào giải quyết các bài tập
- Tổ chức thực hiện:
- Sự điện li, chất điện li là gì? Thế nào là chất điện li mạnh, điện li yếu? Cho Ví dụ và viết phản ứng minh hoạ.
- HOẠT ĐỘNG VẬN DỤNG
- a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
- Nội dung: Dạy học trên lớp, hoạt động nhóm, hoạt động cá nhân.
- Sản phẩm: Bài làm của học sinh, kĩ năng tính toán hóa học
- Tổ chức thực hiện:
Bài 1: Một dung dịch chứa x mol Na+, y mol Ca2+, z mol HCO3-, t mol Cl-. Viết biểu thức liên hệ giữa x, y, z, t .
Bài 2: Em hãy giải thích vì sao nước mưa, nước biển dẫn điện tốt?
* HƯỚNG DẪN VỀ NHÀ
Hướng dẫn HS tìm hiểu thêm các nội dung liên quan đến bài học. HD học sinh tự học, tự tìm hiểu về bài cũ và bài mới, đưa ra các câu hỏi mở rộng cho học sinh tham khảo

Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
=> Giáo án Hóa học 11 kì 1 soạn theo công văn 5512
Từ khóa: Giáo án powerpoint hóa 11, GA trình hóa học 11, GA điện tử hóa học lớp 11Tài liệu giảng dạy môn Hóa học THPT
