Giáo án powerpoint hóa học 10
Giáo án powerpoint hay còn gọi là giáo án điện tử, bài giảng điện tử, giáo án trình chiếu. Dưới đây là bộ giáo án powerpoint hóa học 10. Giáo án được thiết kế theo phong cách hiện đại, đẹp mắt để tạo hứng thú học tập cho học sinh. Với tài liệu này, hi vọng việc dạy môn hóa học 10 của thầy cô sẽ nhẹ nhàng hơn.
Click vào ảnh dưới đây để xem giáo án rõ




Xem video về mẫu Giáo án powerpoint hóa học 10
Một số tài liệu quan tâm khác
Phần trình bày nội dung giáo án
1. GIÁO ÁN POWERPOINT BAO GỒM ĐỦ CÁC BÀI TRONG HÓA HỌC 10
Chương 1: Các loại hợp chất vô cơ
- Bài 1: Thành phần nguyên tử
- Bài 2: Hạt nhân nguyên tử - Nguyên tố hóa học - Đồng vị
- Bài 3: Luyện tập: Thành phần nguyên tử
- Bài 4: Cấu tạo vỏ nguyên tử
- Bài 5: Cấu hình electron
- Bài 6: Luyện tập: Cấu tạo vỏ nguyên tử
Chương 2: Bảng tuần hoàn các nguyên tố hóa học và Định luật tuần hoàn
- Bài 7: Bảng tuần hoàn các nguyên tố hóa học
- Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
- Bài 9: Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học. Định luật tuần hoàn
- Bài 10: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Bài 11: Luyện tập: Bảng tuần hoàn, sự biến đổi tuần hoàn cấu hình electron nguyên tử và tính chất của các nguyên tố hóa học
Chương 3: Liên kết hóa họcBài 12: Liên kết ion - Tinh thể ion
- Bài 13: Liên kết cộng hóa trị
- Bài 14: Tinh thể nguyên tử và tinh thể phân tử
- Bài 15: Hóa trị và số oxi hóa
- Bài 16: Luyện tập: Liên kết hóa học
Chương 4: Phản ứng oxi hóa - khử
- Bài 17: Phản ứng oxi hóa khử
- Bài 18: Phân loại phản ứng trong hóa học vô cơ
- Bài 19: Luyện tập: Phản ứng oxi hóa - khử
- Bài 20: Bài thực hành số 1: Phản ứng oxi hóa khử
Chương 5: Nhóm Halogen
- Bài 21: Khái quát về nhóm halogen
- Bài 22: Clo
- Bài 23: Hiđro clorua - Axit clohiđric và muối clorua
- Bài 24: Sơ lược về hợp chất có oxi của Clo
- Bài 25: Flo - Brom - Iot
- Bài 26: Luyện tập: Nhóm halogen
- Bài 27: Bài thực hành số 2: Tính chất hóa học của khí clo và hợp chất của clo
- Bài 28: Bài thực hành số 3: Tính chất hóa học của brom và iot
- Bài tập chương Halogen: Clo và hợp chất của clo
Chương 6: Oxi - Lưu huỳnh
- Bài 29: Oxi - Ozon
- Bài 30: Lưu huỳnh
- Bài 31: Bài thực hành số 4. Tính chất của oxi, lưu huỳnh
- Bài 32: Hiđro sunfua - Lưu huỳnh đioxit - Lưu huỳnh trioxit
- Bài 33: Axit sunfuric - Muối sunfat
- Bài 34: Luyện tập: Oxi và lưu huỳnh
- Bài 35: Bài thực hành số 5. Tính chất các hợp chất của lưu huỳnh
Chương 7: Tốc độ phản ứng và cân bằng hóa học
- Bài 36: Tốc độ phản ứng hóa học
- Bài 37: Bài thực hành số 6. Tốc độ phản ứng hóa học
- Bài 38: Cân bằng hóa học
- Bài 39: Luyện tập: Tốc độ phản ứng và cân bằng hóa học
2. GIÁO ÁN WORD BÀI
Ngày soạn: / /202...
Ngày dạy: / /202...
Tiết 3. THÀNH PHẦN NGUYÊN TỬ
Môn học/Hoạt động giáo dục: Hoá học; lớp: 10
Thời gian thực hiện: tiết
- MỤC TIÊU
- Kiến thức
Học sinh đạt được các yêu cầu sau:
- Trình bày được thành phần của nguyên tử (nguyên tử vô cùng nhỏ; nguyên tử gồm 2 phần: hạt nhân và lớp vỏ nguyên tử; hạt nhân tạo nên bởi các hạt proton (p), neutron (n); Lớp vỏ tạo nên bởi các electron (e); điện tích, khối lượng mỗi loạihạt).
- So sánh được khối lượng của electron với proton và neutron, kích thước của hạt nhân với kích thước nguyêntử.
-I.1.a, I.2 ( HS tự đọc)
- II.Kích thước và khối lượng của nguyên tử (Hướng dẫn HS tự học)
- Năng lực :
Năng lực chung
+ Năng lực hợp tác;
+ Năng lực giải quyết vấn đề;
+ Năng lực tổng hợp kiến thức;
+ Năng lực làm việc tự học;
Năng lực chuyên biệt:
+ Năng lực sử dụng ngôn ngữ hóa học;
+ Năng lực vận dụng kiến thức hóa học vào thực tiễn.
- Phẩm chất
- Say mê, hứng thú, tự chủ trong học tập; trung thực; yêu khoa học.
- Biết cách đảm bảo an toàn khi thí nghiệm với các nguyên tố halogen
- Biết các ứng dụng của halogen trong cuộc sống.
- THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- 1. Giáo viên (GV)
- Làm các slide trình chiếu, giáo án
- Máy tính, trình chiếu Powerpoint.
- Phiếu học tập, nhiệm vụ cho các nhóm.
- 2. Học sinh (HS)
- Chuẩn bị theo các yêu cầu của GV.
- Tập lịch cũ cỡ lớn hoặc bảng hoạt động nhóm.
- Bút mực viết bảng.
III TIẾN TRÌNH DẠY HỌC
- HOẠT ĐỘNG KHỞI ĐỘNG
- a) Mục tiêu: Huy động kiến thức đã học của HS, tạo nhu cầu tiếp tục tìm hiểu kiến thức mới.
- Huy động các kiến thức đã được học về Bảng tuần hoàn ở HKI, tạo nhu cầu tiếp tục tìm hiểu kiến thức mới.
- Tìm hiểu các thông tin cơ bản của các nguyên tố halogen thông qua trò chơi “ AI NHANH HƠN ”?).
- b) Nội dung: Tái hiện các kiến thức về thành phần nguyên tử đã học.
- c) Sản phẩm: HS hoàn thành các nội dung trong PHT.
- d) Tổ chức thực hiện:
Hoạt động trải nghiệm ở nhà
- Hướng dẫn HS xem lại kiến thức đã học
- Các nhóm thảo luận và hoàn thành phiếu KWL.
Dự kiến một số khó khăn vướng mắc của học sinh: GV có thể gợi ý một số thông tin trước cho HS trong quá trình hoàn thành phiếu KWL: Thuật ngữ nguyên tử xuất hiện vào khoảng thời gian nào? Ai là người đầu tiên sử dụng thuật ngữ đó? - Quan điểm của Đê-mô-crit về nguyên tử? Theo em quan điểm đó của Đê-mô-crit đã đúng hoàn toàn chưa? - Hãy định nghĩa chính xác nguyên tử là gì? Thành phần cấu tạo của nguyên tử như thế nào?
Hoạt động ở lớp
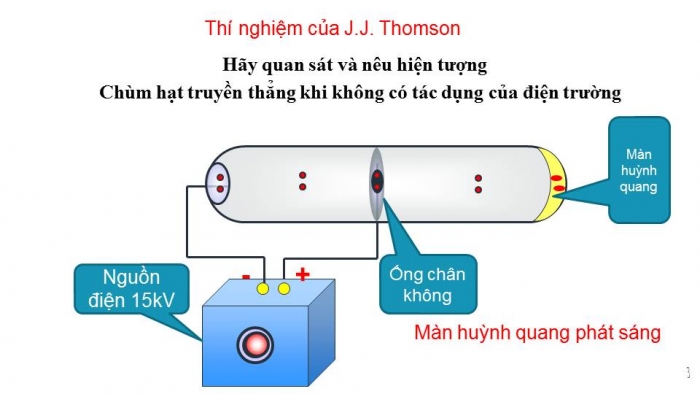
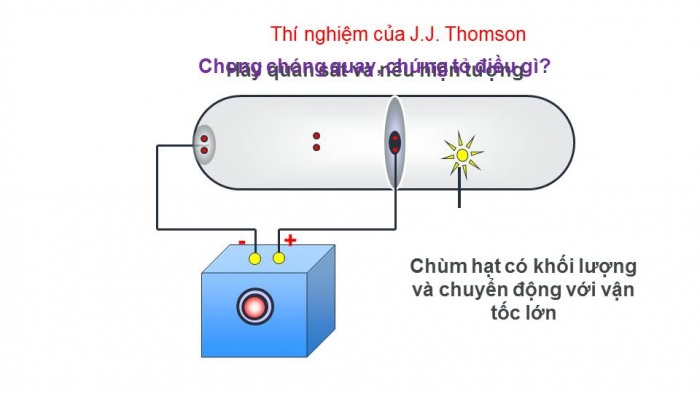
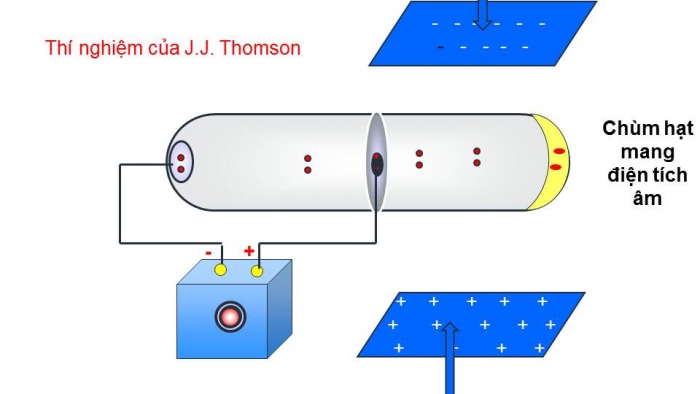
- GV cho HS quan sát video thí nghiệm:
+ Mô phỏng thí nghiệm tạo ra tia âm cực của nhà bác học người Anh Tom-xơn vào năm 1897.
+ Mô phỏng thí nghiệm tìm ra hạt nhân nguyên tử của nhà bác học Rơ-dơ-pho vào năm 1911.
- Hoạt động nhóm: HS hoàn thành phiếu học tập số 1.
- Hoạt động chung cả lớp: Mời một số nhóm lên báo cáo; nhóm khác bổ sung.
- HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
Hoạt động của GV - HS | Sản phẩm dự kiến |
Hoạt động 1: Thành phần cấu tạo của nguyên tử a) Mục tiêu: Sự tìm ra electron, hạt nhân nguyên tử, cấu tạo của hạt nhân nguyên tử. b) Nội dung: Trực quan, cả lớp làm việc với tài liệu, sách giáo khoa, tương tác với các câu hỏi vấn đáp tìm tòi của giáo viên, hoạt động nhóm, cá nhân. c) Sản phẩm: HS tóm lược kiến thức ghi vào vở, hoàn thành nội dung học tập. d) Tổ chức thực hiện: | |
Bước 1: Chuyển giao nhiệm vụ: - Tìm hiểu thành phần nguyên tử gồm + Electron : Sự tìm ra electron, khối lượng và điện tích của electron + Hạt nhân nguyên tử : sự tìm ra hạt nhân nguyên tử,câu tạo của hạt nhân nguyên tử gồm hạt proton và hạt notron. - Hoạt động cá nhân: Nghiên cứu SGK, tiếp tục hoàn chỉnh các câu hỏi trong PHT - Hoạt động nhóm: Trao đổi, giải thích cụ thể các kết quả thí nghiệm. - Hoạt động cả lớp: Mời đại diện nhóm trình bày, cả lớp hoàn chỉnh phần kiến thức. Bước 2: Thực hiện nhiệm vụ: HS: hoạt động cá nhân, hoạt động nhóm hoàn thành các phiếu học tập Bước 3: Báo cáo, thảo luận - GV gọi đại diện các nhóm trả lời câu hỏi trong phiếu học tập Bước 4: Kết luận, nhận định: - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. | I. Thành phần cấu tạo của nguyên tử: * Vỏ nguyên tử chứa electron
Những hạt tạo thành tia âm cực là các electron. * Hạt nhân gồm: proton nơtron - Nguyên tử có cấu tạo rỗng, phần mang điện tích dương là hạt nhân. Khối lượng nguyên tử hầu như tập trung ở hạt nhân. |
Hoạt động 2: Kích thước và khối lượng của nguyên tử a) Mục tiêu: Xác định được kích thước và khối lượng của nguyên tử. b) Nội dung: Trực quan, cả lớp làm việc với tài liệu, sách giáo khoa, tương tác với các câu hỏi vấn đáp tìm tòi của giáo viên, hoạt động nhóm, cá nhân. c) Sản phẩm: HS ghi vào vở để hoàn thành nội dung học tập. d) Tổ chức thực hiện: | |
Bước 1: Chuyển giao nhiệm vụ: - Tìm hiểu kích thước và khối lượng nguyên tử + Kích thước + Khối lượng nguyên tử tính theo kg và tính theo u - Hoạt động cá nhân: HS nghiên cứu SGK và hoàn thành PHT số 2 - Hoạt động nhóm: Trao đổi, thống nhất kết quả. - Hoạt động cả lớp: Mời đại diện nhóm trình bày, cả lớp hoàn chỉnh phần kiến thức. Bước 2: Thực hiện nhiệm vụ: HS: hoạt động cá nhân, hoạt động nhóm hoàn thành các phiếu học tập Bước 3: Báo cáo, thảo luận - GV gọi đại diện các nhóm trả lời câu hỏi trong phiếu học tập Bước 4: Kết luận, nhận định: - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. | II. Kích thước và khối lượng của nguyên tử: 1. Kích thước: - Nguyên tử của các nguyên tố khác nhau có kích thước khác nhau. - Đơn vị đo kích thước nguyên tử là và . (r nguyên tử : 10-1nm; r hạt nhân nguyên tử khoảng: 10-5nm; re,p: 10-8nm). Bán kính của nguyên tử H: 0,053 nm đường kính nguyên tử H: 0,106 nm. 2. Khối lượng: Dùng đơn vị khối lượng nguyên tử (u) (hay đvC). 1u bằng 1/12 khối lượng một nguyên tử đồng vị cacbon-12 ((19,9265.10-27kg). 1u = |
C+ D. HOẠT ĐỘNG LUYỆN TẬP – VẬN DỤNG
- a) Mục tiêu:
- Củng cố, khắc sâu các kiến thức đã học trong bài về thành phần cấu tạo; kích thước và khối lượng của nguyên tử.
- Tiếp tục phát triển các năng lực: tự học, sử dụng ngôn ngữ hóa học, phát hiện và giải quyết vấn đề thông qua môn hóa học.
Mở rộng kiến thức cho HS.
Giúp HS tăng thêm niềm đam mê khoa học, nghiên cứu khoa học.
- b) Nội dung: Dạy học trên lớp, hoạt động nhóm, hoạt động cá nhân.
- c) Sản phẩm: + HS xây dựng được sơ đồ tư duy về chuyên đề “Thành phần nguyên tử”.
+ Kết quả trả lời các câu hỏi trong PHT số 3.
Báo cáo sản phẩm của HS.
- d) Tổ chức thực hiện:
- Cho HS xây dựng sơ đồ tư duy về chuyên đề “Thành phần nguyên tử”
- Hoàn thành phiếu học tập số 3.
- HS hoạt động cặp đôi hoặc trao đổi nhóm nhỏ để cùng giải quyết câu hỏi trong phiếu học tập số 3.
- HĐ chung cả lớp: GV mời một số HS lên trình bày kết quả, các HS khác góp ý, bổ sung. GV giúp HS nhận ra những chỗ sai sót cần chỉnh sửa và chuẩn hóa kiến thức/phương pháp giải bài tập.
HS về nhà đọc thêm tư liệu, lịch sử tìm ra mô hình nguyên tử.
GV hướng dẫn HS tìm nguồn tài liệu tham khảo.
- Lồng ghép giáo dục biến đổi khí hậu về bảo vệ phóng xạ và giáo dục bảo vệ môi trường: đề phòng hiểm họa rò rỉ hạt nhân của các nhà máy điện nguyên tử và đề xuất xử lý chất thải trên cơ sở TCVL, TCHH của chúng.
- I CÂU HỎI/BÀI TẬP KIỂM TRA, ĐÁNH GIÁ
Mức độ nhận biết.
Câu 1: Phát biểu nào sau đây không chính xác?
- Các nguyên tử có cấu tạo rỗng gồm hạt nhân và vỏ electron.
- B. Tất cả các nguyên tử đều chứa đủ 3 loại hạt cơ bản proton, electron và nơtron.
- Hạt nhân nguyên tử được tạo bởi proton và nơtron.
- Vỏ nguyên tử được cấu tạo bởi các electron.
Câu 2: Phát biểu nào sau đây là đúng?
- Khối lượng nguyên tử bằng khối lượng của lớp vỏ electron.
- B. Khối lượng nguyên tử chủ yếu tập trung ở hạt nhân nguyên tử.
- Khối lượng nguyên tử bằng khối lượng hạt nhân nguyên tử.
- Khối lượng nguyên tử bằng tổng khối lượng các hạt proton.
Câu 3: Nguyên tử vàng (Au) có 79 electron ở vỏ nguyên tử. Điện tích hạt nhân của nguyên tử vàng là
- +79. B. -79. C. -1,26.10-17C. D. +1,26.10-17C.
Câu 4: Một nguyên tử có 12 proton và 12 nơtron trong hạt nhân. Điện tích của ion tạo thành khi nguyên tử này bị mất 2 electron là.
- A. 2+. 12+. C. 24+. D. 10+.
Câu 5: Nguyên tử natri có 11 electron ở vỏ nguyên tử và 12 nơtron trong hạt nhân. Tỉ số khối lượng giữa hạt nhân và nguyên tử natri là.
- A. B. 2,1. C. 0,92. D. 1,1.
Mức độ thông hiểu.
Câu 6: Nguyên tử X có 26 proton trong hạt nhân. Cho các phát biểu sau về X:
(1) X có 26 nơtron trong hạt nhân. (2) X có 26 electron ở vỏ nguyên tử.
(3) X có điện tích hạt nhân là 26+. (4) Khối lượng nguyên tử của X là 26u.
Trong các phát biểu trên, số phát biểu đúng là.
- 1. B. 2. C. 3. D. 4.
Câu 7: Một nguyên tử chỉ có 1 electron ở vỏ nguyên tử và hạt nhân nguyên tử có khối lượng là 5,01.10-24 gam. Số hạt proton và hạt nơtron trong hạt nhân nguyên tử này lần lượt là
- 1 và 0. B. 1 và 2. C. 1 và 3. D. 3 và 0.
Mức độ vận dụng.
Câu 8: Cho biết nguyên tử crom có khối lượng là 52u, bán kính nguyên tử này bằng 1,28. Khối lượng riêng của nguyên tử crom là.
- 2,47 g/cm3. B. 9,89 g/cm3. C. 5,20 g/cm3. D. 5,92 g/cm3.
Câu 9: Khối lượng riêng và khối lượng mol của canxi kim loại lần lượt là 1,55g/cm3 và 40g/mol. Giả thiết rằng, trong tinh thể canxi các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng. Tính bán kính nguyên tử canxi.
Câu 10: Nguyên tử vàng có bán kính và khối lượng mol lần lượt là 1,44 và 197g/mol. Biết rằng khối lượng riêng của vàng kim loại là 19,36g/cm3. Hỏi các nguyên tử vàng chiếm bao nhiêu % thể tích trong tinh thể.
- PHỤ LỤC
PHIẾU HỌC TẬP SỐ 1 Thảo luận nhóm trả lời nhanh các câu hỏi sau : Câu hỏi 1. Nguyên tử là gì? Nguyên tử có cấu tạo như thế nào? Câu hỏi 2. Từ các mô hình thí nghiệm, các em rút ra kết luận về: a. Sự tìm ra electron. b. Sự tìm ra hạt nhân nguyên tử. Câu hỏi 3. Cho biết các hạt cấu tạo nên nguyên tử, khối lượng và điện tích của các loại hạt đó. |
PHIẾU HỌC TẬP SỐ 2 Nội dung : Kích thước và khối lượng nguyên tử Hoạt động nhóm trả lời các câu hỏi sau : Câu hỏi 1. Nguyên tử có kích thước rất nhỏ, nếu coi nguyên tử là một khối cầu thì đường kính của nó khoảng bao nhiêu? Vậy kích thước và khối lượng nguyên tử, các loại hạt cấu tạo nên nguyên tử được biểu thị bằng đơn vị đo lường nào và giá trị của chúng bằng bao nhiêu? Bán kính của nguyên tử H bằng bao nhiêu? Câu hỏi 2. Có thể dùng đơn vị gam hay kg để đo khối lượng nguyên tử được không ? Tại sao người ta sử dụng đơn vị u (đvC) bằng 1/12 khối lượng nguyên tử C làm đơn vị ? Câu hỏi 3. Nguyên tử của các nguyên tố khác nhau có kích thước khác nhau không? |
PHIẾU HỌC TẬP SỐ 3 Luyện tập Trao đổi cặp đôi trả lời các câu hỏi và bài tập sau : Câu 1: Các hạt cấu tạo nên hầu hết các nguyên tử là: A. electron và proton. B. nơtron và electron. C. proton và nơtron. D. nơtron, electron và proton. Câu 2: Trong nguyên tử, hạt mang điện tích là A. electron. B. electron và proton. C. proton và nơtron. D. nơtron và electron. Câu 3: Tưởng tượng ta có thể phóng đại hạt nhân thành một quả bóng bàn có đường kính 4 cm thì đường kính của nguyên tử là bao nhiêu? Biết rằng đường kính của nguyên tử lớn hơn đường kính của hạt nhân khoảng 104 lần. A. 4 m. B. 40 m. C. 400 m. D. 4000 m. Câu 4: Khối lượng của 1 proton bằng khoảng bao nhiêu lần khối lượng của electron? A. lần. B. 1836 lần. C. lần. D. 1 lần. |

Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
=> Giáo án Hóa học 10 kì 1 soạn theo công văn 5512
Từ khóa: Giáo án powerpoint hóa 10, GA trình hóa học 10, GA điện tử hóa học lớp 10Tài liệu giảng dạy môn Hóa học THPT
