Giáo án powerpoint hóa học 11 cánh diều
Giáo án powerpoint hay còn gọi là giáo án điện tử, bài giảng điện tử, giáo án trình chiếu. Dưới đây là bộ giáo án powerpoint hóa học 11 sách cánh diều. Giáo án được thiết kế theo phong cách hiện đại, đẹp mắt để tạo hứng thú học tập cho học sinh. Với tài liệu này, hi vọng việc dạy môn hóa học 11 cánh diều của thầy cô sẽ nhẹ nhàng hơn
Click vào ảnh dưới đây để xem giáo án rõ









Xem video về mẫu Giáo án powerpoint hóa học 11 cánh diều
Một số tài liệu quan tâm khác
Phần trình bày nội dung giáo án
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI
KHỞI ĐỘNG
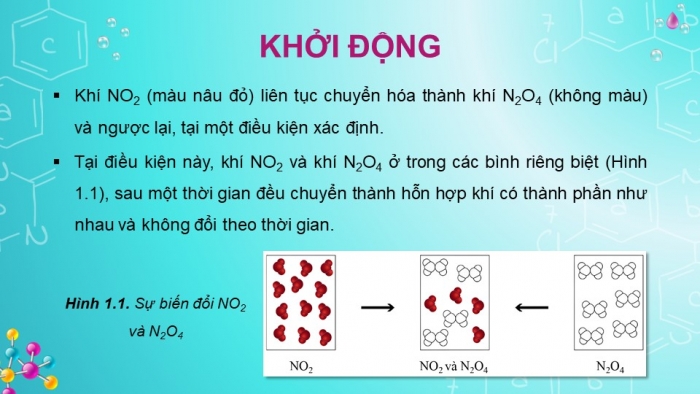
- Khí NO2 (màu nâu đỏ) liên tục chuyển hóa thành khí N2O4 (không màu) và ngược lại, tại một điều kiện xác định.
- Tại điều kiện này, khí NO2 và khí N2O4 ở trong các bình riêng biệt (Hình 1.1), sau một thời gian đều chuyển thành hỗn hợp khí có thành phần như nhau và không đổi theo thời gian.
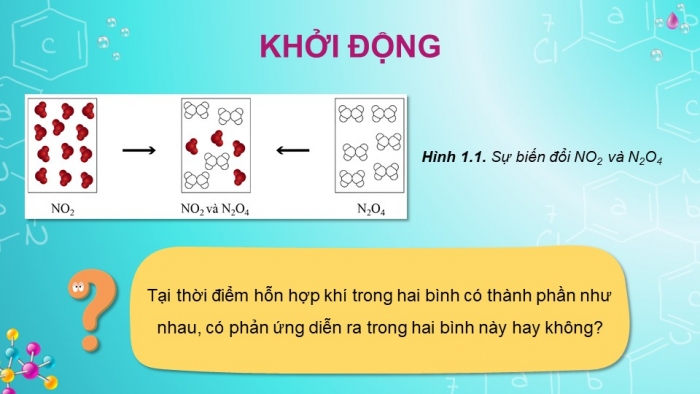
Hình 1.1. Sự biến đổi NO2 và N2O4
Câu hỏi:
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, có phản ứng diễn ra trong hai bình này hay không?
BÀI 1. MỞ ĐẦU VỀ CÂN BẰNG HOÁ HỌC
NỘI DUNG BÀI HỌC
- KHÁI NIỆM PHẢN ỨNG THUẬN NGHỊCH VÀ TRẠNG THÁI CÂN BẰNG
Cho phương trình hóa học sau:
- Fe(s) + 2HCl(aq) FeCl2(aq) + H2(g) (1)
Đặc điểm của phản ứng (1):
- Trong cùng điều kiện, FeCl2(aq) và H2(g) không thể biến đổi lại thành Fe(s) và HCl(aq) được.
- Phản ứng có đặc điểm như vậy được gọi là phản ứng một chiều.
Khái niệm
Phản ứng một chiều là phản ứng chỉ xảy ra theo chiều chất phản ứng biến đổi thành chất sản phẩm.
Ví dụ: Fe(s) + 2HCl(aq) FeCl2(aq) + H2(g)
Các chất sản phẩm không phản ứng lại được với nhau tạo thành chất ban đầu.
Vậy có phản ứng nào mà các chất sản phẩm phản ứng được với nhau để tạo thành chất ban đầu không?
Phản ứng thuận nghịch
HOẠT ĐỘNG CẶP ĐÔI: Tìm hiểu Ví dụ 1 (SGK tr.7) và trả lời câu hỏi
N2(g) + 3H2(g) 2NH3(g) (1)
Chiều các chất ban đầu tạo thành sản phẩm được gọi là chiều gì? => Chiều thuận
Chiều các chất sản phẩm tạo thành chất ban đầu được gọi là chiều gì? => Chiều nghịch
Phản ứng thuận nghịch là gì?
Phản ứng thuận nghịch
Khái niệm: Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
Bài tập
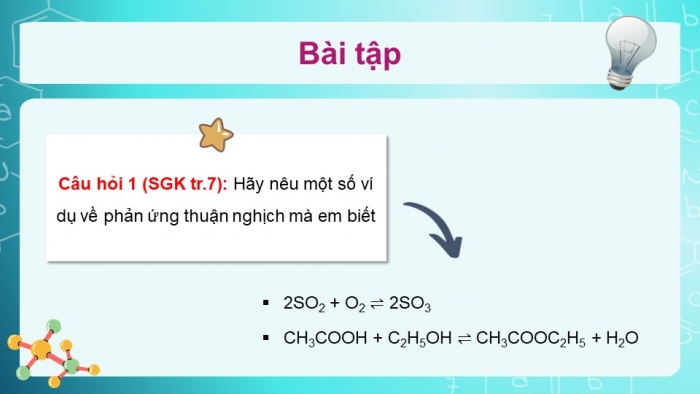
Câu hỏi 1 (SGK tr.7): Hãy nêu một số ví dụ về phản ứng thuận nghịch mà em biết
- 2SO2 + O2 2SO3
- CH3COOH + C2H5OH CH3COOC2H5 + H2O
Trạng thái cân bằng
HOẠT ĐỘNG NHÓM: Nghiên cứu về trạng thái cân bằng hóa học trong Ví dụ 2 (SGK tr.7, 8)
H2(g) + I2(g) 2HI (g)
Câu hỏi 2 (SGK tr.7). Xét Ví dụ 2:
- a) Giải thích vì sao màu tím của hỗn hợp khí lại nhạt dần so với lúc mới bắt đầu trộn hai khí H2 và I2 với nhau.
- b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của chất nào không thay đổi?
Câu hỏi 3 (SGK tr.7). Cho hai đồ thị (a) và (b) dưới đây. Mỗi đồ thị biểu diễn sự thay đổi tốc độ phản ứng thuận và tốc độ phản ứng nghịch theo thời gian:
Hãy cho biết đồ thị nào thể hiện đúng Ví dụ 2. Đường màu xanh trong đồ thị đó biểu diễn tốc độ phản ứng thuận hay tốc độ phản ứng nghịch?
H2(g) + I2(g) 2HI (g)
Câu hỏi 2. a) Sau khi trộn hai khí, phản ứng thuận diễn ra:
- b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi
Nồng độ H2 và I2 giảm dần => giảm dần => Màu tím của hỗn hợp giảm dần
=> Nồng độ của I2 không thay đổi nữa
Câu hỏi 3.
Đồ thị (a) thể hiện đúng Ví dụ 2
Đồ thị (a) thể hiện đúng Ví dụ 2
Nhận xét
Trong thí nghiệm:
- Lúc đầu: Phản ứng thuận có tốc độ lớn hơn phản ứng nghịch, ưu tiên tạo ra hydrogen iodine.
- Theo thời gian: Tốc độ phản ứng thuận giảm dần, tốc độ phản ứng nghịch tăng dần đến khi tốc độ hai phản ứng bằng nhau.
- Tại thời điểm này: Số mol của các chất hydrogen, iodine, hydrogen iodine không thay đổi nữa.
Thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng.
Trạng thái cân bằng
Khái niệm: Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
Trạng thái cân bằng
Cân bằng hóa học là một cân bằng động
Ở trạng thái cân bằng: Phản ứng thuận nghịch vẫn tiếp diễn với tốc độ bằng nhau
Ở trạng thái cân bằng: Nồng độ của một chất bất kì trong phản ứng không đổi
Bài tập
Câu hỏi 4 (SGK tr.8). Vì sao giá trị là một hằng số ở nhiệt độ xác định?
Lời giải:
- Ta có:
- Vì ở trạng thái cân bằng nồng độ của một chất bất kì trong phản ứng không đổi nên giá trị là một hằng số ở nhiệt độ xác định.
- BIỂU THỨC HẰNG SỐ CÂN BẰNG VÀ Ý NGHĨA
- Biểu thức hằng số cân bằng
Biểu thức tính tính hằng số cân bằng của phản ứng thuận nghịch tổng quát:
[M], [N], [A], [B]: Nồng độ mol của các chất M, N, A, B ở trạng thái cân bằng.
m, n, a, b: Hệ số tỉ lượng của các chất trong phương trình hóa học của phản ứng.
KC: Hằng số cân bằng của một phản ứng thuận nghịch.
Phụ thuộc nhiệt độ và bản chất của phản ứng.
Không phụ thuộc nồng độ ban đầu của các chất.
Lưu ý: Nồng độ chất rắn được coi bằng 1 và không có mặt trong biểu thức tính hằng số cân bằng
Lấy ví dụ về phản ứng thuận nghịch có mặt của chất rắn và viết biểu thức hằng số cân bằng của phản ứng?
C(s) + CO2(g) 2CO(g)
Bài tập
Câu hỏi 5 (SGK tr.9). Viết biểu thức hằng số cân bằng KC cho phản ứng thuận nghịch:
- a) N2(g) + 3H2(g) 2NH3(g)
- b) CaCO3(s) CaO(s) + CO2(g)
- a)
b)
Câu hỏi 6 (SGK tr.9). Viết biểu thức hằng số cân bằng KC cho phản ứng (*), (**) dưới đây.
H2(g) + I2(g) 2HI(g) (*) H2(g) + I2(g) HI(g) (**)
Theo em, giá trị hai hằng số cân bằng này có bằng nhau không?
(*):
(**):
Hai giá trị hằng số cân bằng này không bằng nhau
HOẠT ĐỘNG NHÓM: Đọc và tìm hiểu ý nghĩa biểu thức hằng số cân bằng qua các Ví dụ 3, 4 (SGK tr.9, 10)
Nhận xét: Dựa vào độ lớn của hằng số cân bằng có thể biết được:
- Nồng độ của chất tham gia hay chất sản phẩm là chiếm ưu thế ở trạng thái cân bằng.
- Phản ứng thuận có xảy ra thuận lợi hay không?
Hãy rút ra kết luận về ý nghĩa của biểu thức hằng số cân bằng?
- Nếu phản ứng thuận nghịch có KC rất lớn so với 1 thì phản ứng thuận diễn ra như thế nào? Các chất ở trạng thái cân bằng chủ yếu là chất nào?
- Nếu phản ứng thuận nghịch có KC rất nhỏ so với 1 thì phản ứng thuận diễn ra như thế nào? Các chất ở trạng thái cân bằng chủ yếu là chất nào?
KC phụ thuộc vào bản chất của phản ứng và nhiệt độ
KC rất lớn so với 1:
- Phản ứng thuận càng chiếm ưu thế
- Các chất ở trạng thái cân bằng chủ yếu là chất sản phẩm
KC rất nhỏ so với 1:
- Phản ứng nghịch càng chiếm ưu thế
- Các chất ở trạng thái cân bằng chủ yếu là chất ban đầu
Mở rộng kiến thức
Hằng số cân bằng lớn (hay nhỏ) chỉ:
- Cho biết phản ứng thuận diễn ra thuận lợi hay không thuận lợi.
- Không cho biết thời gian đạt đến trạng thái cân bằng là nhanh hay chậm.
-----------------Còn tiếp ------------------

Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
=> Giáo án hóa học 11 cánh diều
Từ khóa: Giáo án powerpoint hóa học 11 cánh diều, giáo án powerpoint hóa học 11 sách cánh diều, tải giáo án điện tử hóa học 11 cánh diều, GA powerpoint hóa học 11 cánh diều 2023Giáo án Powerpoint đủ các môn lớp 11 mới cánh diều, kết nối, chân trời
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 11 CÁNH DIỀU
GIÁO ÁN POWERPOINT LỚP 11 CÁNH DIỀU
GIÁO ÁN CHUYÊN ĐỀ LỚP 11 CÁNH DIỀU
Giáo án chuyên đề Công nghệ cơ khí 11 cánh diều đủ cả năm
Giáo án chuyên đề Tin học 11 Khoa học máy tính cánh diều đủ cả năm
Giáo án chuyên đề Tin học 11 Tin học ứng dụng cánh diều đủ cả năm
Giáo án chuyên đề Âm nhạc 11 cánh diều đủ cả năm
Giáo án chuyên đề Kinh tế pháp luật 11 cánh diều đủ cả năm
GIÁO ÁN DẠY THÊM LỚP 11 CÁNH DIỀU
Giáo án dạy thêm toán 11 cánh diều đủ cả năm
Giáo án dạy thêm ngữ văn 11 cánh diều đủ cả năm
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
