Giáo án điện tử KHTN 8 cánh diều: Bài tập (Chủ đề 1)
Bài giảng điện tử Khoa học tự nhiên 8 (Hoá học) cánh diều. Giáo án powerpoint Bài tập (Chủ đề 1). Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 8 cánh diều
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét











Xem toàn bộ: Giáo án điện tử hoá học 8 cánh diều
NHIỆT LIỆT CHÀO MỪNG CÁC EM ĐẾN VỚI TIẾT HỌC HÔM NAY!
KHỞI ĐỘNG
HOẠT ĐỘNG NHÓM
Nhớ lại các kiến thức đã học, không sử dụng tài liệu và hoàn thành Phiếu học tập.
- Biến đổi vật lí và biến đổi hoá học
Biến đổi vật lí là hiện tượng chất có sự biến đổi về trạng thái, hình dạng, kích thước,... nhưng vẫn giữ nguyên là chất ban đầu.
Biến đổi hóa học là hiện tượng chất có sự biến đổi tạo ra chất khác.
- Phản ứng hoá học và năng lượng của phản ứng hoá học
Phản ứng hóa học là quá trình biến đổi từ chất này thành chất khác
Phản ứng tỏa nhiệt là phản ứng tỏa ra năng lượng dưới dạng nhiệt
Phản ứng thu nhiệt là phản ứng thu vào năng lượng dưới dạng nhiệt
- Định luật bảo toàn khối lượng. Phương trình hoá học
Định luật bảo toàn khối lượng: Trong một phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất phản ứng.
Phương trình hóa học: Là cách thức biểu diễn phản ứng hóa học bằng công thức hóa học của các chất phản ứng và các chất sản phẩm.
Các bước lập phương trình hoá học
Bước 1: Viết sơ đồ của phản ứng
Bước 2: So sánh số nguyên tử của mỗi nguyên tố có trong phân tử các chất phản ứng và các chất sản phẩm
Bước 3: Cân bằng số nguyên tử của mỗi nguyên tố
Bước 4: Kiểm tra và viết phương trình hóa học
- Mol và tỉ khối của chất khí
- Khối lượng mol (kí hiệu là M) của một chất là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó.
- Công thức chuyển đổi giữa số mol (n) và khối lượng (m):
(mol)
- Công thức chuyển đổi giữa số mol (n) và thể tích của chất khí (V) ở đkc: (mol)
- Công thức tính tỉ khối của khí A đối với khí B:
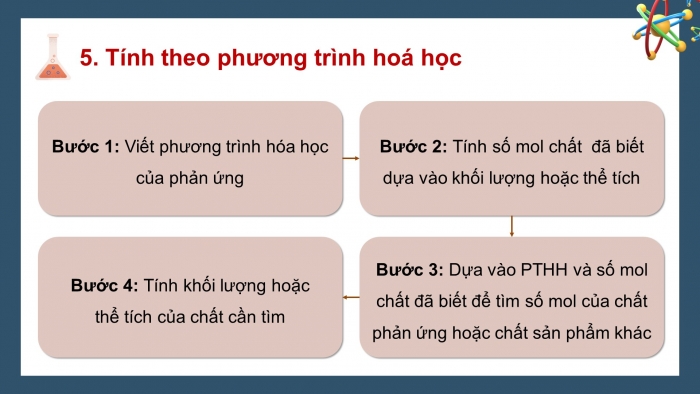
- Tính theo phương trình hoá học
Bước 1: Viết phương trình hóa học của phản ứng
Bước 2: Tính số mol chất đã biết dựa vào khối lượng hoặc thể tích
Bước 4: Tính khối lượng hoặc thể tích của chất cần tìm
Bước 3: Dựa vào PTHH và số mol chất đã biết để tìm số mol của chất phản ứng hoặc chất sản phẩm khác
Hiệu suất phản ứng: là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
- Nồng độ dung dịch
Dung dịch:
Là hỗn hợp lỏng đồng nhất của chất tan và dung môi.
Độ tan:
Độ tan (kí hiệu là S) của một chất trong nước là số gam chất đó hòa tan trong 100 g nước để tạo thành dung dịch bão hòa ở một nhiệt độ, áp suất xác định.
- Nồng độ phần trăm (kí hiệu là C%) của một dung dịch là số gam chất tan có trong 100 gam dung dịch.
- Nồng độ mol (kí hiệu là CM) của một dung dịch là số mol chất tan có trong 1 lít dung dịch.
- 7. Tốc độ phản ứng và chất xúc tác
- Tốc độ phản ứng là đại lượng chỉ mức độ nhanh hay chậm của một phản ứng hóa học.
- Các yếu tố ảnh hưởng đến tốc độ phản ứng:
- Diện tích bề mặt tiếp xúc
- Nhiệt độ
- Nồng độ các chất phản ứng
- Chất xúc tác
- Chất ức chế
LUYỆN TẬP
Bài 1 (SGK - tr.46)
- a) Hiện nay, gas thường được dùng làm nhiên liệu để đun nấu. Quá trình nào có sự biến đổi hóa học xảy ra trong các quá trình diễn ra dưới đây?
(1) Các chất khí (chủ yếu là butane và propane) được nén ở áp suất cao, hóa lỏng và tích trữ ở bình gas.
(2) Khi mở khóa bình gas, gas lỏng trong bình chuyển lại thành khí.
(3) Gas bắt lửa và cháy trong không khí chủ yếu tạo thành khí carbon dioxide và nước.
- b) Gas thường rất dễ bắt cháy lại không mùi lên rất nguy hiểm nếu bị rò gỉ. Để dễ nhận biết, các nhà sản xuất thường bổ sung một khí có mùi vào bình gas. Theo em, cần làm gì nếu ngửi thấy có mùi gas trong nhà?
Khóa van gas
Mở hết các cửa sổ
Thông báo cho mọi người
Video: Xử lí khi phát hiện có mùi gas trong nhà
Bài 2 (SGK - tr46). Đốt cháy hoàn toàn 9 gam kim loại magnesium trong oxygen thu được 15 gam magnesium oxide.
- Viết phương trình hoá học của phản ứng xảy ra.
- Viết phương trình bảo toàn khối lượng của các chất trong phản ứng.
- Tính khối lượng oxygen đã phản ứng.
Giải
- a) Phương trình hóa học của phản ứng:
2Mg + O2 ⟶ 2MgO
- b) Phương trình bảo toàn khối lượng của các chất trong phản ứng:
mMg + mO2 = mMgO
- c) Khối lượng oxygen đã phản ứng:
mO2 = mMgO – mMg = 15 – 9 = 6 (gam)
Bài 3 (SGK - tr.46). Cho các sơ đồ phản ứng sau:
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 8 cánh diều
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 8 CÁNH DIỀU
GIÁO ÁN POWERPOINT LỚP 8 CÁNH DIỀU
GIÁO ÁN DẠY THÊM LỚP 8 CÁNH DIỀU
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
