Giáo án điện tử KHTN 8 cánh diều Bài 12: Muối (P1)
Bài giảng điện tử Khoa học tự nhiên 8 (Hoá học) cánh diều. Giáo án powerpoint Bài 12: Muối (P1). Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 8 cánh diều
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét






Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 8 cánh diều
CHÀO MỪNG CÁC EM ĐẾN VỚI TIẾT HÓA HỌC!
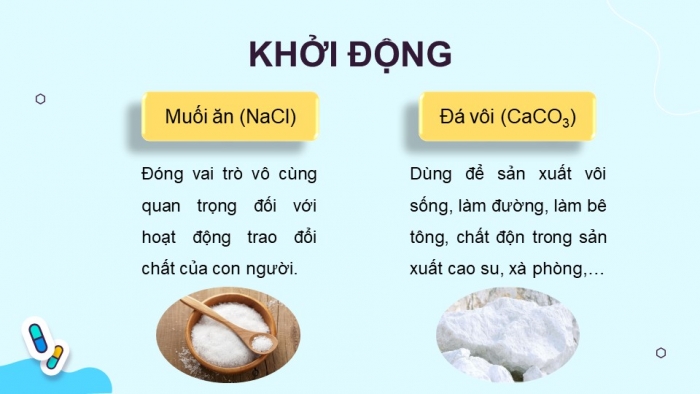
KHỞI ĐỘNG
Muối ăn (NaCl)
Đóng vai trò vô cùng quan trọng đối với hoạt động trao đổi chất của con người.
Đá vôi (CaCO3)
Dùng để sản xuất vôi sống, làm đường, làm bê tông, chất độn trong sản xuất cao su, xà phòng,…
- Các em hãy cho biết muối ăn và đá vôi có nhiều ở đâu?
- Chúng có những ứng dụng gì trong đời sống sản xuất?
BÀI 12. MUỐI
NỘI DUNG BÀI HỌC
Khái niệm muối
Tên gọi của muối
Tính tan của muối
Tính chất hóa học của muối
Mối quan hệ giữa acid, base, oxide và muối
Một số phương pháp điều chế muối.
I KHÁI NIỆM MUỐI
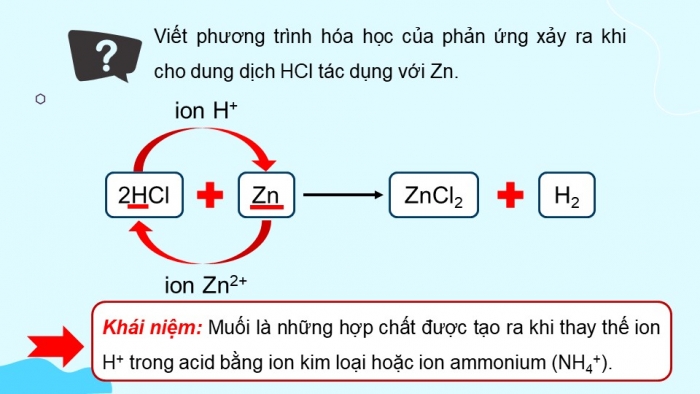
Viết phương trình hóa học của phản ứng xảy ra khi cho dung dịch HCl tác dụng với Zn.
2HCl
ion H+
ion Zn2+
Zn
ZnCl2
H2
Khái niệm: Muối là những hợp chất được tạo ra khi thay thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium (NH4+).
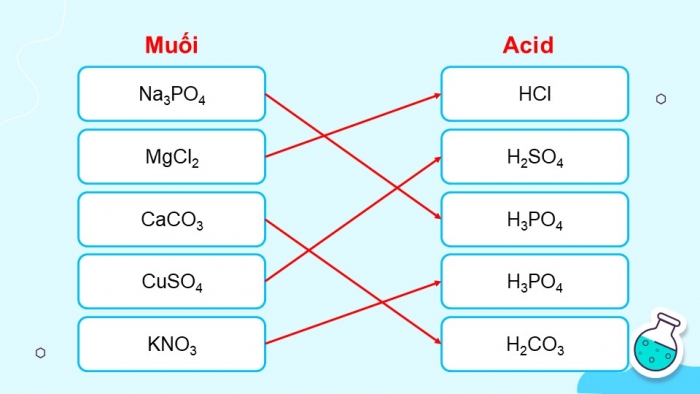
Cho biết các muối Na3PO4, MgCl2, CaCO3, CuSO4, và KNO3 tương ứng với acid nào trong số các acid sau: HCl, H2SO4, H3PO4, HNO3, H2CO3.
Muối
|
| Acid
|
Na3PO4
|
| HCl
|
MgCl2
|
| H2SO4
|
CaCO3
|
| H3PO4
|
CuSO4
|
| H3PO4
|
KNO3
|
| H2CO3
|
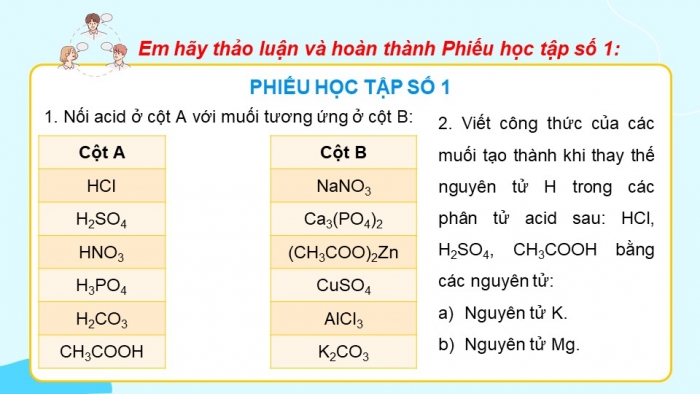
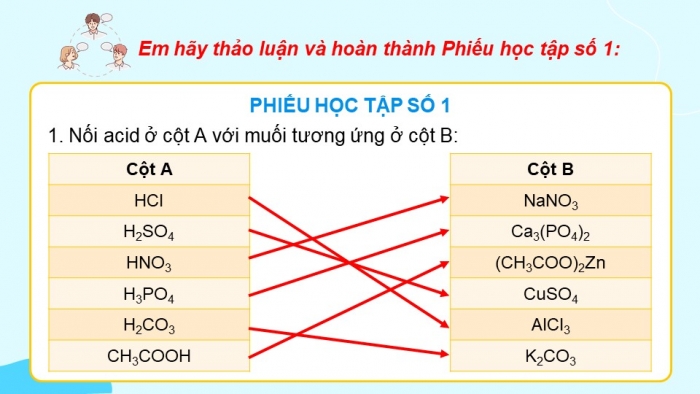
Em hãy thảo luận và hoàn thành Phiếu học tập số 1:
PHIẾU HỌC TẬP SỐ 1
- Nối acid ở cột A với muối tương ứng ở cột B:
Cột A | Cột B | |
HCl | NaNO3 | |
H2SO4 | Ca3(PO4)2 | |
HNO3 | (CH3COO)2Zn | |
H3PO4 | CuSO4 | |
H2CO3 | AlCl3 | |
CH3COOH | K2CO3 |
- Viết công thức của các muối tạo thành khi thay thế nguyên tử H trong các phân tử acid sau: HCl, H2SO4, CH3COOH bằng các nguyên tử:
- Nguyên tử K.
- Nguyên tử Mg.
- Viết công thức của các muối tạo thành khi thay thế nguyên tử H trong các phân tử acid sau: HCl, H2SO4, CH3COOH bằng các nguyên tử:
- a) Nguyên tử K: ….....................................................................................
….................................................................................................................
…................................................................................................................
- b) Nguyên tử Mg: …...................................................................................
…................................................................................................................
…................................................................................................................
KCl, K2SO4, CH3COOK
MgCl2, MgSO4, (CH3COO)2Mg
II TÊN GỌI CỦA MUỐI
Em hãy quan sát Bảng 12.1 và rút ra cách gọi tên muối của một số acid.
Kết luận
Cách gọi tên
Tên kim loại + Tên muối của acid (tên gốc acid
Tên muối
Copper (II) sulfate
Potassium phosphate
Trường hợp kim loại có nhiều hóa trị cần thêm hóa trị của kim loại trong tên gọi của muối.
BẢNG TÊN GỌI MỘT SỐ GỐC ACID | |||
Gốc acid | Tên gọi | Gốc acid | Tên gọi |
-Cl | chloride | -CH3COO | acetate |
-Br | bromide | =S | sulfide |
-I | iodide | -HS | hydrogensulfide |
-NO3 | nitrate | =CO3 | carbonate |
=SO4 | sulfate | -HCO3 | hydrogencarbonate |
-HSO4 | hydrogensulfate | ≡PO4 | phosphate |
=SO3 | sulfite | =HPO4 | hydrogenphosphate |
Em hãy trả lời Luyện tập 1 – SGK tr.63: Gọi tên các muối sau: KCl, ZnSO4, MgCO3, Ca3(PO4)2, Cu(NO3)2, Al2(SO4)3.
Muối | Tên các muối |
KCl | |
ZnSO4 | |
MgCO3 | |
Ca3(PO4)2 | |
Cu(NO3)2 | |
Al2(SO4)3 |
III TÍNH TAN CỦA MUỐI
PHỤ LỤC. BẢNG TÍNH TAN TRONG NƯỚC CỦA MỘT SỐ ACID – BASE – MUỐI | ||||||||||||
Nhóm hydroxide và gốc acid | HYDROGEN VÀ CÁC KIM LOẠI | |||||||||||
H+ | K+ | Na+ | Ag+ | Mg2+ | Ca2+ | Ba2+ | Zn2+ | Cu2+ | Fe2+ | Fe3+ | Al3+ | |
OH- | t | t | − | k | i | t | k | k | k | k | k | |
Cl- | t/b | t | t | k | t | t | t | t | t | t | t | t |
NO3- | t/b | t | t | t | t | t | t | t | t | t | t | t |
SO42- | t/kb | t | t | i | t | i | k | t | t | t | t | t |
CO32- | t/b | t | t | k | k | k | k | k | k | k | − | − |
PO43- | t/kb | t | t | k | k | k | k | k | k | k | k | k |
T: hợp chất tan được trong nước. K: hợp chất không tan. i: hợp chất ít tan | B: hợp chất bay hơi hoặc dễ phân hủy thành khí bay lên. Kb: hợp chất không bay hơi. Vạch ngang “-”: hợp chất không tồn tại/bị phân hủy trong nước. | |||||||||||
Dựa vào bảng tính tan, em hãy kể tên một số muối tan, muối ít tan và muối không tan.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 8 cánh diều
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 8 CÁNH DIỀU
GIÁO ÁN POWERPOINT LỚP 8 CÁNH DIỀU
GIÁO ÁN DẠY THÊM LỚP 8 CÁNH DIỀU
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
