Giáo án điện tử KHTN 8 cánh diều Bài 7: Tốc độ phản ứng và chất xúc tác
Bài giảng điện tử Khoa học tự nhiên 8 (Hoá học) cánh diều. Giáo án powerpoint Bài 7: Tốc độ phản ứng và chất xúc tác. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 8 cánh diều
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét










Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 8 cánh diều
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI
KHỞI ĐỘNG
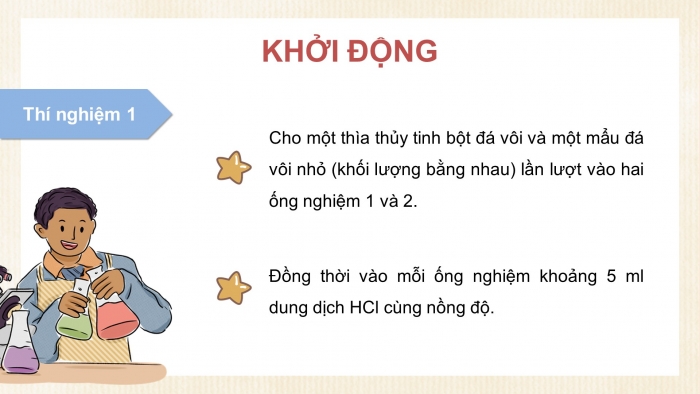
Thí nghiệm 1
Cho một thìa thủy tinh bột đá vôi và một mẩu đá vôi nhỏ (khối lượng bằng nhau) lần lượt vào hai ống nghiệm 1 và 2.
Đồng thời vào mỗi ống nghiệm khoảng 5 ml dung dịch HCl cùng nồng độ.
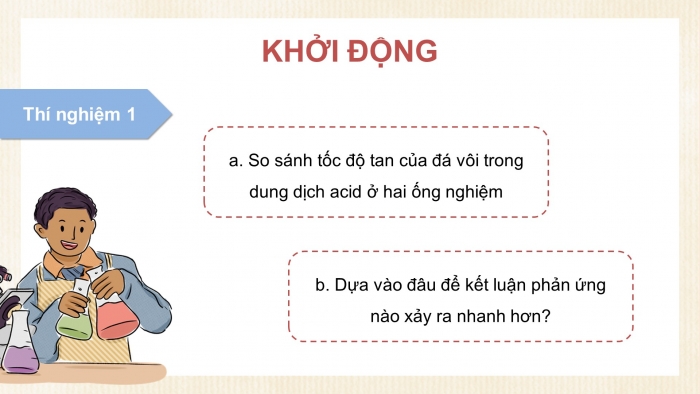
- So sánh tốc độ tan của đá vôi trong dung dịch acid ở hai ống nghiệm
- Dựa vào đâu để kết luận phản ứng nào xảy ra nhanh hơn?
BÀI 7. TỐC ĐỘ PHẢN ỨNG VÀ CHẤT XÚC TÁC
NỘI DUNG BÀI HỌC
Tốc độ của phản ứng hoá học là gì?
Các yếu tố ảnh hưởng đến tốc độ của phản ứng hoá học
- TỐC ĐỘ CỦA PHẢN ỨNG HOÁ HỌC
Các phản ứng hóa học xảy ra với tốc độ rất nhanh nhưng cũng có phản ứng xảy ra rất chậm.
Khi vắt chanh vào nước rau muống, lập tức nước rau muống chuyển vàng.
® Đây là phản ứng xảy ra nhanh.
Ủ vài ngày xôi nếp để lên men thành rượu nếp là phản ứng xảy ra chậm.
Câu hỏi 1 (SGK tr.41): Quan sát Hình 7.1 và cho biết phản ứng nào xảy ra nhanh hơn, phản ứng nào xảy ra chậm hơn.
Phản ứng đốt cháy cồn xảy ra nhanh hơn so với sự gỉ của sắt
Khái niệm
Tốc độ của phản ứng hóa học là đại lượng chỉ mức độ nhanh hay chậm của một phản ứng hóa học.
Luyện tập 1 (SGK tr.42). Trường hợp nào có phản ứng xảy ra với tốc độ nhanh hơn trong hai trường hợp sau:
- Để que đóm còn tàn đỏ ở ngoài không khí
- Đưa que đóm còn tàn đỏ vào bình chứa oxygen
- Trường hợp b) có phản ứng xảy ra với tốc độ nhanh hơn vì que đóm cháy trong khí oxygen nguyên chất.
- Trường hợp a) que đóm cháy trong không khí (thành phần oxygen chỉ chiếm xấp xỉ 21%)
- CÁC YẾU TỐ ẢNH HƯỞNG ĐẾN TỐC ĐỘ CỦA PHẢN ỨNG HOÁ HỌC
- Ảnh hưởng của diện tích lên bề mặt tiếp xúc
Thí nghiệm 1
Ở ống nghiệm 1: bọt khí thoát ra nhanh hơn và bột đá vôi trong dung dịch acid tan nhanh hơn ống nghiệm 2
Dựa vào dấu hiệu tan của đá vôi nhanh hơn hay chậm hơn để kết luận phản ứng trong ống nghiệm 1 nhanh hơn ống nghiệm 2
Nếu chia một vật thành nhiều phần nhỏ thì tổng diện tích bề mặt sẽ như thế nào?
Tăng lên
Diện tích bề mặt tiếp xúc càng lớn, tốc độ phản ứng sẽ như thế nào?
Càng nhanh
Diện tích bề mặt tiếp xúc có ảnh hưởng đến tốc độ của phản ứng hóa học.
Diện tích bề mặt tiếp xúc càng lớn, tốc độ phản ứng càng nhanh.
> Ví dụ: Nấu cháo từ bột gạo sẽ nhanh hơn nấu cháo từ hạt gạo.
Luyện tập 2 (SGK tr.42): Cho cùng một lượng Zn hạt và Zn bột vào hai ống nghiệm 1 và 2. Sau đó, cho cùng một thể tích dung dịch HCl dư cùng nồng độ vào hai ống nghiệm. Dự đoán lượng Zn ở ống nghiệm nào sẽ tan hết trước.
Dự đoán: Zn ở ống nghiệm 2 sẽ tan hết trước do diện tích tiếp xúc với dung dịch HCl của Zn dạng bột lớn hơn dạng hạt.
- Ảnh hưởng của nhiệt độ
Hoạt động nhóm:
Tiến hành thí nghiệm 2 để tìm hiểu ảnh hưởng của nhiệt độ đến tốc độ phản ứng và trả lời các câu hỏi trong Phiếu học tập số 1.
Phiếu học tập số 1
Câu 1. Hiện tượng thí nghiệm 2: Ở ống nghiệm 1, bọt khí thoát ra nhanh và nhiều hơn ống nghiệm 2. Có bọt khí thoát ra là do có PƯHH sau:
Fe + H2SO4 FeSO4 + H2
Giải thích: Tốc độ của phản ứng ở ống nghiệm 1 nhanh hơn ở ống nghiệm 2 do ống nghiệm 1 được đun nóng lên.
Câu 2.
Nhận xét ảnh hưởng của nhiệt độ đến tốc độ phản ứng: Khi tăng nhiệt độ, phản ứng diễn ra với tốc độ nhanh hơn.
Trả lời câu hỏi Luyện tập 3 (SGK tr.43):
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 8 cánh diều
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 8 CÁNH DIỀU
GIÁO ÁN POWERPOINT LỚP 8 CÁNH DIỀU
GIÁO ÁN DẠY THÊM LỚP 8 CÁNH DIỀU
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
