Giáo án và PPT KHTN 8 cánh diều Bài 5: Tính theo phương trình hoá học
Đồng bộ giáo án word và powerpoint (ppt) Bài 5: Tính theo phương trình hoá học. Thuộc chương trình Khoa học tự nhiên 8 (Hoá học) cánh diều. Giáo án được biên soạn chỉnh chu, hấp dẫn. Nhằm tạo sự lôi cuốn và hứng thú học tập cho học sinh.
Click vào ảnh dưới đây để xem giáo án WORD rõ nét











Giáo án ppt đồng bộ với word









Còn nữa....
Các tài liệu bổ trợ khác
Xem toàn bộ: Trọn bộ giáo án và PPT Hoá học 8 cánh diều
BÀI 5: TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC
HOẠT ĐỘNG KHỞI ĐỘNG
GV yêu cầu HS quan sát hình ảnh và trả lời:
Trong công nghiệp, người ta sản xuất nhôm từ aluminium oxide (Al2O3). Làm thế nào tính được khối lượng nguyên liệu cần dùng để sản xuất nhôm hoặc tính khối lượng nhôm tạo ra nếu biết khối lượng nguyên liệu đã dùng?
HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
I. XÁC ĐỊNH KHỐI LƯỢNG, SỐ MOL CỦA CHẤT PHẢN ỨNG VÀ SẢN PHẨM TRONG PHẢN ỨNG HÓA HỌC
GV cho HS đọc thí nghiệm 1 và trả lời câu hỏi:
- Để tính khối lượng và số mol của chất phản ứng và chất sản phẩm trong một phản ứng hóa học, ta thực hiện theo các bước như thế nào?
- Đốt cháy hết 0,54 gam Al trong không khí thu được aluminium oxide theo sơ đồ phản ứng:
Al + O2![]() Al2O3
Al2O3
Lập phương trình hóa học của phản ứng và tính:
a) Khối lượng aluminium oxide tạo ra
b) Thể tích khí oxygen tham gia phản ứng ở điều kiện chuẩn
Sản phẩm dự kiến:
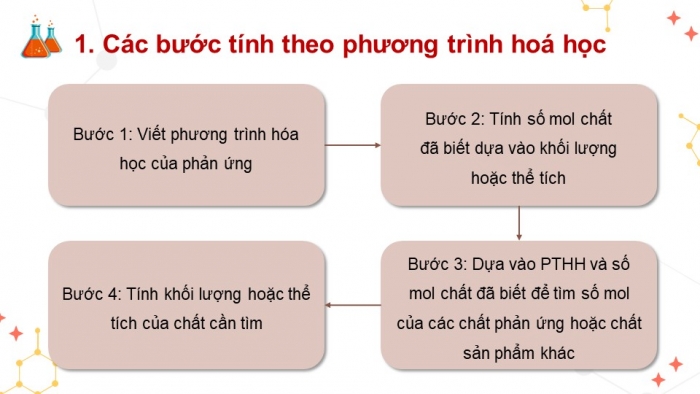
- Để tính khối lượng và số mol của chất phản ứng và chất sản phẩm trong một phản ứng hóa học, ta thực hiện theo các bước sau:
+Bước 1: Viết phương trình hóa học của phản ứng
+Bước 2: Tính số mol chất đã biết dựa vào khối lượng hoặc thể tích
+Bước 3: Dựa vào phương trình hóa học và số mol chất đã biết để tìm số mol của các chất phản ứng hoặc chất sản phẩm khác
+Bước 4: Tính khối lượng hoặc thể tích của chất cần tìm
- Phương trình hóa học của phản ứng :
![]() (mol)
(mol)
4Al + 3O2 ![]() 2Al2O3
2Al2O3
0,02 0,015 0,01
a) ![]() (gam)
(gam)
b) ![]() (lit)
(lit)
II. HIỆU SUẤT PHẢN ỨNG
Hoạt động 1: Chất phản ứng hết, chất phản ứng dư
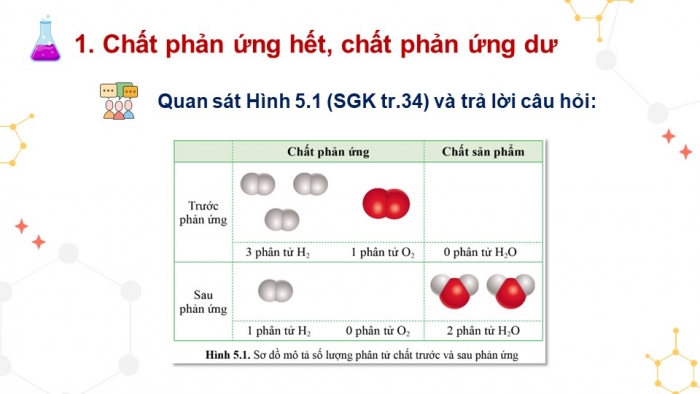
GV cho HS quan sát Hình 5.1 trang 34 SGK và trả lời câu hỏi:
- Cho biết số phân tử O2, H2 trước phản ứng, tham gia phản ứng và còn lại sau phản ứng?
- Cho biết số phân tử H2O tạo thành sau phản ứng.
- Khi phản ứng kết thúc, chất phản ứng nào hết và chất nào còn dư.
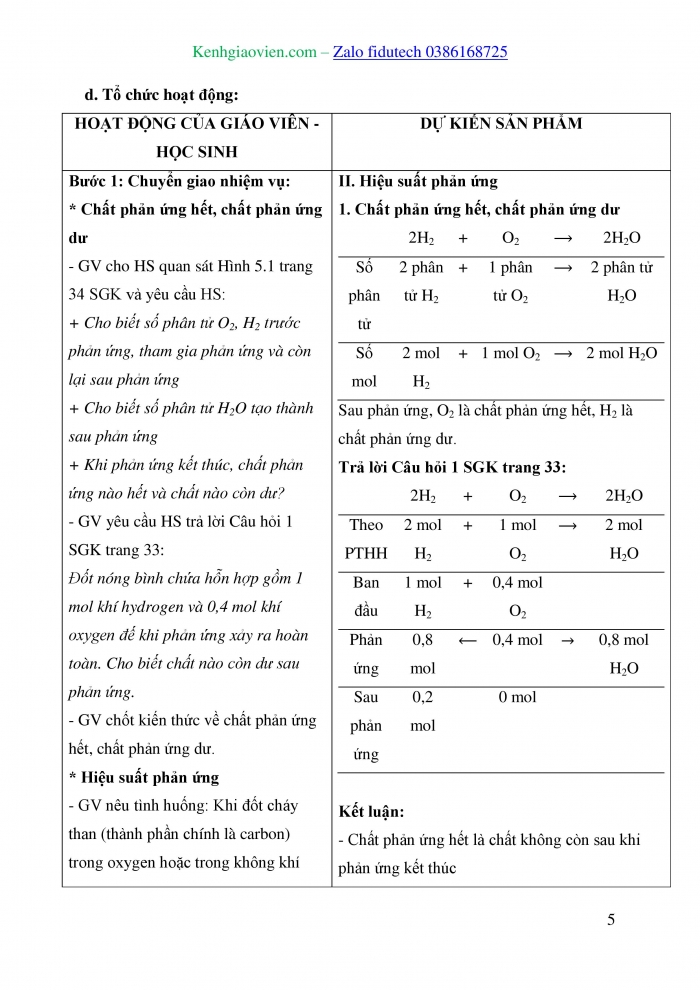
- Đốt nóng bình chứa hỗn hợp gồm 1 mol khí hydrogen và 0,4 mol khí oxygen đế khi phản ứng xảy ra hoàn toàn. Cho biết chất nào còn dư sau phản ứng.
Sản phẩm dự kiến:
| 2H2 | + | O2 |
| 2H2O |
Số phân tử | 2 phân tử H2 | + | 1 phân tử O2 |
| 2 phân tử H2O |
Số mol | 2 mol H2 | + | 1 mol O2 |
| 2 mol H2O |
Sau phản ứng, O2 là chất phản ứng hết, H2 là chất phản ứng dư.
| 2H2 | + | O2 |
| 2H2O |
Theo PTHH | 2 mol H2 | + | 1 mol O2 |
| 2 mol H2O |
Ban đầu | 1 mol H2 | + | 0,4 mol O2 |
|
|
Phản ứng | 0,8 mol |
| 0,4 mol |
| 0,8 mol H2O |
Sau phản ứng | 0,2 mol |
| 0 mol |
|
|
Hoạt động 2: Hiệu suất phản ứng
HS thảo luận trả lời câu hỏi:
- Hiệu suất phản ứng là gì?
- Hiệu suất phản ứng được tính bằng cách nào?
- Khi nào hiệu suất của phản ứng bằng 100%
Sản phẩm dự kiến:
- Hiệu suất phản ứng (kí hiệu là H) là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết
- Công thức hiệu suất phản ứng:
![]()
Trong đó:
+ H là hiệu suất phản ứng (%)
+mtt là khối lượng chất (gam) thu được theo thực tế
+mlt là khối lượng chất (gam) thu được theo lí thuyết (tính theo phương trình hóa học)
- Hiệu suất của phản ứng là 100% tức là phản ứng hóa học xảy ra hoàn toàn
HOẠT ĐỘNG LUYỆN TẬP
Câu 1: Khi tính toán theo phương trình hóa học, cần thực hiện mấy bước cơ bản?
A. 4 bước
B. 2 bước
C. 3 bước
D. 1 bước
Câu 2. Khối lượng vôi sống (CaO) thu được khi nung hoàn toàn đá vôi chứa 50 gam CaCO3 là
A. 27 gam
B. 26 gam
C. 28 gam
D. 29 gam
Câu 3. Cho phương trình phản ứng: Mg + 2HCl ![]() MgCl2 + H2
MgCl2 + H2
Biết rằng khi cho 8,4 g Mg tác dụng với dung dịch HCl thì thu được 23,275 g MgCl2. Hiệu suất của phản ứng là
A. 60%
B. 80%
C. 65%
D. 70%
Sản phẩm dự kiến:
Câu 1: A
Câu 2: C
Câu 3: D
HOẠT ĐỘNG VẬN DỤNG
Vận dụng kiến thức, GV yêu cầu HS trả lời câu hỏi:
Câu 1: Cho phương trình phản ứng: Ba + 2HCl ![]() BaCl2 + H2
BaCl2 + H2
Để thu được 4,16 g BaCl2 cần bao nhiêu mol HCl?
Câu 2: Cho phương trình phản ứng: S + O2 ![]() SO2. Biết khối lượng S là 3,2 g và hiệu suất của phản ứng là 80%. Tính V lít khí SO2 ở đkc.
SO2. Biết khối lượng S là 3,2 g và hiệu suất của phản ứng là 80%. Tính V lít khí SO2 ở đkc.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Trọn bộ giáo án và PPT Hoá học 8 cánh diều
TÀI LIỆU GIẢNG DẠY KHTN 8 (HOÁ HỌC) KẾT NỐI TRI THỨC
Giáo án hóa học 8 kết nối tri thức đủ cả năm
Giáo án điện tử hoá học 8 kết nối tri thức
Trò chơi khởi động Hoá học 8 kết nối tri thức
Video AI khởi động Hoá học 8 kết nối tri thức hấp dẫn
Giáo án tích hợp NLS Hoá học 8 kết nối tri thức
Câu hỏi và bài tập trắc nghiệm hóa học 8 kết nối tri thức
Đề thi hóa học 8 kết nối tri thức
File word đáp án hoá học 8 kết nối tri thức
Bài tập file word hoá học 8 kết nối tri thức
Kiến thức trọng tâm hóa học 8 kết nối tri thức
Đề kiểm tra 15 phút Hoá học 8 kết nối tri thức
Đề thi, đề kiểm tra cuối kì 2 hoá học 8 kết nối tri thức
Phiếu học tập theo bài Hoá học 8 kết nối tri thức cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 8 kết nối tri thức cả năm
Trắc nghiệm đúng sai Hoá học 8 kết nối tri thức cả năm
TÀI LIỆU GIẢNG DẠY KHTN 8 (HOÁ HỌC) CHÂN TRỜI SÁNG TẠO
Giáo án hóa học 8 chân trời sáng tạo
Giáo án powerpoint hóa học 8 chân trời sáng tạo
Video AI khởi động Hoá học 8 chân trời sáng tạo hấp dẫn
TÀI LIỆU GIẢNG DẠY KHTN 8 (HOÁ HỌC) CÁNH DIỀU
Giáo án hóa học 8 cánh diều đủ cả năm
Giáo án điện tử hoá học 8 cánh diều
Trò chơi khởi động Hoá học 8 cánh diều
Video AI khởi động Hoá học 8 cánh diều hấp dẫn
Câu hỏi và bài tập trắc nghiệm hóa học 8 cánh diều
Đề thi hóa học 8 cánh diều
File word đáp án hoá học 8 cánh diều
Bài tập file word Hoá học 8 cánh diều
Kiến thức trọng tâm hóa học 8 cánh diều
Đề kiểm tra 15 phút Hoá học 8 Cánh diều
Đề thi, đề kiểm tra cuối kì 2 hoá học 8 cánh diều
Phiếu học tập theo bài Hoá học 8 cánh diều cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 8 cánh diều cả năm
Trắc nghiệm đúng sai Hoá học 8 cánh diều cả năm
