Đề thi hoá học 9 chân trời sáng tạo có ma trận
Ma trận đề thi, đề kiểm tra Khoa học tự nhiên 9 (Hoá học) chân trời sáng tạo. Cấu trúc của đề thi gồm: trắc nghiệm, tự luận, cấu trúc điểm, bảng ma trận và bảng đặc tả. Bộ tài liệu có nhiều đề thi giữa kì 1, cuối kì 1, giữa kì 2, cuối kì 2. Tài liệu là bản word, có thể tải về và điều chỉnh những chỗ cần thiết. Hi vọng bộ đề thi tham khảo Hoá học 9 chân trời sáng tạo này giúp ích được cho thầy cô.
Click vào ảnh dưới đây để xem giáo án rõ





Một số tài liệu quan tâm khác
Phần trình bày nội dung giáo án
|
PHÒNG GD & ĐT ………………. |
Chữ kí GT1: ........................... |
|
TRƯỜNG THCS………………. |
Chữ kí GT2: ........................... |
ĐỀ KIỂM TRA GIỮA HỌC KÌ 1
HÓA HỌC 9 – CHÂN TRỜI SÁNG TẠO
NĂM HỌC: 2024 - 2025
Thời gian làm bài: 45 phút (Không kể thời gian phát đề)
|
Họ và tên: …………………………………… Lớp: ……………….. Số báo danh: …………………………….……Phòng KT:………….. |
Mã phách |
"
|
Điểm bằng số
|
Điểm bằng chữ |
Chữ ký của GK1 |
Chữ ký của GK2 |
Mã phách |
- PHẦN TRẮC NGHIỆM (4 điểm)
Khoanh tròn vào chữ cái đứng trước câu trả lời đúng:
Câu 1. Kim loại nào sau đây không tác dụng với dung dịch HCl?
- Mg.
- Na.
- Al.
- Ag.
Câu 2. Kim loại nào sau đây tác dụng với hơi nước ở nhiệt độ cao tạo thành oxide kim loại?
- Cu.
- Ag.
- Mg.
- Au.
Câu 3. Kim loại nào dưới đây khi tác dụng với oxygen có hiện tượng “tạo khói màu nâu đỏ”?
- Fe.
- Al.
- Zn.
- Au.
Câu 4. Dùng búa đập vào sợi dây nhôm, sợi dây bị cán mỏng dẹt ra. Điều này chứng tỏ nhôm có
- tính rắn chắc.
- tính bền.
- tính cứng.
- tính dẻo.
Câu 5. Phương pháp được sử dụng để điều chế các kim loại hoạt động hóa họa mạnh như Na, K, Ca từ các hợp chất muối của chúng là
- phương pháp nhiệt luyện.
- phương pháp điện phân nóng chảy.
- phương pháp thủy luyện.
- phương pháp điện phân dung dịch.
Câu 6. Dãy kim loại nào dưới đây được sắp xếp theo chiều hoạt động hóa học giảm dần?
- Al, Zn, Na.
- Mg, Al, Na.
- Pb, Al, Mg.
- Na, Mg, Zn.
Câu 7. Phương trình hóa học của phản ứng tách sắt ra khỏi hợp chất iron (III) oxide là
- Fe2O3+ 3CO 2Fe + 3CO2.
- 2FeS + 3O22FeO + 2SO2.
- 3Fe + 3O22Fe2O3.
- 3Zn + Fe2O33ZnO + 2Fe.
Câu 8. Có một mẫu dung dịch MgSO4 bị lẫn tạp chất là ZnSO4, có thể làm sạch mẫu dung dịch này bằng kim loại
- Cu.
- Zn.
- Mg.
- Fe.
- PHẦN TỰ LUẬN (6 điểm)
Câu 1. (3 điểm) Hãy cho biết hiện tượng xảy ra, viết các phương trình hóa học (nếu có) và giải thích khi cho thanh kim loại
- Ag vào dung dịch CuCl2.
- Zn vào dung dịch CuCl2.
- Cu vào dung dịch AgNO3.
- Zn vào dung dịch MgCl2.
Câu 2. (2 điểm) Cho 9,6 gam kim loại Mg vào 120 gam dung dịch HCl (vừa đủ).
- Viết phương trình hóa học xảy ra.
- Tính nồng độ phần trăm của dung dịch sau phản ứng.
Câu 3 (1 điểm) Để xác định tên một kim loại, một bạn hòa tan hoàn toàn 0,9 g kim loại đó trong dung dịch HCl 2,5 M thấy dùng hết 40 mL dung dịch. Hãy xác định kim loại trên (biết hóa trị của kim loại trong khoảng từ I đến III).
BÀI LÀM
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
TRƯỜNG THCS .............
HƯỚNG DẪN CHẤM KIỂM TRA GIỮA HỌC KÌ 1 (2023 – 2024)
MÔN: HÓA HỌC 9 – CHÂN TRỜI SÁNG TẠO
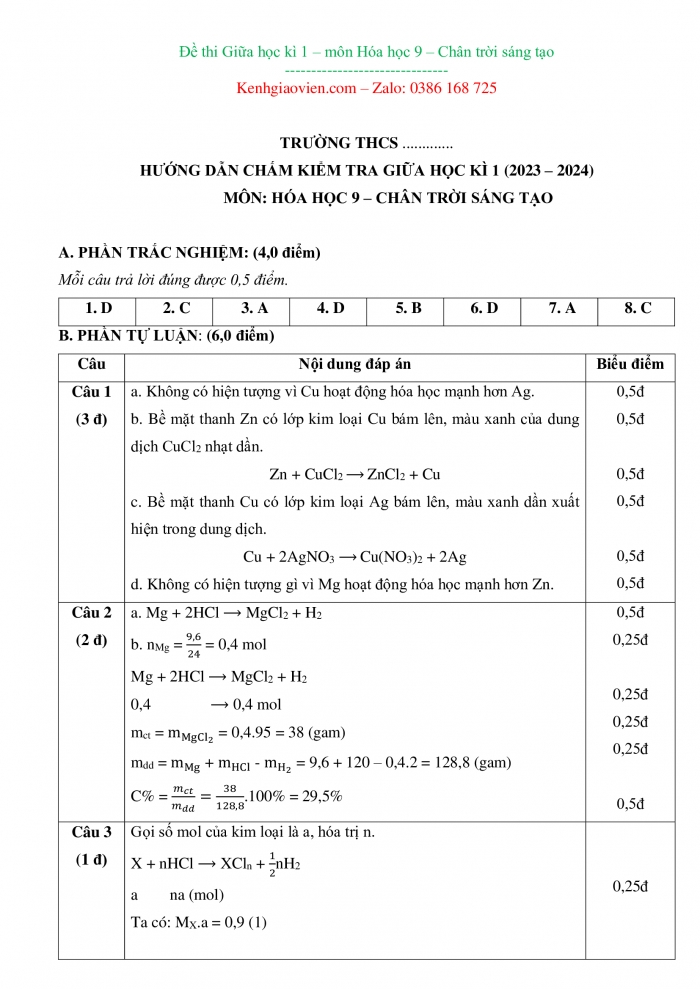
- A. PHẦN TRẮC NGHIỆM: (4,0 điểm)
Mỗi câu trả lời đúng được 0,5 điểm.
|
1. D |
2. C |
3. A |
4. D |
5. B |
6. D |
7. A |
8. C |
- PHẦN TỰ LUẬN: (6,0 điểm)
|
Câu |
Nội dung đáp án |
Biểu điểm |
||||||||
|
Câu 1 (3 đ) |
a. Không có hiện tượng vì Cu hoạt động hóa học mạnh hơn Ag. b. Bề mặt thanh Zn có lớp kim loại Cu bám lên, màu xanh của dung dịch CuCl2 nhạt dần. Zn + CuCl2 ZnCl2 + Cu c. Bề mặt thanh Cu có lớp kim loại Ag bám lên, màu xanh dần xuất hiện trong dung dịch. Cu + 2AgNO3 Cu(NO3)2 + 2Ag d. Không có hiện tượng gì vì Mg hoạt động hóa học mạnh hơn Zn. |
0,5đ 0,5đ
0,5đ 0,5đ
0,5đ 0,5đ |
||||||||
|
Câu 2 (2 đ) |
a. Mg + 2HCl MgCl2 + H2 b. nMg = = 0,4 mol Mg + 2HCl MgCl2 + H2 0,4 0,4 mol mct = = 0,4.95 = 38 (gam) mdd = + - = 9,6 + 120 – 0,4.2 = 128,8 (gam) C% = .100% = 29,5% |
0,5đ 0,25đ
0,25đ 0,25đ 0,25đ
0,5đ |
||||||||
|
Câu 3 (1 đ) |
Gọi số mol của kim loại là a, hóa trị n. X + nHCl XCln + nH2 a na (mol) Ta có: MX.a = 0,9 (1) na = 2,5.0,04 = 0,1 (2) Lấy (1) chia (2) ta có: = 9 Xét bảng sau:
Chọn cặp nghiệm n = 1; MX = 27 Vậy kim loại cần tìm là nhôm (Al) |
0,25đ
0,25đ
0,25đ 0,25đ |
TRƯỜNG THCS .............
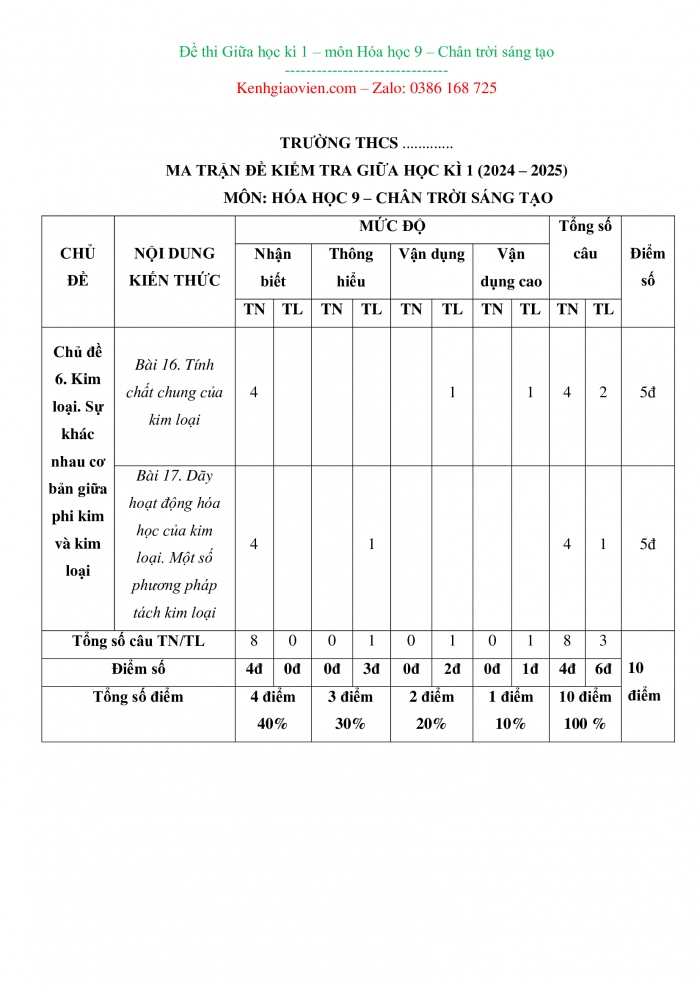
MA TRẬN ĐỀ KIỂM TRA GIỮA HỌC KÌ 1 (2024 – 2025)
MÔN: HÓA HỌC 9 – CHÂN TRỜI SÁNG TẠO
|
CHỦ ĐỀ |
NỘI DUNG KIẾN THỨC |
MỨC ĐỘ |
Tổng số câu |
Điểm số |
||||||||
|
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
|||||||||
|
TN |
TL |
TN |
TL |
TN |
TL |
TN |
TL |
TN |
TL |
|||
|
Chủ đề 6. Kim loại. Sự khác nhau cơ bản giữa phi kim và kim loại
|
Bài 16. Tính chất chung của kim loại |
4 |
|
|
|
|
1 |
|
1 |
4 |
2 |
5đ |
|
Bài 17. Dãy hoạt động hóa học của kim loại. Một số phương pháp tách kim loại |
4 |
|
|
1 |
|
|
|
|
4 |
1 |
5đ |
|
|
Tổng số câu TN/TL |
8 |
0 |
0 |
1 |
0 |
1 |
0 |
1 |
8 |
3 |
10 điểm |
|
|
Điểm số |
4đ |
0đ |
0đ |
3đ |
0đ |
2đ |
0đ |
1đ |
4đ |
6đ |
||
|
Tổng số điểm |
4 điểm 40% |
3 điểm 30% |
2 điểm 20% |
1 điểm 10% |
10 điểm 100 % |
|||||||
TRƯỜNG THCS .............
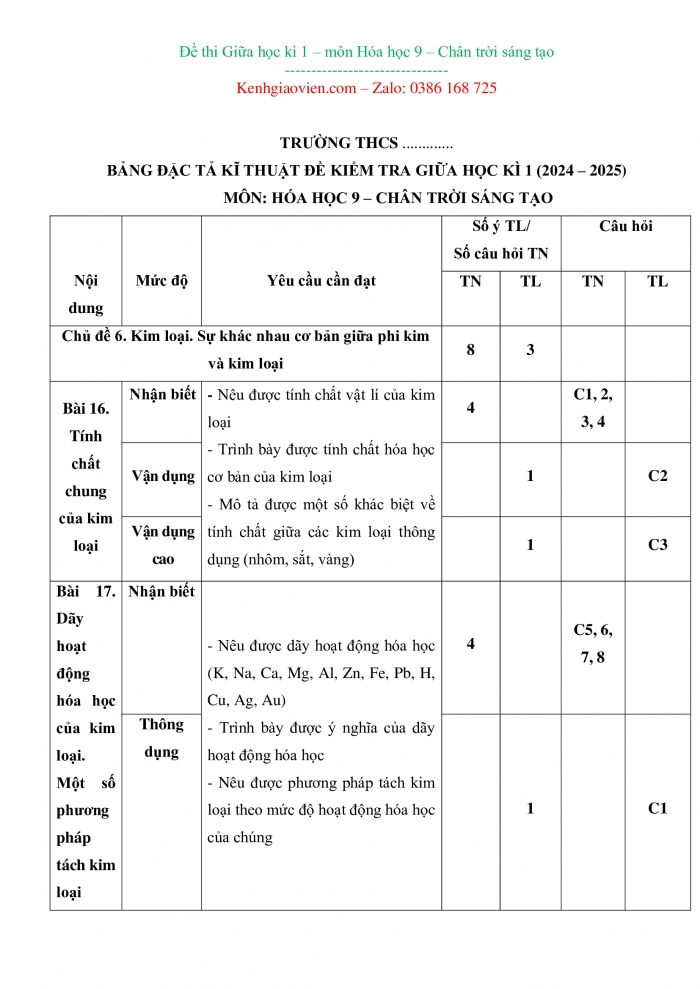
BẢNG ĐẶC TẢ KĨ THUẬT ĐỀ KIỂM TRA GIỮA HỌC KÌ 1 (2024 – 2025)
MÔN: HÓA HỌC 9 – CHÂN TRỜI SÁNG TẠO
|
Nội dung |
Mức độ |
Yêu cầu cần đạt |
Số ý TL/ Số câu hỏi TN |
Câu hỏi |
||
|
TN |
TL |
TN |
TL |
|||
|
Chủ đề 6. Kim loại. Sự khác nhau cơ bản giữa phi kim và kim loại |
8 |
3 |
|
|
||
|
Bài 16. Tính chất chung của kim loại |
Nhận biết
|
- Nêu được tính chất vật lí của kim loại - Trình bày được tính chất hóa học cơ bản của kim loại - Mô tả được một số khác biệt về tính chất giữa các kim loại thông dụng (nhôm, sắt, vàng) |
4 |
|
C1, 2, 3, 4 |
|
|
Vận dụng |
|
1 |
|
C2 |
||
|
Vận dụng cao |
|
1 |
|
C3 |
||
|
Bài 17. Dãy hoạt động hóa học của kim loại. Một số phương pháp tách kim loại |
Nhận biết
|
- Nêu được dãy hoạt động hóa học (K, Na, Ca, Mg, Al, Zn, Fe, Pb, H, Cu, Ag, Au) - Trình bày được ý nghĩa của dãy hoạt động hóa học - Nêu được phương pháp tách kim loại theo mức độ hoạt động hóa học của chúng |
4 |
|
C5, 6, 7, 8 |
|
|
Thông dụng |
|
1 |
|
C1 |
||

Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
=> Giáo án hoá học 9 chân trời sáng tạo
Từ khóa: đề thi giữa kì 1 hoá học 9 chân trời sáng tạo, đề thi cuối kì 1 hoá học 9 chân trời sáng tạo, đề thi khoa học tự nhiên 9 hoá học sách chân trời, đề thi KHTN hoá học 9 sách chân trời sáng tạo mớiTài liệu giảng dạy môn Hóa học THCS
