Giáo án điện tử KHTN 8 kết nối Bài 10: Oxide
Bài giảng điện tử Khoa học tự nhiên 8 (Hoá học) kết nối tri thức. Giáo án powerpoint Bài 10: Oxide. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 8 kết nối tri thức
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét






Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 8 kết nối tri thức
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC NGÀY HÔM NAY!
KHỞI ĐỘNG
CaO
Khử chua đất
Làm vôi vữa, sản xuất xi măng
CO2
Bình cứu hỏa để dập tắt đám cháy
Đá khô để bảo quản thức ăn
Vôi sống (CaO), carbon dioxide (CO2) đều là hợp chất oxide. Vậy oxide là gì, chúng có tính chất hóa học và ứng dụng như thế nào?”
BÀI 10. OXIDE
NỘI DUNG BÀI HỌC
Khái niệm
Tính chất hóa học
I KHÁI NIỆM
THẢO LUẬN NHÓM
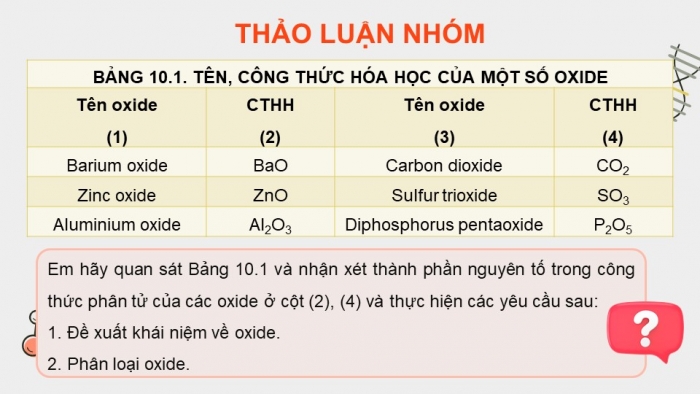
BẢNG 10.1. TÊN, CÔNG THỨC HÓA HỌC CỦA MỘT SỐ OXIDE | |||
Tên oxide (1) | CTHH (2) | Tên oxide (3) | CTHH (4) |
Barium oxide | BaO | Carbon dioxide | CO2 |
Zinc oxide | ZnO | Sulfur trioxide | SO3 |
Aluminium oxide | Al2O3 | Diphosphorus pentaoxide | P2O5 |
Em hãy quan sát Bảng 10.1 và nhận xét thành phần nguyên tố trong công thức phân tử của các oxide ở cột (2), (4) và thực hiện các yêu cầu sau:
- Đề xuất khái niệm về oxide.
- Phân loại oxide.
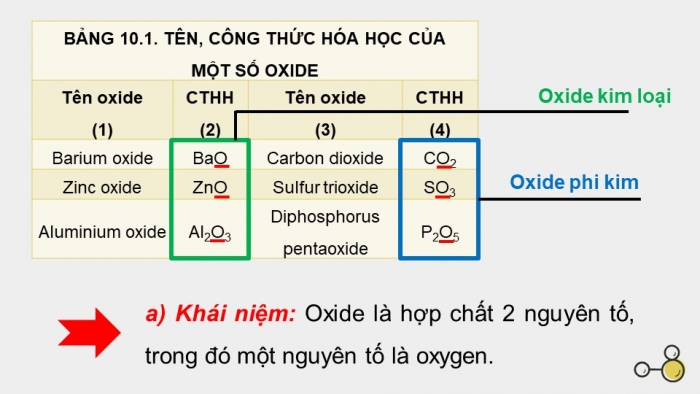
Oxide kim loại
Oxide phi kim
- a) Khái niệm: Oxide là hợp chất 2 nguyên tố, trong đó một nguyên tố là oxygen.
THẢO LUẬN NHÓM
Em hãy đọc thông tin mục I – SGK tr.44 và thực hiện nhiệm vụ:
- Phân loại oxide theo tính chất hóa học
- Cách đọc tên của oxide
- Trả lời câu hỏi – SGK tr.45.
Cho các sơ đồ phản ứng sau:
(1) …?… + O2 → Al2O3 (2) P + …?... → P2O5
(3) S + …?... → SO2 (4) Mg + O2 → …?...
Hoàn thành các phương trình hóa học và đọc tên các sản phẩm tạo thành.
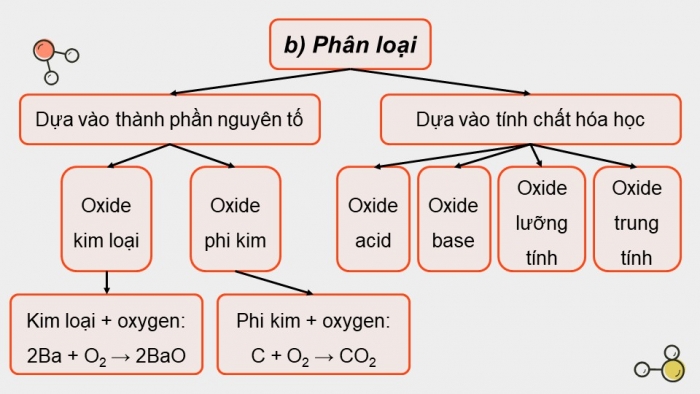
- b) Phân loại
Dựa vào thành phần nguyên tố
Oxide kim loại
Kim loại + oxygen:
2Ba + O2 → 2BaO
Oxide phi kim
Phi kim + oxygen:
C + O2 → CO2
Dựa vào tính chất hóa học
- Oxide acid
- Oxide base
- Oxide lưỡng tính
- Oxide trung tính
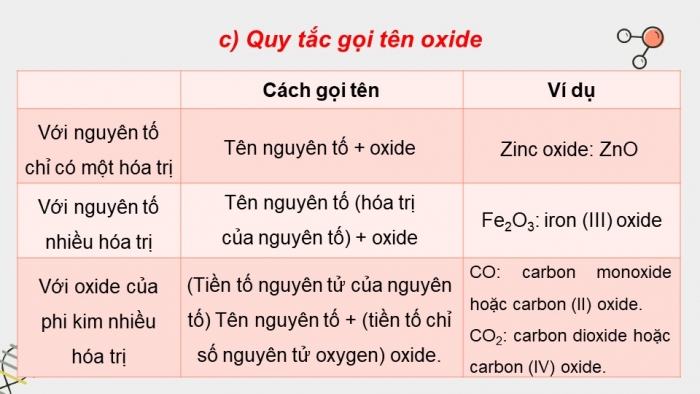
- c) Quy tắc gọi tên oxide
Cách gọi tên | Ví dụ | |
Với nguyên tố chỉ có một hóa trị | Tên nguyên tố + oxide | Zinc oxide: ZnO |
Với nguyên tố nhiều hóa trị | Tên nguyên tố (hóa trị của nguyên tố) + oxide | Fe2O3: iron (III) oxide |
Với oxide của phi kim nhiều hóa trị | (Tiền tố nguyên tử của nguyên tố) Tên nguyên tố + (tiền tố chỉ số nguyên tử oxygen) oxide. | CO: carbon monoxide hoặc carbon (II) oxide. CO2: carbon dioxide hoặc carbon (IV) oxide. |
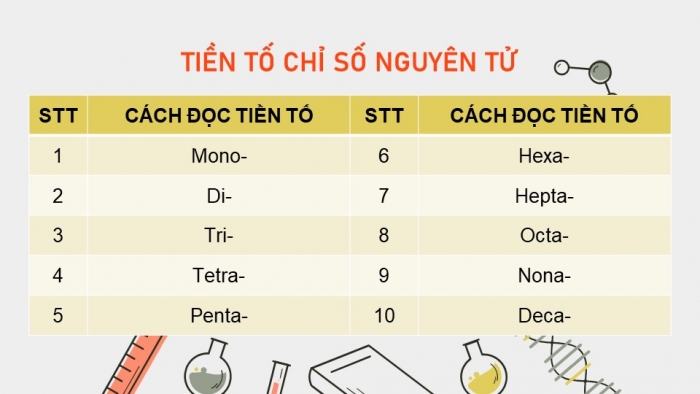
TIỀN TỐ CHỈ SỐ NGUYÊN TỬ
STT | CÁCH ĐỌC TIỀN TỐ | STT | CÁCH ĐỌC TIỀN TỐ |
1 | Mono- | 6 | Hexa- |
2 | Di- | 7 | Hepta- |
3 | Tri- | 8 | Octa- |
4 | Tetra- | 9 | Nona- |
5 | Penta- | 10 | Deca- |
Cho các sơ đồ phản ứng sau:
(1) …?… + O2 → Al2O3 (2) P + …?... → P2O5
(3) S + …?... → SO2 (4) Mg + O2 → …?...
Hoàn thành các phương trình hóa học và đọc tên các sản phẩm tạo thành.
(1) 4Al + 3O2 -> to 2Al2O3
Aluminium oxide (oxide kim loại)
(2) 4P + 5O2 -> to 2P2O5
Diphosphorus pentoxide (oxide phi kim)
(3) S + O2 -> to SO2
Sulfur dioxide (oxide phi kim)
(4) 4Mg + O2 -> to 2MgO
Magnesium oxide (oxide kim loại)
II TÍNH CHẤT HÓA HỌC
HOẠT ĐỘNG NHÓM
Nhóm chẵn: Tìm hiểu tính chất hóa học của oxide acid.
Nhóm lẻ: Tìm hiểu tính chất hóa học của oxide base.
STT | Tiến hành | Hiện tượng | PTHH | Giải thích |
1 | Dẫn khí CO2 vào cốc đựng khoảng 2 mL dung dịch Ca(OH)2. | |||
2 | Cho khoảng 3 mL dung dịch H2SO4 loãng vào ống nghiệm chưa 1 thìa bột CuO. |
Thí nghiệm 1: Tìm hiểu tính chất hóa học của oxide acid.
Chuẩn bị
- Dung dịch hydrochloric acid HCl 0,1 M.
- Thìa lấy hóa chất.
- Ống thủy tinh hình chữ L, nút cao su.
- Ống nghiệm (1) đựng khoảng 1 gam đá vôi (CaCO3) đã đập nhỏ.
- Ống nghiệm (2) đựng nước vôi trong Ca(OH)2.
Tiến hành
Cho vào ống nghiệm (1) khoảng 3 ml dung dịch hydrochloric acid 0,1 M để điều chế khí carbondioxide.
Đậy ống nghiệm bằng nút cao su có ống thủy tinh hình chữ L xuyên qua.
Dẫn khí carbon dioxide vào ống nghiệm (2). Quan sát.
Yêu cầu
- Nêu hiện tường xảy ra khi mới dẫn khí carbon dioxide vào nước vôi trong và khi dẫn khí carbon dioxide vào nước trong một khoảng thời gian.
- Nhận xét về sản phẩm khi cho oxide acid tác dụng với base.
Thí nghiệm 2: Tìm hiểu tính chất hóa học của oxide base.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 8 kết nối tri thức
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 8 KẾT NỐI TRI THỨC
Giáo án ngữ văn 8 kết nối tri thức đủ cả năm
Giáo án địa lí 8 kết nối tri thức đủ cả năm
Giáo án lịch sử 8 kết nối tri thức đủ cả năm
Giáo án khoa học tự nhiên 8 kết nối tri thức đủ cả năm
Giáo án vật lí 8 kết nối tri thức đủ cả năm
Giáo án sinh học 8 kết nối tri thức đủ cả năm
Giáo án hóa học 8 kết nối tri thức đủ cả năm
Giáo án tin học 8 kết nối tri thức đủ cả năm
Giáo án công dân 8 kết nối tri thức đủ cả năm
Giáo án công nghệ 8 kết nối tri thức đủ cả năm
Giáo án âm nhạc 8 kết nối tri thức đủ cả năm
Giáo án thể dục 8 kết nối tri thức đủ cả năm
Giáo án mĩ thuật 8 kết nối tri thức đủ cả năm
Giáo án hoạt động trải nghiệm 8 kết nối tri thức đủ cả năm
GIÁO ÁN POWERPOINT LỚP 8 KẾT NỐI TRI THỨC
GIÁO ÁN DẠY THÊM LỚP 8 KẾT NỐI TRI THỨC
Giáo án dạy thêm toán 8 kết nối tri thức đủ cả năm
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
