Giáo án điện tử hóa học 10 cánh diều bài 14: Phản ứng hoá học và enthalpy
Bài giảng điện tử hóa học 10 cánh diều. Giáo án powerpoint bài 14: Phản ứng hoá học và enthalpy. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt tạo hứng thú học tập cho học sinh. Thầy cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 10 cánh diều (bản word)
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét









Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 10 cánh diều
CHỦ ĐỂ 5: NĂNG LƯỢNG HOÁ HỌC
BÀI 14: PHẢN ỨNG HOÁ HỌC VÀ ENTHALPY
- KHỞI ĐỘNG
Em hãy quan sát các hình ảnh đây và trả lời các câu hỏi sau:
- Viết phương trình phản ứng?
- Phản ứng nào toả nhiệt, phản ứng nào thu nhiệt?
H/A LÒ NUNG VÔI
H/A ĐỐT CHÁY CỒN
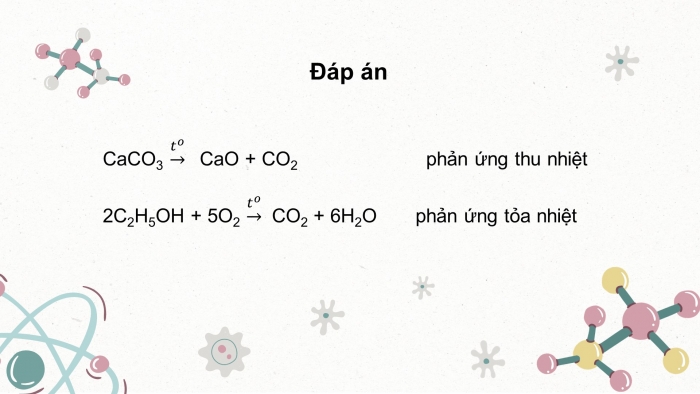
Đáp án
CaO +CO2 phản ứng thu nhiệt
phản ứng tỏa nhiệt
- NỘI DUNG BÀI HỌC
- Phản ứng toả nhiệt và phản ứng thu nhiệt
- Enthalpy tạo thành và biến thiên enthalpy của phản ứng hoá học
III. PHẦN TRIỂN KHAI KIẾN THỨC
- Phản ứng toả nhiệt và phản ứng thu nhiệt
Thảo luận nhóm: tiếnh ành lần lượt 2 thí nghiệm:
+ Thí nghiệm 1: Đặt một nhiệt kế vào trong cốc thủy tinh chứa khoảng 50 mL dung dịch hydrochloric acid (HCl) 1M (hình 14.1). Khi nhiệt độ trong cốc ổn định, ghi nhiệt độ ban đầu. Thêm vào cốc khoảng 1 gam magnesium oxide (MgO) rồi dùng đũa thủy tinh khuấy liên tục. Quan sát hiện tượng phản ứng và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
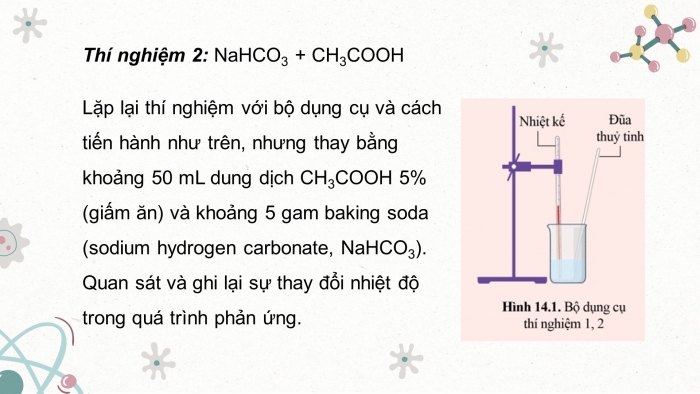
HÌNH 14.1
+ Thí nghiệm 2: Lặp lại thí nghiệm với bộ dụng cụ và cách tiến hành như trên, nhưng thay bằng khoảng 50 mL dung dịch CH3COOH 5% (giấm ăn) và khoảng 5 gam baking soda (sodium hydrogen carbonate, NaHCO3). Quan sát và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Thực hiện các yêu cầu sau:
(1) Viết phương trình hóa học xảy ra ở hai thí nghiệm trên và cho biết phản ứng nào tỏa nhiệt, phản ứng nào là thu nhiệt?
(2) Khi làm thí nghiệm, làm thế nào để biết một phản ứng là tỏa nhiệt hay thu nhiệt ?
(3) Để thuận lợi cho việc so sánh nhiệt lượng trong các phản ứng , người ta sử dụng điều kiện chuẩn, hãy cho biết điều kiện chuẩn là gì?
Đáp án:
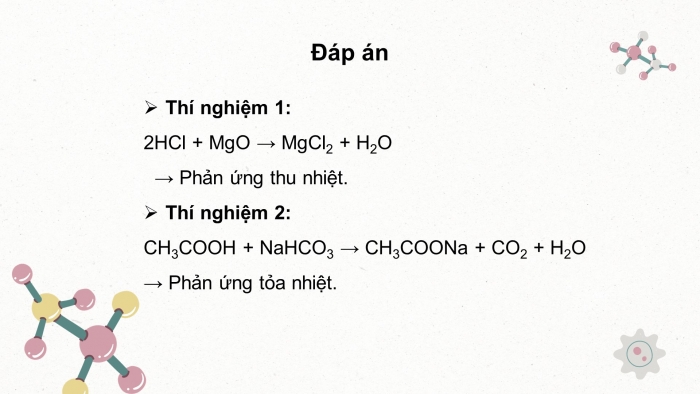
Thí nghiệm 1:
2HCl + MgO → MgCl2 + H2O
Phản ứng thu nhiệt.
Thí nghiệm 2:
CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
Phản ứng tỏa nhiệt.
Kết luận:
- Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
- Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
- Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (đối với chất khí). nồng độ 1 mol. L-1 (đối với các chất trong dung dịch) và nhiệt độ thường được chọn là 298K (25oC).
Hoạt động nhóm: Hoàn thành Phiếu bài tập số 1
PHIẾU BÀI TẬP 1 1) Lấy ví dụ về những phản ứng nào giải phóng năng lượng dưới dạng nhiệt (phản ứng tỏa nhiệt)? Những phản ứng nào hấp thu năng lượng dưới dạng nhiệt? 2) Trong những phản ứng sau phản ứng nào tỏa nhiệt? phản ứng nào thu nhiệt? a) NH4Cl(s) HCl(g) + NH3(g) b) Na2O(s) + H2O(l) → 2NaOH(aq) c) Fe2O3(s) + 2Al(s) Al2O3(s) + 2Fe d) C2H5OH(aq) + O2(g) → CO2(g) + H2O(g) e) Collagen → gelatin |
Đáp án
1)- Phản ứng tỏa nhiệt: phản ứng đốt cháy nhiên liệu, phản ứng tạo gỉ sắt, phản ứng oxi hóa glucose trong cơ thể, ...
- Phản ứng thu nhiệt: phản ứng trong lò nung vôi, nung clinker xi măng,…
2) a) NH4Cl(s) HCl(g) + NH3(g)
Phản ứng thu nhiệt.
- b) Na2O(s) + H2O(l) → 2NaOH(aq)
Phản ứng tỏa nhiệt.
- c) Fe2O3(s) + 2Al(s) Al2O3(s) + 2Fe
Phản ứng tỏa nhiệt.
- d) C2H5OH + O2→ CO2 + H2O
Phản ứng tỏa nhiệt.
- e) Collagen → gelatin
Phản ứng thu nhiệt.
- Enthalpy tạo thành và biến thiên enthalpy của phản ứng hoá học
2.1. Enthalpy tạo thành chuẩn của một chất hoá học
Thực hiện nhiệm vụ: Đọc thông tin mục II.1 SGK và trả lời câu hỏi:
+ Thế nào là enthalpy tạo thành chuẩn của một chất hoá học?
+ Kí hiệu enthalpy tạo thành chuẩn của một chất hoá học?
Đáp án
Enthalpy tạo thành chuẩn (nhiệt tạo thành chuẩn) của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn.
- Kí hiệu:
Trong đó: f viết tắt của formation (sự tạo thành)
H: enthalpy
0: số chỉ điều kiện chuẩn
298: 298K hay 250C.
Nếu > 0 : phản ứng thu nhiệt.
Nếu < 0 : phản ứng tỏa nhiệt.
Em hãy đọc VD1 và VD2
= −417,98 kJ.mol-
= - 26,48 kJ.mol-
Em hãy hoàn thành Phiếu học tập số 2:
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 10 cánh diều
GIÁO ÁN WORD LỚP 10 - SÁCH CÁNH DIỀU
Giáo án Toán 10 cánh diều đủ cả năm
Giáo án Ngữ văn 10 cánh diều đủ cả năm
Giáo án Vật lí 10 cánh diều đủ cả năm
Giáo án Sinh học 10 cánh diều đủ cả năm
Giáo án Hoá học 10 cánh diều đủ cả năm
Giáo án Âm nhạc 10 cánh diều đủ cả năm
Giáo án Bóng rổ 10 cánh diều đủ cả năm
Giáo án Bóng đá 10 cánh diều đủ cả năm
Giáo án Cầu lông 10 cánh diều đủ cả năm
Giáo án chuyên đề Công nghệ trồng trọt 10 cánh diều đủ cả năm
Giáo án chuyên đề Khoa học máy tính 10 cánh diều đủ cả năm
Giáo án chuyên đề Kinh tế pháp luật 10 cánh diều đủ cả năm
Giáo án chuyên đề Lịch sử 10 cánh diều đủ cả năm
Giáo án chuyên đề Sinh học 10 cánh diều đủ cả năm
Giáo án chuyên đề Thiết kế công nghệ 10 cánh diều đủ cả năm
Giáo án chuyên đề Tin học ứng dụng 10 cánh diều đủ cả năm
Giáo án chuyên đề Vật lí 10 cánh diều đủ cả năm
Giáo án Tin học 10 cánh diều đủ cả năm
Giáo án Công nghệ 10 thiết kế công nghệ cánh diều đủ cả năm
Giáo án Công nghệ 10 trồng trọt cánh diều đủ cả năm
Giáo án Hoạt động trải nghiệm, hướng nghiệp 10 cánh diều đủ cả năm
Giáo án Kinh tế pháp luật 10 cánh diều đủ cả năm
Giáo án lịch sử 10 cánh diều đủ cả năm
Giáo án chuyên đề Địa lí 10 cánh diều đủ cả năm
Giáo án Quốc phòng an ninh 10 cánh diều đủ cả năm
GIÁO ÁN POWERPOINT LỚP 10 - SÁCH CÁNH DIỀU
GIÁO ÁN CHUYÊN ĐỀ LỚP 10 - SÁCH CÁNH DIỀU
GIÁO ÁN LỚP 10 CÁC BỘ SÁCH KHÁC
Giáo án lớp 10 sách chân trời sáng tạo (bản word)
Giáo án lớp 10 sách chân trời sáng tạo (bản powrerpoint)
Giáo án lớp 10 sách kết nối tri thức (bản word)
Giáo án lớp 10 sách kết nối tri thức (bản powrerpoint)
Cách đặt mua:
Liên hệ Zalo: Fidutech - Nhấn vào đây
