Giáo án điện tử hóa học 10 chân trời bài 17: Tính chất vật lí và hóa học các đơn chất nhóm viia
Bài giảng điện tử hóa học 10 chân trời. Giáo án powerpoint bài 17: Tính chất vật lí và hóa học các đơn chất nhóm viia. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt tạo hứng thú học tập cho học sinh. Thầy cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 10 chân trời sáng tạo (bản word)
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét










Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 10 chân trời sáng tạo
BÀI 17. TÍNH CHẤT VẬT LÍ VÀ HÓA HỌC CÁC ĐƠN CHẤT NHÓM VIIA
- KHỞI ĐỘNG
Đèn halogen được sử dụng trong các máy sưởi, lò nướng, bếp halogen hồng ngoại,… do đặc điểm tỏa nhiều nhiệt.
HÌNH ẢNH ĐÈN HALOGEN
Cách xử lí nước phổ biến hiện nay là sử dụng nước chlorine hoặc các chất có chứa chlorine để khử trùng nước
HÌNH ẢNH SỬ DỤNG CHLORINE ĐỂ KHỬ TRÙNG NƯỚC
Nhóm halogen gồm những nguyên tố nào? Halogen có những tính chất và ứng dụng trong lĩnh vực nào?
- NỘI DUNG BÀI HỌC
- Vị trí của nhóm halogen trong bảng tuần hoàn
- Trạng thái tự nhiên của các halogen
- Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen. Đặc điểm cấu tạo phân tử halogen
- Tính chất vật lí của các halogen
- Tính chất hóa học của các halogen
- Ứng dụng của các halogen
III. PHẦN TRIỂN KHAI KIẾN THỨC
- Vị trí của nhóm halogen trong bảng tuần hoàn
Em hãy trả lời Câu hỏi 1 SGK trang 106
- Quan sát hình 17.1, cho biết vị trí của nhóm halogen trong bảng tuần hoàn
HÌNH 17.1
Đáp án
Nhóm halogen là nhóm VIIA trong bảng tuần hoàn các nguyên tố hóa học
- Trạng thái tự nhiên của các halogen
Thảo luận nhóm: Đọc thông tin SGK, trả lời Câu hỏi 2, 3, Luyện tập trang 106, 107
- Hãy kể tên một số chất chứa nguyên tố halogen.
- Từ các thông tin và quan sát Hình 17.2, nhận xét dạng tồn tại của các nguyên tố halogen trong tự nhiên.
HÌNH 17.2
Luyện tập. Khoảng 71% bề mặt Trái Đất được bao phủ bởi biển và đại dương, phần còn lại là các lục địa và đảo. Theo em, hàm lượng nguyên tố halogen nào nhiều nhất trong tự nhiên?
Đáp án
Trong thực tiễn, các nguyên tố halogen có mặt trong muối ăn, kem đánh răng, nước tẩy rửa, nước sát trùng, đèn halogen ( bóng đèn, đèn ô tô, xe máy), bếp halogen hồng ngoại,…
3.
Trong tự nhiên, halogen chỉ tồn tại ở trạng thái hợp chất, chủ yếu ở dạng muối ion halide. Phần lớn ion halide có trong nước biển, một số tồn tại trong các loại quặng, ở thể rắn.
Luyện tập
Các ion halide được tìm thấy trong nước biển và đại dương có hàm lượng giảm dần: Cl-, Br-, I- và F-. Trong đó Cl- có hàm lượng 55,04%.
Kết luận: Trong tự nhiên, halogen chỉ tồn tại ở trạng thái hợp chất. Hợp chất chủ yếu của halogen là muối halide.
- Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen. Đặc điểm cấu tạo phân tử halogen
Hoạt động nhóm: Đọc thông tin SGK, trả lời Câu hỏi 4, 5 SGK trang 107
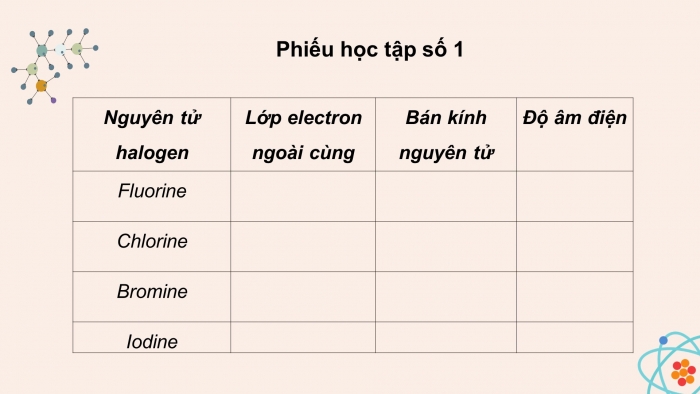
- Viết cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen
5. Từ đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, nhận xét xu hướng hình thành liên kết trong phân tử halogen
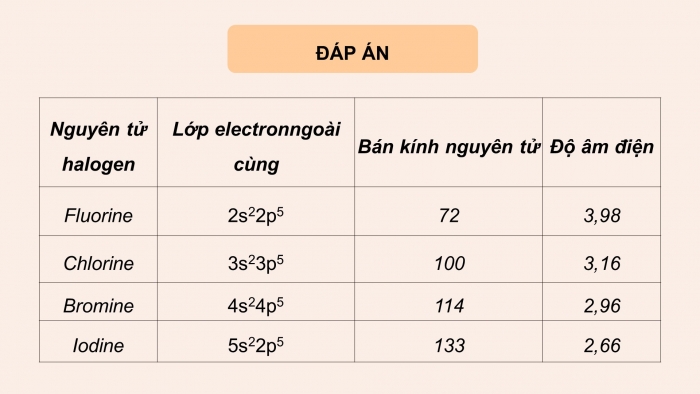
Đáp án
F: (He)2s22p5
Cl: (Ne)3s23p5
Br: (Ar)4s24p5
I: (Kr)5s25p5
Nguyên tử halogen có 7 electron lớp ngoài cùng, chưa đạt cấu hình bền vững (theo quy tắc octet) nên mỗi nguyên tử halogen có xu hướng góp chung 1 electron để hình thành liên kết cộng hóa trị không phân cực trong phân tử X2. Công thức cấu tạo các halogen: F – F, Cl – Cl, Br – Br, I – I. Tổng quát: X – X
=> Kết luận: Đơn chất halogen tồn tại ở dạng phân tử X2, liên kết trong phân tử là liên kết cộng hóa trị không phân cực.
- Tính chất vật lí của các halogen
Hoạt động nhóm: Trả lời Câu hỏi 6, 7, Luyện tập SGK trang 108
- Dựa vào Bảng 17.1, nhận xét sự biến đổi về màu sắc, thể các chất ở điều kiện thường, nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen
BẢNG 17.1
- Giải thích sự biến đổi nhiệt độ nóng chảy, nhiệt độ sôi từ fluorine đến iodine
Luyện tập. Ở điều kiện thường, hãy dự đoán astatine tồn tại ở thể khí, thể lỏng hay thể rắn. Giải thích
Đáp án
6.
- Thể tập hợp tạp 20 độ C của F và Cl là thể khí, Br là thể lỏng, I là thể khí.
- Nhiệt độ nóng chảy, nhiệt độ sôi tăng dần từ F đến I.
7.
Giữa các phân tử halogen hình thành tương tác van der Waals, ảnh hưởng đến sự biến đổi nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen, từ F đến I, bán kính nguyên tử và khối lượng phân tử tăng dần làm tăng tương tác giữa các phân tử, nên nhiệt độ nóng chảy, nhiệt độ sôi tăng.
Luyện tập.
- Theo chiều tăng dần của bán kính nguyên tử và khối lượng phân tử à tương tác van der Waals tăng à các nguyên tố halogen từ thể khí (F2, Cl2) sang lỏng (Br2) và rắn (I2) àDự đoán astatine tồn tại ở thể rắn.
Kết luận:
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 10 chân trời sáng tạo
