Giáo án và PPT Hoá học 10 cánh diều Bài 3: Nguyên tố hoá học
Đồng bộ giáo án word và powerpoint (ppt) Bài 3: Nguyên tố hoá học. Thuộc chương trình Hoá học 10 cánh diều. Giáo án được biên soạn chỉnh chu, hấp dẫn. Nhằm tạo sự lôi cuốn và hứng thú học tập cho học sinh.
Click vào ảnh dưới đây để xem giáo án WORD rõ nét








Giáo án ppt đồng bộ với word









Còn nữa....
Các tài liệu bổ trợ khác
Xem toàn bộ: Trọn bộ giáo án và PPT Hoá học 10 cánh diều
BÀI 3. NGUYÊN TỐ HÓA HỌC
HOẠT ĐỘNG KHỞI ĐỘNG
GV chi HS làm việc cá nhân, điền các thông tin vào phiếu KWL. GV có thể giao nhiệm vụ này cho HS làm trước ở nhà, điền phiếu KWL theo nội dung: Hãy nêu những điều em đã biết về nguyên tố hóa học (Nguyên tố hóa học là gì? Nhìn vào một ô nguyên tố trong bảng tuần hoàn, ta biết những điều gì?...)
Bảng KWL:
K Những điều em đã biết (Know) | W Những điều em muốn biết (Want) | L Những điều em đã học được ( Learned) |
|
|
|
HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
I. NGUYÊN TỐ HÓA HỌC.
Hoạt động 1. Khái niệm nguyên tố hóa học
GV yêu cầu HS hoạt động nhóm 2 trả lời câu hỏi:
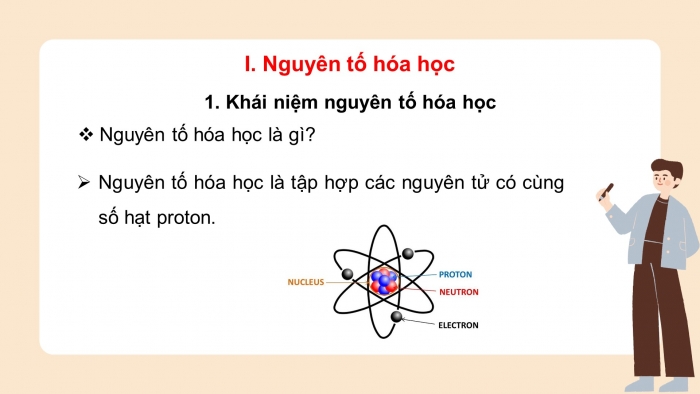
Nguyên tố hóa học là gì?
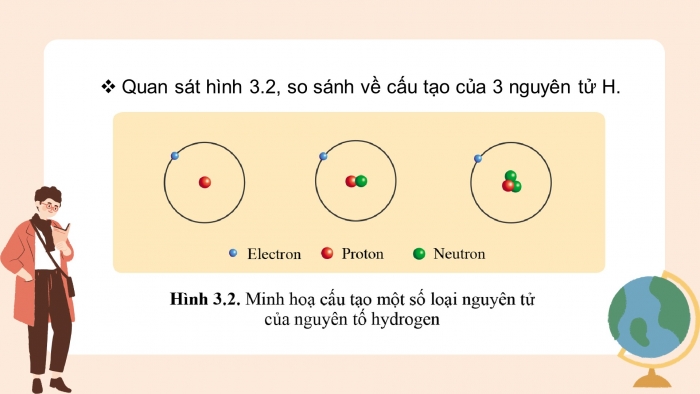
Quan sát hình 3.2, so sánh về cấu tạo của 3 nguyên tử H.
Sản phẩm dự kiến:
- Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton.
- So sánh:
Giống: đều có 1 proton và 1 electron trong nguyên tử
Khác:
Nguyên tử H thứ nhất không có neutron
Nguyên tử H thứ hai chứa 1 neutron
Nguyên tử H thứ ba chứa 2 neutron
- Trả lời câu hỏi 1 sgk trang 16:
Ion Li+ có 3 proton trong hạt nhân.
Hoạt động 2. Số hiệu nguyên tử, số khối, kí hiệu nguyên tử
GV đưa ra câu hỏi:
Số hiệu nguyên tử là gì? Kí hiệu là gì?
Số khối là gì? Nêu công thức tính số khối.
Kí hiệu nguyên tử được viết như thế nào? Kí hiệu nguyên tử có ý nghĩa gì? Cho ví dụ.
Sản phẩm dự kiến:
- Số proton trong mỗi hạt nhân nguyên tử được gọi là số hiệu nguyên tử, kí hiệu là Z.
- Số khối là tổng số proton (Z) và neutron (N) trong một hạt nhân nguyên tử , kí hiệu là A
Công thức: A= Z+N
- Kí hiệu nguyên tử: ![]()
Ý nghĩa: cho biết kí hiệu hóa học của nguyên tố (X), số hiệu nguyên tử Z và số khối A
Ví dụ hình 3.4

- Trả lời luyện tập 1 sgk trang 17:
Phân tử S8 có 128 electron
=> S có 128:8 = 16 (electron)
=> p =e = 16
Vậy số hiệu nguyên tử của lưu huỳnh là 16.
- Trả lời luyện tập 2 sgk trang 17:
Khối lượng gần đúng của nguyên tử này:
Z.1 + Z.0,00055 + N.1 = Z + N (amu)
Số khối của nguyên tử này: Z + N
Khối lượng gần đúng theo amu xấp xỉ bằng số khối của nguyên tử.
- Trả lời câu luyện tập 3 sgk trang 17:
Nguyên tử | Số p | Số n | Kí hiệu nguyên tử |
C | 6 | 6 |
|
X | 11 | 12 |
|
- Trả lời câu hỏi 2 sgk trang 17:
Kí hiệu là: ![]()
II. ĐỒNG VỊ, NGUYÊN TỬ KHỐI TRUNG BÌNH
Hoạt động 1. Đồng vị
GV yêu cầu học sinh hoạt động theo nhóm:
Điền đáp án phiếu học tập.
Nêu khái niệm đồng vị. Lấy ví dụ.
Sản phẩm dự kiến:
Đáp án phiếu học tập:
 : Nguyên tử H có điện tích hạt nhân là 1 và số khối là 1
: Nguyên tử H có điện tích hạt nhân là 1 và số khối là 1
=> số neutron = 0
![]() : Nguyên tử H có điện tích hạt nhân là 1 và số khối là 2
: Nguyên tử H có điện tích hạt nhân là 1 và số khối là 2
=> số neutron =1
![]() : Nguyên tử H có điện tích hạt nhân là 1 và số khối là 3
: Nguyên tử H có điện tích hạt nhân là 1 và số khối là 3
=> số neutron = 2
Khái niệm đồng vị: Các nguyên tử của cùng một nguyên tố hóa học có cùng số neutron khác nhau là đồng vị của nhau.
Nguyên tử M và T là đồng vị của nhau.
Hoạt động 2. Nguyên tử khối trung bình
GV đưa ra câu hỏi:
Nguyên tử khối trung bình là gì? Nêu kí hiệu của nguyên tử khối trung bình.
Viết công thức tính nguyên tử khối trung bình.
Sản phẩm dự kiến:
Nguyên tử khối là khối lượng tương đối của của một nguyên tử, cho biết khối lượng của một nguyên tử nặng gấp bao nhiêu lần 1 amu.
Nguyên tử khối của nguyên tố hóa học có nhiều đồng vị là nguyên tử khối trung bình của đồng vị kí hiệu là

Công thức tính nguyên tử khối trung bình:

Trong đó:
X, Y, Z… lần lượt là số khối của các đồng vị
x, y, z … là phần trăm số nguyên tử các đồng vị tương ứng.
Trả lời câu luyện tập 4 sgk trang 18:
Áp dụng công thức tính nguyên tử khối trung bình ta có:
![]()
HOẠT ĐỘNG LUYỆN TẬP
Câu 1: Nguyên tử X có tổng số hạt proton, neutron, electron là 34. Biết số neutron nhiều hơn số proton là 1. Số khối của nguyên tử X là
A. 35.
B. 23.
C. 11.
D. 46.
Câu 2: Theo Viện Thiên văn học 20Ne và 22Ne là một trong những chất khí tạo nên mặt trời. Phát biểu nào sau đây là đúng ?
A. 20 Ne và 22 Ne là đồng vị của nhau.
B. 20 Ne và 22 Ne có cùng tổng số hạt trong hạt nhân.
C. 20 Ne và 22 Ne có cùng khối lượng.
D. 20 Ne và 22 Ne có cùng số neutron.
Câu 3: Trong tự nhiên Chlorine có hai đồng vị bền: 37Clchiếm 24,23% tổng số nguyên tử, còn lại là 35Cl. Thành phần % theo khối lượng của 37Cl trong HClO4 là
A. 8,92%.
B. 8,79%.
C. 8,43%.
D. 8,56%.
Câu 4: Một nguyên tử có 29 proton, 36 neutron và 29 electron. Số hiệu nguyên tử và số khối của nguyên tử có giá trị:
A. Số hiệu nguyên tử = 36, số khối = 65.
B. Số hiệu nguyên tử = 16, số khối = 36.
C. Số hiệu nguyên tử = 29, số khối = 65.
D. Số hiệu nguyên tử = 29, số khối = 36.
Sản phẩm dự kiến:
Câu 1: B
Câu 2: A
Câu 3: A
Câu 4: C
HOẠT ĐỘNG VẬN DỤNG
Vận dụng kiến thức, GV yêu cầu HS trả lời câu hỏi:
Câu 1: Nguyên tử X có 12 electron, 12 neutron, viết kí hiệu nguyên tử của X.
Câu 2: Trong tự nhiên, nguyên tử Chlorine có hai đồng vị bền là 35Cl và 37Cl. Tại sao nguyên tử khối tương đối của Chlorine thường được sử dụng là 35,5?
Câu 3: Trong tự nhiên, Iridium có hai đồng vị bền có số khối lần lượt là 191 và 193. Nguyên tử khối trung bình của Iridium là 192,22. Tỉ lệ số nguyên tử của hai đồng vị là bao nhiêu?
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Trọn bộ giáo án và PPT Hoá học 10 cánh diều
TÀI LIỆU GIẢNG DẠY HOÁ HỌC 10 KẾT NỐI TRI THỨC
Giáo án Hoá học 10 kết nối tri thức đủ cả năm
Giáo án điện tử hoá học 10 kết nối tri thức
Giáo án chuyên đề Hóa học 10 kết nối tri thức đủ cả năm
Giáo án điện tử chuyên đề Hoá học 10 kết nối tri thức
Trò chơi khởi động Hoá học 10 kết nối tri thức
Video AI khởi động Hoá học 10 kết nối tri thức hấp dẫn
Giáo án tích hợp NLS Hoá học 10 kết nối tri thức
Trắc nghiệm Hóa học 10 kết nối tri thức
Đề thi hóa học 10 kết nối tri thức
File word đáp án hóa học 10 kết nối tri thức
Bài tập file word Hóa học 10 kết nối tri thức
Kiến thức trọng tâm hóa học 10 kết nối tri thức
Câu hỏi tự luận Hóa học 10 kết nối tri thức
Đề kiểm tra 15 phút Hoá học 10 kết nối tri thức
Phiếu học tập theo bài Hoá học 10 kết nối tri thức cả năm
Trắc nghiệm đúng sai Hoá học 10 kết nối tri thức cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 10 kết nối tri thức cả năm
TÀI LIỆU GIẢNG DẠY HOÁ HỌC 10 CHÂN TRỜI SÁNG TẠO
Giáo án Hoá học 10 chân trời sáng tạo đủ cả năm
Giáo án điện tử hoá học 10 chân trời sáng tạo
Giáo án chuyên đề Hóa học 10 chân trời sáng tạo đủ cả năm
Giáo án điện tử chuyên đề Hoá học 10 chân trời sáng tạo
Trò chơi khởi động Hoá học 10 chân trời sáng tạo
Video AI khởi động Hoá học 10 chân trời sáng tạo hấp dẫn
Trắc nghiệm hoá học 10 chân trời sáng tạo
Đề thi hóa học 10 chân trời sáng tạo
File word đáp án hóa học 10 chân trời sáng tạo
Bài tập file word Hóa học 10 chân trời sáng tạo
Kiến thức trọng tâm hóa học 10 chân trời sáng tạo
Đề kiểm tra 15 phút Hoá học 10 chân trời sáng tạo
Phiếu học tập theo bài Hoá học 10 chân trời sáng tạo cả năm
Trắc nghiệm đúng sai Hoá học 10 chân trời sáng tạo cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 10 chân trời sáng tạo cả năm
TÀI LIỆU GIẢNG DẠY HOÁ HỌC 10 CÁNH DIỀU
Giáo án Hoá học 10 cánh diều đủ cả năm
Giáo án điện tử hoá học 10 cánh diều
Giáo án chuyên đề Hóa học 10 cánh diều đủ cả năm
Giáo án điện tử chuyên đề Hoá học 10 cánh diều
Trò chơi khởi động Hoá học 10 cánh diều
Video AI khởi động Hoá học 10 cánh diều hấp dẫn
Trắc nghiệm hoá học 10 cánh diều
Đề thi hóa học 10 cánh diều
File word đáp án hóa học 10 cánh diều
Bài tập file word Hóa học 10 cánh diều
Kiến thức trọng tâm hóa học 10 cánh diều
Đề kiểm tra 15 phút Hoá học 10 cánh diều
Phiếu học tập theo bài Hoá học 10 cánh diều cả năm
Trắc nghiệm đúng sai Hoá học 10 cánh diều cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 10 cánh diều cả năm
