Trắc nghiệm câu trả lời ngắn Hoá học 10 kết nối Bài 17: Biến thiên enthalpy trong các phản ứng hoá học
Tài liệu trắc nghiệm dạng câu trả lời ngắn Hoá học 10 kết nối tri thức Bài 17: Biến thiên enthalpy trong các phản ứng hoá học. Dựa trên kiến thức của bài học, bộ tài liệu được biên soạn chi tiết, đúng trọng tâm và rõ ràng. Câu hỏi đa dạng với các mức độ khó dễ khác nhau. Tài liệu có file Word tải về. Thời gian tới, nội dung này sẽ tiếp tục được bổ sung.
Xem: => Giáo án hóa học 10 kết nối tri thức (bản word)
Các tài liệu bổ trợ
BÀI 17. BIẾN THIÊN ENTHALPY TRONG CÁC PHẢN ỨNG HOÁ HỌC
Câu 1: Nhiệt tạo thành chuẩn của một chất là nhiệt lượng tạo thành x mol chất đó từ các đơn chất bền vững nhất ở điều kiện chuẩn. Giá trị của x là
1
Câu 2: Dựa vào phương trình nhiệt hóa học của các phản ứng sau:
ZnSO4(s) → ZnO(s) + SO3(g) ∆rHo298 = +235,21 kJ (1)
3H2(g) + N2(g) → 2NH3(g) ∆rHo298 = -91,8 kJ (2)
2H2S(g) + SO2(g)→ 2H2O(g) + 3S(s) ∆rHo298 = -237 kJ (3)
H2O(g) →H2 + ½ O2(g) ∆rHo298 = +241,8 kJ (4)
Các phản ứng thu nhiệt là
14
Câu 3: Khi tạo ra 1 mol HCl từ các đơn chất bền có giải phóng ra một lượng nhiệt là 91,98 kJ/mol. Nếu phân huỷ 365 gam khí HCl thành các đơn chất thì lượng nhiệt kèm theo quá trình đó là bao nhiêu
919,8
Câu 4: Biến thiên enthalpy chuẩn của quá trình hóa hơi của hơi nước H2O(l) → H2O(g) có giá trị ∆rHo298 = +44 kJ/mol.
132
Câu 5: Chlorine phản ứng với ethane để tạo ra chloroethane và hydrogen chloride theo phương trình:
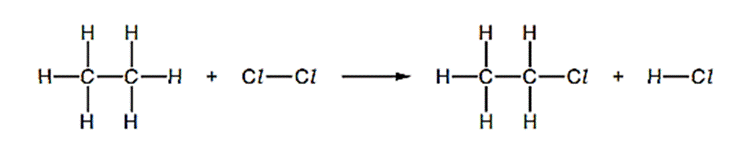
Biến thiên enthalpy chuẩn của phản ứng tính theo năng lượng liên kết nhận giá trị nào dưới đây? Biết năng lượng liên kết của một số loại liên kết được cho trong bảng sau.
| Liên kết | Năng lượng liên kết (kJ/mol) |
| C-Cl | +340 |
| C-C | +350 |
| C-H | +410 |
| Cl-Cl | +240 |
| H-Cl | +430 |
230
Câu 6: Dung dịch glucose (C6H12O6) 5%, có khối lượng riêng là 1,02 g/mL, phản ứng oxi hóa 1 mol glucose tạo thành CO2 (g) và H2O (l) tỏa ra nhiệt lượng là 2803,0 kJ.
Một người bệnh được truyền một chai nước chứa 500 mL dung dịch glucose 5%. Năng lượng tối đa từ phản ứng oxi hóa hoàn toàn glucose mà bệnh nhân đó có thể nhận được là
397,09
BÀI TẬP THAM KHẢO THÊM
Câu 1: Phản ứng tỏa nhiệt là gì?
Trả lời: Là phản ứng phóng năng lượng dạng nhiệt
Câu 2: Thế nào là phản ứng thu nhiệt?
Trả lời: Là phản ứng hấp thụ năng lượng dạng nhiệt.
Câu 3: Điều kiện để xảy ra phản ứng tỏa nhiệt (t= 25oC)?
Trả lời: ![]()
![]() 0
0
Câu 4: Nhiệt kèm theo phản ứng trong điều kiện chuẩn là gì?
Trả lời: Biến thiên enthalpy chuẩn (hay nhiệt phản ứng chuẩn) của phản ứng đó, kí hiệu là ![]() tHo298K
tHo298K
Câu 5: Cho 2 phương trình nhiệt hóa học sau:
C (s) + H2O (g) ![]() CO (g) + H2 (g)
CO (g) + H2 (g) ![]() tHo298K = +121,25 kJ (1)
tHo298K = +121,25 kJ (1)
CuSO4 (aq) + Zn (s) ![]() ZnSO4 (aq) + Cu (s)
ZnSO4 (aq) + Cu (s) ![]() tHo298K = -230,04 kJ (2)
tHo298K = -230,04 kJ (2)
Nêu loại phản ứng của phản ứng trên.
Trả lời: Phản ứng (1) là phản ứng thu nhiệt, phản ứng 2 là phản ứng tỏa nhiệt
Câu 6: Kí hiệu của nhiệt tạo thành chuẩn là?
Trả lời: ………………………………………
Câu 7: Đơn vị của nhiệt tạo thành chuẩn là?
Trả lời: ………………………………………
Câu 8: Cho phản ứng: N2 (g) + 3H2 (g) ![]() 2NH3 (g)
2NH3 (g)
Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ tỏa ra 91,8kJ. Enthalpy tạo thành chuẩn của NH3 là:
Trả lời: ………………………………………
Câu 9: Sắp xếp các ý sau vào loại phản ứng phù hợp (thu nhiệt, tỏa nhiệt):
a. tăng enthalpy. d. nhiệt bị hấp thụ.
b. có thể xảy ra một cách tự phát. e. nhiệt được giải phóng.
c. giảm enthalpy. f. để xảy ra cần cung cấp năng lượng.
Trả lời: ………………………………………
Câu 10: Giá trị nhiệt độ và áp suất được chọn ở điều kiện chuẩn là:
Trả lời: ………………………………………
Câu 11: Cho các quá trình sau:
(1) Quá trình hô hấp của thực vật. (2) Cồn cháy trong không khí.
(3) Quá trình quang hợp của thực vật. (4) Hấp chín bánh bao.
Quá trình nào là quá trình tỏa nhiệt?
Trả lời: ………………………………………
Câu 12: Tính chất của enthapy là
Trả lời: ………………………………………
Câu 13: Ý nghĩa của enthapy là
Trả lời: ………………………………………
Câu 14: Biến thiên enthalpy của phản ứng nào có giá trị âm?
Trả lời: ………………………………………
Câu 15: Cho các phản ứng sau:
(1) C(s) + O2(g) →CO2(g) ![]() = -393,5 kJ
= -393,5 kJ
(2) 2Al(s) + 3/2O2(g) →Al2O3(s) ![]() = -1675,7 kJ
= -1675,7 kJ
(3) CH4(g) + 2O2(g) →CO2(g) + 2H2O(l) ![]() = -890,36 kJ
= -890,36 kJ
(4) C2H2(g) + 5/2O2(g) →2CO2(g) + H2O (l) ![]() = -1299,58 kJ
= -1299,58 kJ
Trong các phản ứng trên, phản ứng nào tỏa nhiều nhiệt nhất?
Trả lời: ………………………………………
Câu 16: Vì sao khi nung vôi, người ta phải xếp đá vôi lẫn với than trong lò?
Trả lời: ………………………………………
Câu 17: Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất, kí hiệu là ![]() , là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn. Khi phản ứng tỏa nhiệt thì
, là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn. Khi phản ứng tỏa nhiệt thì
Trả lời: ………………………………………
Câu 18: Ở điều kiện chuẩn, cần phải cung cấp 26,48 kJ nhiệt lượng cho quá trình 0,5 mol H2(g) phản ứng với 0,5 mol I2(s) để thu được 1 mol HI(g). Như vậy, enthalpy tạo thành của hydrogen iodide (HI) là
Trả lời: ………………………………………
Câu 19: Cho phản ứng: 1/2N2(g) + 3/2H2(g) →NH3(g). Biết enthalpy tạo thành chuẩn của NH3 là –45,9 kJ mol-1. Để thu được 2 mol NH3 ở cùng điều kiện phản ứng thì
Trả lời: ………………………………………
Câu 20: Cho phản ứng: H2(g) + Cl2(g) →→2HCl(g). Ở điều kiện chuẩn, cứ 1 mol H2 phản ứng hết sẽ tỏa ra -184,6 kJ. Tính enthalpy tạo thành chuẩn của HCl(g).
Trả lời: ………………………………………
Câu 21: Cho ![]() = (Fe2O3, s) = − 825,5 kJ/mol. Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị (kcal) của Fe2O3 (s) là
= (Fe2O3, s) = − 825,5 kJ/mol. Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị (kcal) của Fe2O3 (s) là
Trả lời: ………………………………………
Câu 22: Cho phản ứng: Na (s) + 1/2Cl2 (g) ⟶NaCl (s) có ![]() (NaCl, s) = − 411,1 kJ/mol. Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
(NaCl, s) = − 411,1 kJ/mol. Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
Trả lời: ………………………………………
Câu 23: Một hộ gia đình mua than đá làm nhiên liệu đun nấu và trung bình mỗi ngày dùng hết 1,60 kg
than. Giả thiết loại than đá trên chứa 90% carbon về khối lượng, còn lại là các tạp chất trơ.
Cho phản ứng: C(s) + O2(g) → CO2(g) ![]()
Nhiệt lượng cung cấp cho hộ gia đình từ quá trình đốt than trong một ngày tương đương bao nhiêu số điện?
Biết rằng 1 số điện = 1 kWh = 3600 kJ. Nguyên tử khối của carbon là 12. (kết quả làm tròn đến hàng đơn vị)
Trả lời: ………………………………………
Câu 24: Bình “ga” sử dụng trong một hộ gia đình có chứa 12 kg khí hóa lỏng (LPG) gồm propan (C3H8) và butan (C4H10) với tỉ lệ mol tương ứng là 2 : 3. Khi được đốt cháy hoàn toàn, 1 mol propan tỏa ra lượng nhiệt là 2220 kJ và 1 mol butan tỏa ra lượng nhiệt là 2850 kJ (sản phẩm gồm H2O ở trạng thái lỏng và khí CO2). Trung bình, lượng nhiệt tiêu thụ từ' đốt khí “ga” của hộ gia đình Y là 10.000 kJ/ngày và hiệu suất sử dụng nhiệt là 67,3%.
Sau bao nhiêu ngày hộ gia đình sẽ sử dụng hết bình ga trên? (kết quả làm tròn đến hàng đơn vị)
Trả lời: ………………………………………
Câu 25: Cho các phản ứng sau xảy ra ở điều kiện chuẩn:
CH4(g) + 2O2(g) →CO2(g) + 2H2O(l)![]() = -890,36 kJ
= -890,36 kJ
CaCO3(s) →CaO(s) + CO2(s) ![]() )= 178,29 kJ
)= 178,29 kJ
Ở điều kiện tiêu chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam CH4(g) để cung cấp nhiệt cho phản ứng tạo 2 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%.
Trả lời: ………………………………………
----------------------------------
----------------------- Còn tiếp -------------------------
