Giáo án điện tử hóa học 10 kết nối bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học.
Bài giảng điện tử hóa học 10 kết nối tri thức. Giáo án powerpoint bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học.. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt tạo hứng thú học tập cho học sinh. Thầy cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 10 kết nối tri thức (bản word)
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét








Xem video về mẫu Giáo án điện tử hóa học 10 kết nối bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học.
Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 10 kết nối tri thức
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC NGÀY HÔM NAY!
CHƯƠNG 2:
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC VÀ ĐỊNH LUẬT TUẦN HOÀN
KHỞI ĐỘNG
Hãy ghi những điều các em đã biết về bảng tuần hoàn vào cột K, những điều các em chưa biết và muốn biết vào cột W; những điều các em học được sẽ ghi vào cột L sau khi kết thúc bài học này.
BÀI 5:
CẤU TẠO CỦA BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC.
- Lịch sử phát minh bảng tuần hoàn các nguyên tố hóa học
Năm 1829, A. Lavoisier là người đầu tiên phân loại các nguyên tố hóa học thành các nhóm:
- Chất khí
- Kim loại
- Phi kim
- Đất
- Năm 1929, J.W. Döbereiner phân loại các nhóm có tính chất hóa học giống nhau.
- Năm 1866, J. Newlands xếp lại các nguyên tố theo chiều tăng khối lượng nguyên tử thành các octave.
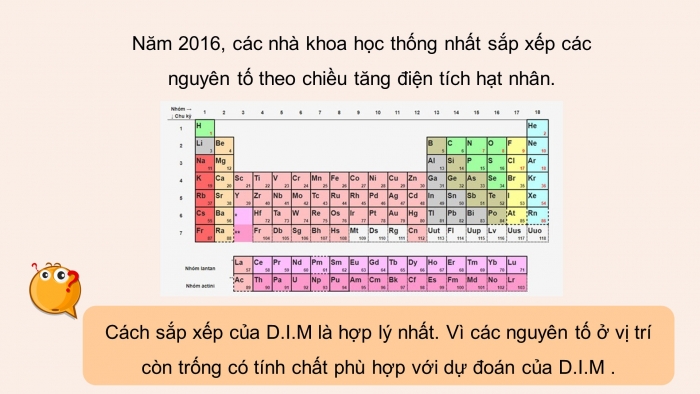
Năm 1969, D. I. Mendeleev và J. L. Meyer, sắp xếp các nguyên tố theo chiều tăng khối lượng vào từng hàng từng cột và nhận thấy tính chất hóa học của các nguyên bắt đầu tố lặp lại, ngoài ra D.I.M thay đổi một số vị trí cho phù hợp.
Cách sắp xếp của D.I.M là hợp lý nhất. Vì các nguyên tố ở vị trí còn trống có tính chất phù hợp với dự đoán của D.I.M .
Theo tiến trình lịch sử, các nhà khoa học đã phân loại các nguyên tố hóa học trên các cơ ở nào ?
Theo tiến trình lịch sử, các nhà khoa học đã phân loại các nguyên tố hóa học dựa trên các sơ sở:
- Tính chất hóa học
- Hóa trị
- Khối lượng nguyên tử
- Điện tích hạt nhân nguyên tử
- Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn
Electron hóa trị là gì ?
Electron hóa trị là các electron có khả năng tham tạo thành liên kết hóa học, chúng thường nằm ở lớp electron ngoài cùng và phân lớp sát lớp ngoài cùng.
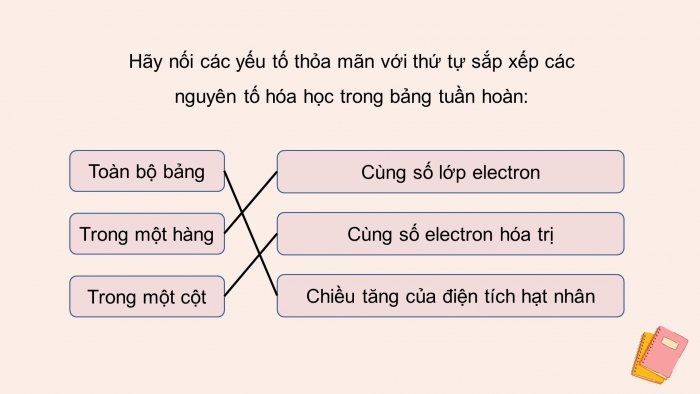
Hãy nối các yếu tố thỏa mãn với thứ tự sắp xếp các nguyên tố hóa học trong bảng tuần hoàn:
Kết luận
Những nguyên tắc sắp xếp các nguyên tố
trong bảng tuần hoàn.
- Các nguyên tố được sắp xếp theo chiều tăng dần điện tích hạt nhân.
- Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng.
- Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp thành một cột.
Câu 2 (sgk): Trong bảng tuần hoàn, các nguyên tố hóa học được sắp xếp theo 3 nguyên tắc, nguyên tắc nào sau đây là đúng?
- Nguyên tử khối tăng dần
- Cùng số lớp electron xếp cùng cột
- Điện tích hạt nhân tăng dần
- Cùng số electron hóa trị xếp cùng hàng
III. Cấu tạo bảng tuần hoàn
- Ô nguyên tố
Số hiệu nguyên tử
Nêu ý nghĩa của từng dữ liệu trong ô nguyên tố bên.
Ô nguyên tố: cho biết số hiệu nguyên tử, kí hiệu nguyên tố, tên nguyên tố và nguyên tử khối trung bình, …
- Chu kì
Hãy nêu nhận xét:
- Về số hiệu nguyên tử.
- Về số lớp electron và hình thành khái niệm chu kì.
- Mỗi nguyên tố trong chu kì 2 và và chu kì 3 có bao nhiêu lớp electron? Từ đó, em hãy nhận xét mối quan hệ giữa số lớp electron và số thứ tự chu kì.
Nhận xét về các hàng của bảng tuần hoàn:
- Điện tích hạt nhân tăng dần.
- Trong 1 hàng số lớp electron bằng
Trong chu kì 2, mỗi nguyên tố đều có 2 lớp electron trong nguyên tử:
B (Z=5) : 1s22s22p1 C (Z=6) : 1s22s22p2
N (Z=7) : 1s22s22p3
Kết luận: Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron được xếp theo chiều tăng dần của điện tích nguyên tử.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 10 kết nối tri thức
