Giáo án điện tử Hoá học 11 chân trời: Ôn tập chương 1
Bài giảng điện tử Hoá học 11 chân trời sáng tạo. Giáo án powerpoint Ôn tập chương 1. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 11 chân trời sáng tạo
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét








Xem toàn bộ: Giáo án điện tử hoá học 11 chân trời sáng tạo
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC HÔM NAY!
MẢNH GHÉP BÍ ẨN
YÊU CẦU
Lựa chọn mảnh ghép để trả lời câu hỏi tương ứng. Nếu trả lời đúng câu hỏi, mảnh ghép sẽ được mở khóa…!!!
BẮT ĐẦU
ĐÁP ÁN
Johannes Nicolaus Brønsted và Thomas Martin Lowry
Câu hỏi 1:
Dung dịch H2SO4 0,005 M có giá trị pH là bao nhiêu?
pH = 2
Câu hỏi 2:
Tại sao nước biển, nước ao hồ hay nước suối dẫn điện được?
Do bên trong nước ao hồ có lẫn các tạp chất như muối NaCl, có khả năng phân li ra các ion → nước có khả năng dẫn điện.
Câu hỏi 3:
Quá trình phân li các chất trong nước thành ion gọi là gì?
Sự điện li/ Hiện tượng điện li
Câu hỏi 4:
Các ion sau: Na+, Ba2+, Fe3+, Al3+, Zn2+ được gọi chung là gì?
Cation
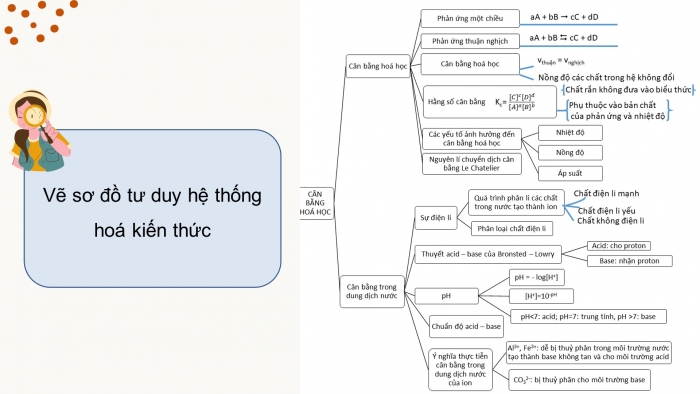
BÀI 3: ÔN TẬP CHƯƠNG I
Vẽ sơ đồ tư duy hệ thống hoá kiến thức
LUYỆN TẬP
Câu 1
Phát biểu nào sau đây đúng?
- Hằng số cân bằng KC của tất cả phản ứng đều tăng khi tăng nhiệt độ.
- Hằng số cân bằng KC càng nhỏ, hiệu suất phản ứng càng lớn.
- Khi một phản ứng thuận nghịch ở trạng thái cân bằng cũ chuyển sang một trạng thái cân bằng mới ở nhiệt độ không đổi, hằng số cân bằng KC cũng thay đổi.
- Khi thay dồi hệ số tỉ lượng các chất trong phương trình hoá học của một phản ứng, giá trị của hằng số cân bằng KC thay đổi.
Câu 2
Phát biểu nào sau đây đúng?
- Mọi phản ứng đều đạt đến trạng thái cân bằng hóa học
- Khi phản ứng thuận nghịch ở trạng thái cân bằng thì phản ứng dừng lại
- Chỉ có những phản ứng thuận nghịch mới có trạng thái cân bằng hoá học
- Ở trạng thái cân bằng, khối lượng các chất ở hai vế của phương trình phản ứng phải bằng nhau
Câu 3
Phương trình điện li nào sau đây không đúng?
- HCl → H+ + Cl-
- CH3CH2COOH ⇆ CH3CH2COO- + H+
- KCI ⇆ K+ + Cl-
- Ca(OH)2 → Ca2+ + 2OH-
Câu 4
Dãy các chất nào sau đây đều là chất điện li mạnh?
- KOH, NaCl, H2CO3
- Na2S, Zn(OH)2, HCl
- HClO2, KNO3, Ca(OH)2
- HNO3, Fe(NO3)2, Ba(OH)2
Câu 5
Chất nào dưới đây không phân li ra ion khi hòa tan trong nước?
- MgCl2
- HClO3
- Ba(OH)2
- C6H12O6 (glucose)
Câu 6
Phương trình 2H+ + S2-➝ H2S là phương trình ion rút gọn của phản ứng:
- FeS + HCl ➝ FeCl2 + H2S
- H2SO4 đặc + Mg ➝ MgSO4 + H2S + H2O
- K2S + 2HCl ➝ H2S + 2KCl
- BaS + H2SO4 ➝ BaSO4 + H2S
Câu 7
Chất nào sau đây thuộc loại chất điện li yếu?
- KCl
- HF
- HNO3
- NH4Cl
Câu 8
Đối với dung dịch axit yếu CH3COOH 0,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
- [H+] = 0,10M
- [H+] > [CH3COO-]
- [H+] < [CH3COO-]
- [H+] < 0,10 M
VẬN DỤNG
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 11 chân trời sáng tạo
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 11 CHÂN TRỜI SÁNG TẠO
GIÁO ÁN POWERPOINT LỚP 11 CHÂN TRỜI SÁNG TẠO
GIÁO ÁN CHUYÊN ĐỀ 11 CHÂN TRỜI SÁNG TẠO
GIÁO ÁN DẠY THÊM 11 CHÂN TRỜI SÁNG TẠO
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
