Giáo án điện tử Hoá học 11 chân trời Bài 1: Khái niệm về cân bằng hoá học
Bài giảng điện tử Hoá học 11 chân trời sáng tạo. Giáo án powerpoint Bài 1: Khái niệm về cân bằng hoá học. Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 11 chân trời sáng tạo
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét











Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 11 chân trời sáng tạo
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI
KHỞI ĐỘNG
- Trong các phản ứng hóa học, có một loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu ® Phản ứng xảy ra không hoàn toàn và thường có hiệu suất không cao.
- Phản ứng tổng hợp ammonia từ nitrogen và hydrogen thuộc loại phản ứng này.
Các phản ứng này được gọi là phản ứng gì?
Để tăng hiệu suất, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,… như thế nào?
CHƯƠNG I. CÂN BẰNG HOÁ HỌC
BÀI 1. KHÁI NIỆM VỀ CÂN BẰNG HOÁ HỌC
NỘI DUNG BÀI HỌC
Phản ứng một chiều, phản ứng thuận nghịch và cân bằng hoá học
Hằng số cân bằng của phản ứng thuận nghịch
Sự chuyển dịch cân bằng hoá học
Các yếu tố ảnh hưởng đến cân bằng hoá học
- PHẢN ỨNG MỘT CHIỀU, PHẢN ỨNG THUẬN NGHỊCH VÀ CÂN BẰNG HOÁ HỌC
- Phản ứng điều chế khí oxygen trong phòng thí nghiệm bằng cách đun nóng tinh thể KMnO4 (thuốc tím) tạo thành K2MnO4, MnO2, O2 có phương trình hóa học như sau:
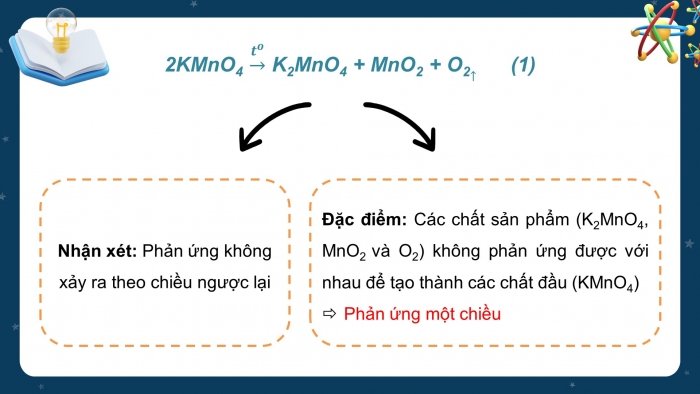
2KMnO4 K2MnO4 + MnO2 + O2 (1)
Câu hỏi thảo luận: Dựa vào phương trình hóa học của phản ứng điều chế khí oxygen từ KMnO4, em hãy cho biết phản ứng có xảy ra theo chiều ngược lại không?
Nhận xét: Phản ứng không xảy ra theo chiều ngược lại
Đặc điểm: Các chất sản phẩm (K2MnO4, MnO2 và O2) không phản ứng được với nhau để tạo thành các chất đầu (KMnO4)
- Phản ứng một chiều
Nhận xét
- Khái niệm: Phản ứng một chiều là phản ứng chỉ xảy ra theo chiều từ chất tham gia tạo thành sản phẩm mà sản phẩm không thể tác dụng lại với nhau để tạo thành chất ban đầu.
- Kí hiệu chiều phản ứng:
Ví dụ : NaOH + HCl NaCl + H2O
Vậy có phản ứng nào mà các chất sản phẩm lại phản ứng được với nhau để tạo thành chất đầu không ?
Phản ứng thuận nghịch
THẢO LUẬN NHÓM: Quan sát phản ứng sau và trả lời câu hỏi câu hỏi 2 (SGK tr.6)
Cl2(g) + H2O(l) HCl(aq) + HClO(aq) (2)
Phản ứng Cl2 tác dụng với H2O có đặc điểm gì khác với phản ứng nhiệt phân thuốc tím?
> Phản ứng trên xảy ra theo hai chiều, các chất sản phẩm tác dụng được với nhau tạo lại Cl2 và H2O
> Phản ứng thuận nghịch
Phản ứng thuận:
Cl2 + H2O HCl + HClO
Phản ứng nghịch:
HCl + HClO Cl2 + H2O
- Khái niệm: Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều ngược nhau trong cùng điều xác định.
- Kí hiệu chiều phản ứng: . Chiều từ trái sang phải là chiều thuận, chiều từ phải sang trái là chiều nghịch.
Ví dụ: 3O2 2O3
THẢO LUẬN NHÓM: Nghiên cứu trạng thái cân bằng hóa học thông qua phản ứng và trả lời câu hỏi 3, 4 (SGK tr.6)
N2(g) + 3H2(g) 2NH3(g)
Câu hỏi 3 (SGK tr.6). Quan sát Hình 1.1, nhận xét sự biến thiên nồng độ của các chất trong hệ phản ứng theo thời gian (với điều kiện nhiệt độ không đổi).
Trạng thái cân bằng
Câu hỏi 4 (SGK tr.6). Quan sát Hình 1.2, nhận xét về tốc độ của phản ứng thuận và tốc độ của phản ứng nghịch theo thời gian trong điều kiện nhiệt độ không đổi. Nồng độ các chất trong phản ứng thay đổi như thế?
Câu hỏi 3.
Theo thời gian: số mol N2, H2 giảm dần và đến một thời điểm ® Không thay đổi nữa
Theo thời gian: số mol NH3 tăng dần và đến cùng một thời điểm ® Không thay đổi nữa
Câu hỏi 4.
- Biểu thức định luật tác dụng khối lượng đối với phản ứng thuận:
vt = kt N2. H23
- Biểu thức định luật tác dụng khối lượng đối với phản ứng nghịch:
vn = kn NH32
Theo thời gian, số mol N2, H2 giảm dần
[N2] và [H2] giảm dần
Tốc độ phản ứng thuận giảm
Theo thời gian, số mol NH3 tăng dần
[NH3] tăng dần
Tốc độ phản ứng nghịch tăng
Nhận xét
- Trong thí nghiệm:
- Lúc đầu: Phản ứng thuận có tốc độ lớn hơn phản ứng nghịch, ưu tiên tạo ra ammonia.
- Theo thời gian: Tốc độ phản ứng thuận giảm dần, tốc độ phản ứng nghịch tăng dần đến khi tốc độ hai phản ứng bằng nhau.
- Tại thời điểm này: Số mol của các chất hydrogen, nitrogen, ammonia không thay đổi nữa.
- Thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng.
Trạng thái cân bằng
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 11 chân trời sáng tạo
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 11 CHÂN TRỜI SÁNG TẠO
GIÁO ÁN POWERPOINT LỚP 11 CHÂN TRỜI SÁNG TẠO
GIÁO ÁN CHUYÊN ĐỀ 11 CHÂN TRỜI SÁNG TẠO
GIÁO ÁN DẠY THÊM 11 CHÂN TRỜI SÁNG TẠO
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
