Giáo án điện tử Hoá học 11 cánh diều Bài 12: Alkane (Phần 1)
Bài giảng điện tử Hoá học 11 cánh diều. Giáo án powerpoint Bài 12: Alkane (Phần 1). Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 11 cánh diều
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét








Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 11 cánh diều
CHÀO MỪNG CẢ LỚP
QUAY TRỞ LẠI VỚI MÔN HỌC!
KHỞI ĐỘNG
Quan sát video và cho biết khí thiên nhiên thuộc loại hợp chất hữu cơ nào? Video cung cấp cho các em thông tin gì về khí thiên nhiên?
CHỦ ĐỀ 4: HYDROCARBON
BÀI 12: ALKANE
NỘI DUNG BÀI HỌC
Khái niệm và danh pháp
Tính chất vật lí
Tính chất hóa học
Nguồn alkane trong tự nhiên, ứng dụng của alkane
I.
KHÁI NIỆM VÀ DANH PHÁP
- Khái niệm
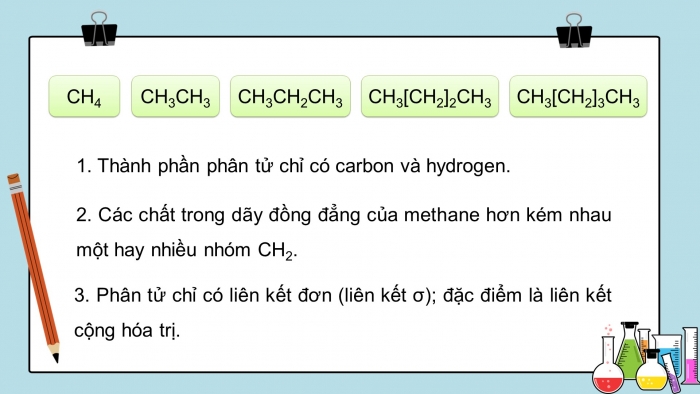
Cho một số chất thuộc dãy đồng đẳng của alkane:
- Nhận xét về thành phần nguyên tố của các chất trong dãy đồng đẳng của methane.
- Sự khác nhau về số lượng nguyên tử H và C tuân thủ theo luật nào?
- Nhận xét đặc điểm liên kết hóa học trong phân tử các chất.
- Thành phần phân tử chỉ có carbon và hydrogen.
- Các chất trong dãy đồng đẳng của methane hơn kém nhau một hay nhiều nhóm CH2.
- Phân tử chỉ có liên kết đơn (liên kết σ); đặc điểm là liên kết cộng hóa trị.
GHI NHỚ
- Alkane là hydrocarbon mạch hở, trong phân tử chỉ có liên kết đơn.
- Công thức chung: CnH2n+2 (n ≥ 1).
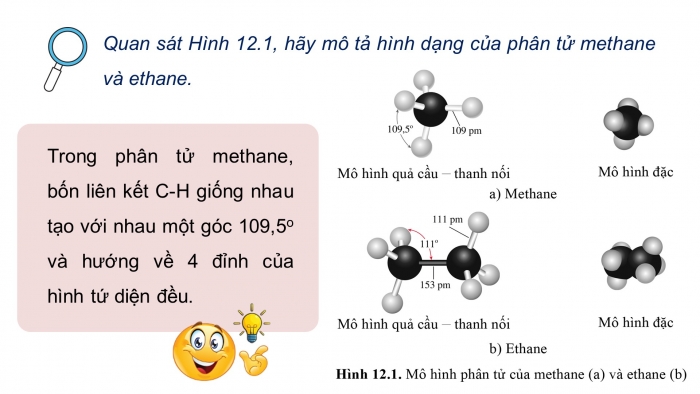
Quan sát Hình 12.1, hãy mô tả hình dạng của phân tử methane và ethane.
Trong phân tử methane, bốn liên kết C-H giống nhau tạo với nhau một góc 109,5o và hướng về 4 đỉnh của hình tứ diện đều.
Trong phân tử ethane, mỗi nguyên tử C nằm ở tâm của một tứ diện mà bốn đỉnh là các nguyên tử hydrogen và carbon, có góc liên kết khoảng 111o
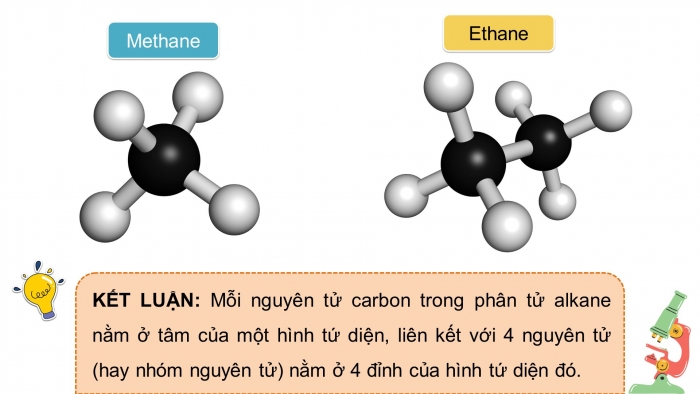
KẾT LUẬN: Mỗi nguyên tử carbon trong phân tử alkane nằm ở tâm của một hình tứ diện, liên kết với 4 nguyên tử (hay nhóm nguyên tử) nằm ở 4 đỉnh của hình tứ diện đó.
- Đồng phân
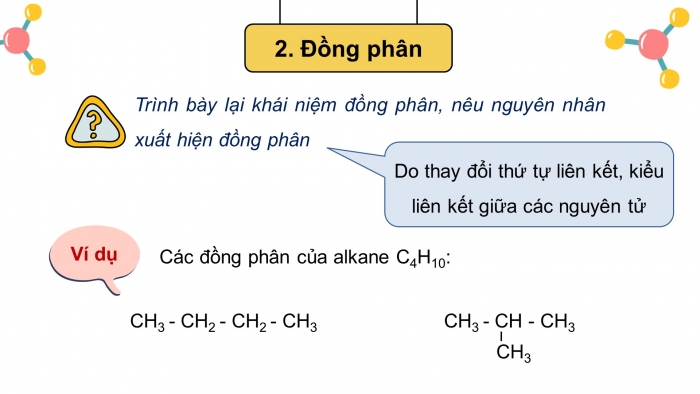
Trình bày lại khái niệm đồng phân, nêu nguyên nhân xuất hiện đồng phân
Do thay đổi thứ tự liên kết, kiểu liên kết giữa các nguyên tử
Ví dụ
Các đồng phân của alkane C4H10:
GHI NHỚ
Các alkane có từ bốn nguyên tử C trở lên có đồng phân về mạch carbon.
Các alkane mạch không phân nhánh có mạch carbon mà trong đó mỗi nguyên tử carbon chỉ liên kết với tối đa hai nguyên tử carbon khác.
Alkane mạch phân nhánh chứa nguyên tử carbon liên kết với ba hoặc bốn nguyên tử carbon khác.
Viết các đồng phân cấu tạo của alkane có công thức phân tử C5H12
- Danh pháp
Quan sát tên gọi của 10 alkane mạch không nhánh đầu tiên qua Bảng 12.1 SGK trang 75 và học thuộc tên 5 alkane mạch không nhánh đầu tiên (C1–C5)
GHI NHỚ
- Theo danh pháp thay thế, tên của alkane gồm hai phần:
Phần tiền tố (chỉ số lượng nguyên tử C trong mạch carbon)
Cho biết số lượng nguyên tử carbon cũng được sử dụng chung cho các loại hợp chất hữu cơ khác có cùng số lượng nguyên tử carbon
- Tên của alkane mạch phân nhánh:
Vị trí nhóm thế alkyl
tên nhóm thế alkyl
tên alkane mạch chính
Trong đó:
- Mạch carbon dài nhất là mạch chính.
- Mạch carbon còn lại là mạch nhánh, được xem là nhóm thế alkyl của mạch chính.
- Vị trí nhóm thế alkyl là vị trí của nguyên tử carbon trong mạch chính liên kết với nhóm thế đó.
- Đánh số các nguyên tử C trên mạch chính xuất phát từ đầu gần mạch nhánh nhất để tổng số chỉ vị trí của các nhánh là nhỏ nhất.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 11 cánh diều
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 11 CÁNH DIỀU
GIÁO ÁN POWERPOINT LỚP 11 CÁNH DIỀU
GIÁO ÁN CHUYÊN ĐỀ LỚP 11 CÁNH DIỀU
Giáo án chuyên đề Công nghệ cơ khí 11 cánh diều đủ cả năm
Giáo án chuyên đề Tin học 11 Khoa học máy tính cánh diều đủ cả năm
Giáo án chuyên đề Tin học 11 Tin học ứng dụng cánh diều đủ cả năm
Giáo án chuyên đề Âm nhạc 11 cánh diều đủ cả năm
Giáo án chuyên đề Kinh tế pháp luật 11 cánh diều đủ cả năm
GIÁO ÁN DẠY THÊM LỚP 11 CÁNH DIỀU
Giáo án dạy thêm toán 11 cánh diều đủ cả năm
Giáo án dạy thêm ngữ văn 11 cánh diều đủ cả năm
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
