Giáo án điện tử Hoá học 11 kết nối Bài 8: Sulfuric acid và muối sulfate (Phần 1)
Bài giảng điện tử Hoá học 11 kết nối tri thức. Giáo án powerpoint Bài 8: Sulfuric acid và muối sulfate (Phần 1). Giáo án thiết kế theo phong cách hiện đại, nội dung đầy đủ, đẹp mắt, tạo hứng thú học tập cho học sinh. Thầy, cô giáo có thể tham khảo.
Xem: => Giáo án hóa học 11 kết nối tri thức
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét






Các tài liệu bổ trợ khác
Xem toàn bộ: Giáo án điện tử hoá học 11 kết nối tri thức
CHÀO MỪNG CÁC EM ĐẾN VỚI TIẾT HỌC HÔM NAY!
KHỞI ĐỘNG
Số 6: Thực phẩm nào được dùng thay thế cho mỡ động vật trong các gia đình?
OXI HOA
BÀI 8: SULFURIC ACID VÀ MUỐI SULFATE
NỘI DUNG BÀI HỌC
- SULFURIC ACID
- MUỐI SULFATE
- SULFURIC ACID
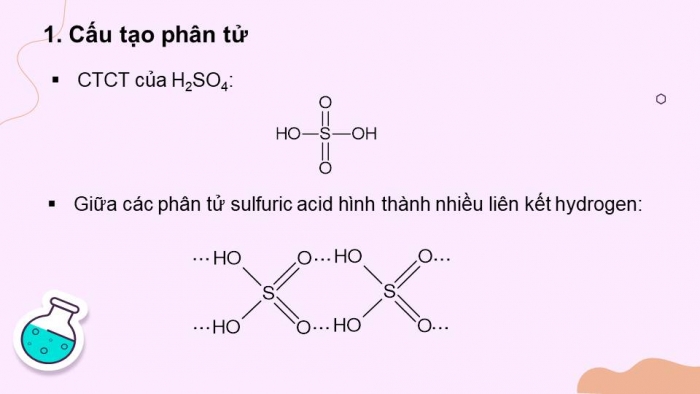
- Cấu tạo phân tử
- CTCT của H2SO4:
- Giữa các phân tử sulfuric acid hình thành nhiều liên kết hydrogen:
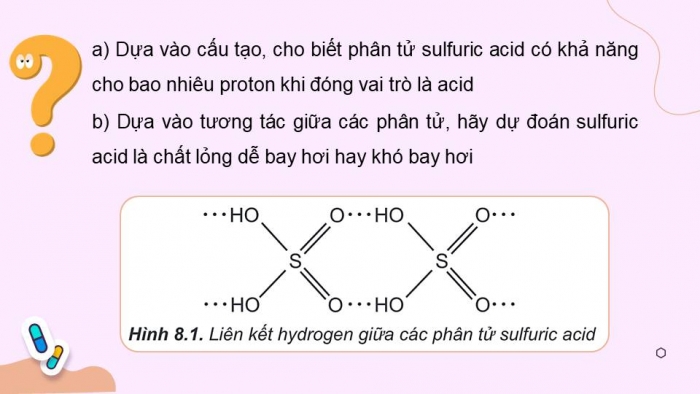
- a) Dựa vào cấu tạo, cho biết phân tử sulfuric acid có khả năng cho bao nhiêu proton khi đóng vai trò là acid
- b) Dựa vào tương tác giữa các phân tử, hãy dự đoán sulfuric acid là chất lỏng dễ bay hơi hay khó bay hơi
Trả lời
- a) Từ cấu tạo phân tử cho thấy, phân tử H2SO4 có hai liên kết O – H phân cực mạnh, có khả năng cho 2 proton là acid hai nấc
H2SO4 + H2O
+ H2O
+ H3O+
Trả lời
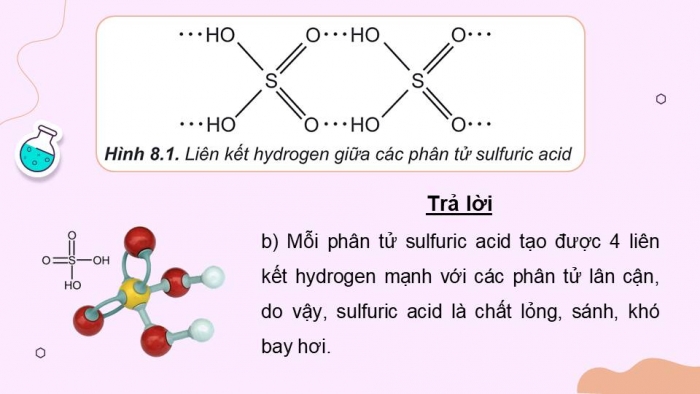
- b) Mỗi phân tử sulfuric acid tạo được 4 liên kết hydrogen mạnh với các phân tử lân cận, do vậy, sulfuric acid là chất lỏng, sánh, khó bay hơi.
THẢO LUẬN NHÓM ĐÔI
1
Nêu tính chất vật lí của Sulfuric acid khi ở điều kiện thường
2 Cho biết tính tan của H2SO4 trong nước
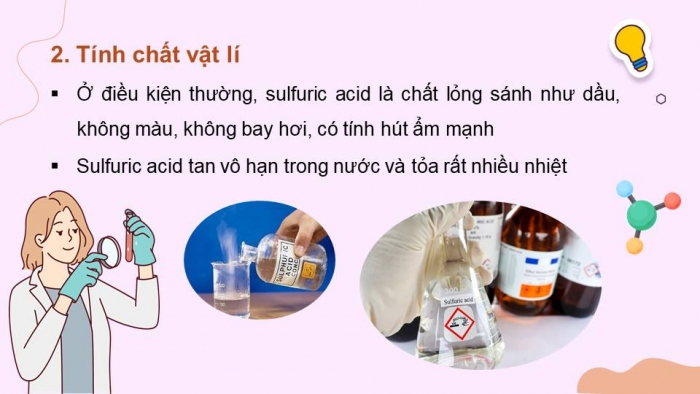
- Tính chất vật lí
- Ở điều kiện thường, sulfuric acid là chất lỏng sánh như dầu, không màu, không bay hơi, có tính hút ẩm mạnh
- Sulfuric acid tan vô hạn trong nước và tỏa rất nhiều nhiệt
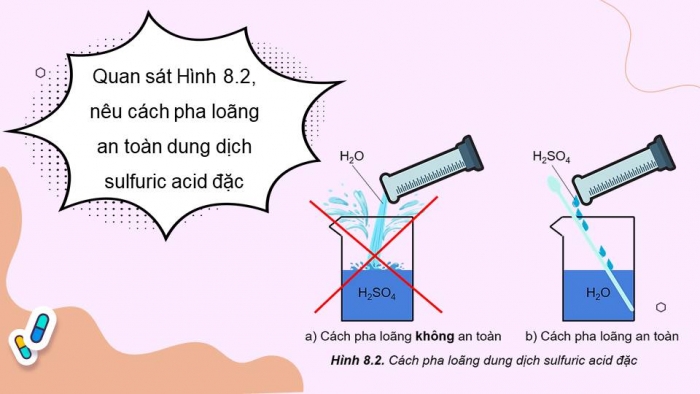
Quan sát Hình 8.2, nêu cách pha loãng an toàn dung dịch sulfuric acid đặc
Khi pha loãng dung dịch sulfuric acid đặc, để đảm bảo an toàn phải rót từ từ dung dịch sulfuric acid đặc vào nước, vừa rót vừa khuấy (không làm ngược lại)
- Quy tắc an toàn
Bảo quản
Sulfuric acid được bảo quản trong chai, lọ có nút đậy chặt, đặt ở vị trí chắc chắn, cách xa các lọ chứa dễ gây cháy nổ
- Quy tắc an toàn
Sử dụng
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng
(5) Không được đổ nước vào dung dịch acid đặc
- Quy tắc an toàn
Sơ cứu khi bỏng aicd
(1) Nhanh chóng rửa ngay với nước lạnh nhiều lần:
- Nếu bỏng ở vùng mặt thì nhắm chặt mắt khi ngâm rửa
- Nếu acid bắn vào mắt thì úp mặt vào chậu nước sạch, mở mắt và chớp nhiều lần để rửa acid
(2) Tiến hành trung hòa acid bằng NaHCO3 loãng (2%)
(3) Băng bó tạm thời vết bỏng bằng băng sạch, uống bù nước điện giải rồi đến cơ sở y tế gần nhất
- Tính chất hóa học
- a) Dung dịch sulfuric acid loãng
Câu 1 (SGK – tr50). Em hãy cho biết các tính chất hoá học cơ bản của một acid.
Câu 2 (SGK – tr50) Viết phương trình hoá học minh hoạ tính acid của dung dịch H2SO4 loãng với: kim loại Fe, bột MgO, dung dịch Na2CO3, dung dịch BaCl2.
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử hoá học 11 kết nối tri thức
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 11 KẾT NỐI TRI THỨC
GIÁO ÁN POWERPOINT LỚP 11 KẾT NỐI TRI THỨC
GIÁO ÁN CHUYÊN ĐỀ LỚP 11 KẾT NỐI TRI THỨC
GIÁO ÁN DẠY THÊM 11 KẾT NỐI TRI THỨC
CÁCH ĐẶT MUA:
Liên hệ Zalo: Fidutech - nhấn vào đây
