Giáo án kì 2 Hoá học 12 kết nối tri thức
Đầy đủ giáo án kì 2, giáo án cả năm Hoá học 12 kết nối tri thức. Bộ giáo án chất lượng, chỉn chu, được hỗ trợ tốt nhất hiện nay. Khi mua giáo án được tặng thêm: bộ phiếu trắc nghiệm, bộ đề kiểm tra theo cấu trúc mới. Giáo án được gửi ngay và luôn. Có thể xem trước bất kì bài nào phía dưới trước khi mua.
Một số tài liệu quan tâm khác
Phần trình bày nội dung giáo án
I. GIÁO ÁN WORD KÌ 2 HOÁ HỌC 12 KẾT NỐI TRI THỨC
- Giáo án Hoá học 12 kết nối Bài 15: Thế điện cực và nguồn điện hoá học
- Giáo án Hoá học 12 kết nối Bài 16: Điện phân
- Giáo án Hoá học 12 kết nối Bài 17: Ôn tập chương 5
- Giáo án Hoá học 12 kết nối Bài 18: Cấu tạo và liên kết trong tinh thể kim loại
- Giáo án Hoá học 12 kết nối Bài 19: Tính chất vật lí và tính chất hoá học của kim loại
- Giáo án Hoá học 12 kết nối Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại
- Giáo án Hoá học 12 kết nối Bài 21: Hợp kim
- Giáo án Hoá học 12 kết nối Bài 22: Sự ăn mòn kim loại
- Giáo án Hoá học 12 kết nối Bài 23: Ôn tập chương 6
- Giáo án Hoá học 12 kết nối Bài 24: Nguyên tố nhóm IA
- Giáo án Hoá học 12 kết nối Bài 25: Nguyên tố nhóm IIA
- Giáo án Hoá học 12 kết nối Bài 26: Ôn tập chương 7
- Giáo án Hoá học 12 kết nối Bài 27: Đại cương về kim loại chuyển tiếp dãy thứ nhất
- Giáo án Hoá học 12 kết nối Bài 28: Sơ lược về phức chất
- Giáo án Hoá học 12 kết nối Bài 29: Một số tính chất và ứng dụng của phức chất
- Giáo án Hoá học 12 kết nối Bài 30: Ôn tập chương 8
Ngày soạn:…/…/…
Ngày dạy:…/…/…
CHƯƠNG 6: ĐẠI CƯƠNG VỀ KIM LOẠI
BÀI 18. CẤU TẠO VÀ LIÊN KẾT TRONG TINH THỂ KIM LOẠI
I. MỤC TIÊU
1. Về kiến thức
Sau bài học này, HS sẽ:
Trình bày được đặc điểm cấu tạo của nguyên tử kim loại và tinh thể kim loại.
Nêu được đặc điểm của liên kết kim loại.
2. Năng lực
Năng lực chung:
Năng lực giao tiếp và hợp tác: Chủ động giao tiếp trong nhóm, trình bày rõ ý tưởng cá nhân và hỗ trợ nhau hoàn thành nhiệm vụ chung, tự tin và biết kiểm soát cảm xúc, thái độ khi nói trước nhiều người.
Năng lực giải quyết vấn đề và sáng tạo: Thu thập và làm rõ thông tin có liên quan đến vấn đề; phân tích để xây dựng được các ý tưởng phù hợp.
Năng lực đặc thù:
Năng lực vận dụng kiến thức, kĩ năng đã học: Nhận ra, giải thích được vấn đề thực tiễn dựa trên kiến thức hoá học.
Năng lực tìm hiểu tự nhiên dưới góc độ hoá học:
Sử dụng được ngôn ngữ, hình vẽ, sơ đồ, biểu bảng để biểu đạt quá trình tìm hiểu vấn đề và kết quả tìm kiếm.
Viết được báo cáo quá trình tìm hiểu.
Năng lực nhận thức hoá học:
Trình bày được đặc điểm cấu tạo của nguyên tử kim loại và tinh thể kim loại.
Nêu được đặc điểm của liên kết kim loại.
3. Phẩm chất
Tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
Cẩn trọng, trung thực và thực hiện các yêu cầu trong bài học.
Sử dụng tiết kiệm, an toàn các sản phẩm bằng kim loại.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Đối với giáo viên
Tài liệu: SGK, SGV Hóa học 12, các hình ảnh liên quan đến bài học.
Thiết bị dạy học: Máy tính, máy chiếu.
2. Đối với học sinh
Tài liệu: SGK Hóa học 12.
Tranh ảnh, tư liệu sưu tầm liên quan đến bài học theo yêu cầu của GV.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a. Mục tiêu:
- Huy động được vốn hiểu biết, kĩ năng có sẵn của học sinh về ứng dụng của kim loại để chuẩn bị cho bài học mới; học sinh cảm thấy vấn đề sắp học rất gần gũi với mình.
- Kích thích sự tò mò, khơi dậy hứng thú của học sinh về chủ đề sẽ học; tạo không khí lớp học sôi nổi, chờ đợi, thích thú.
- Học sinh trải nghiệm qua tình huống có vấn đề, trong đó chứa đựng những nội dung kiến thức, những kĩ năng để phát triển phẩm chất, năng lực mới.
b. Nội dung: HS quan sát hình ảnh GV cung cấp và thực hiện yêu cầu của GV.
c. Sản phẩm: Câu trả lời của HS về một số ứng dụng của kim loại.
d. Tổ chức thực hiện
Bước 1: GV chuyển giao nhiệm vụ học tập
- GV yêu cầu HS quan sát các hình sau.
|
|
|
Thép | Đồng | Vàng |
GV nêu câu hỏi: Em hãy cho biết ứng dụng của các kim loại tương ứng với mỗi hình.
Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập
- HS làm việc cá nhân, tham gia trò chơi và suy nghĩ trả lời câu hỏi của GV.
- GV hướng dẫn, hỗ trợ HS (nếu cần thiết).
Bước 3: Báo cáo kết quả hoạt động, thảo luận
- GV mời 2 – 3 HS trả lời câu hỏi:
+ Thép: là vật liệu xây dựng.
+ Đồng: lõi dây dẫn điện.
+ Vàng: trang sức.
- Các HS khác lắng nghe để nhận xét câu trả lời của bạn mình.
- GV khuyến khích HS có thể có nhiều ý kiến khác nhau.
Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập
- GV đánh giá, nhận xét của câu trả lời HS, dẫn dắt HS vào bài học: Kim loại được sử dụng nhiều trong cuộc sống như các kết cấu bằng thép, dây dẫn điện bằng đồng, đồ trang sức bằng vàng,…. Kim loại có đặc điểm gì về cấu tạo nguyên tử và liên kết mà hữu dụng như vậy? Để đi tìm câu trả lời, chúng ta cùng vào bài học ngày hôm nay Bài 18 – Cấu tạo và liên kết trong tinh thể kim loại.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
Hoạt động 1. Đặc điểm cấu tạo nguyên tử kim loại
a. Mục tiêu: HS trình bày được đặc điểm cấu tạo của nguyên tử kim loại.
b. Nội dung: HS đọc thông tin trong SGK trang 87 và thực hiện yêu cầu của GV.
c. Sản phẩm: Câu trả lời của HS về đặc điểm cấu tạo của nguyên tử kim loại.
d. Tổ chức hoạt động:
HOẠT ĐỘNG CỦA GV - HS | DỰ KIẾN SẢN PHẨM |
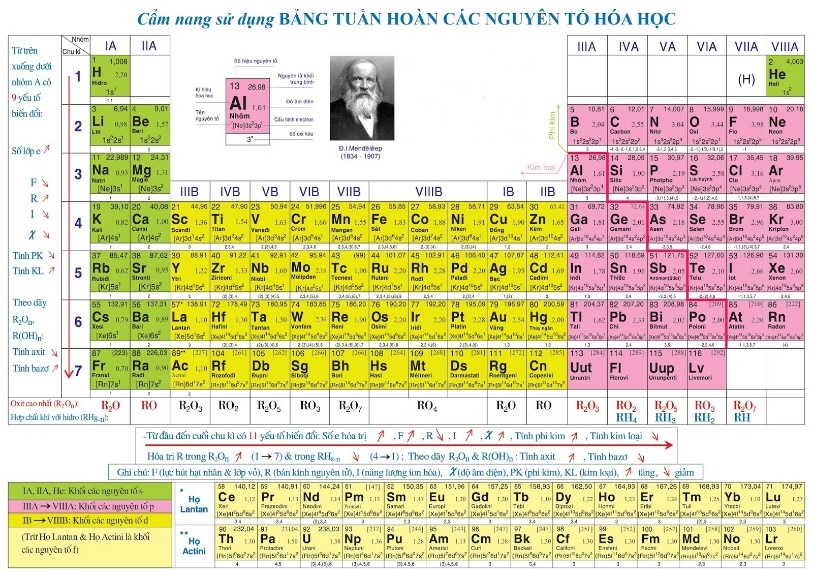
Bước 1: GV chuyển giao nhiệm vụ học tập - GV tổ chức cho HS quan sát bảng tuần hoàn các nguyên tố hóa học:
- GV yêu cầu HS dựa vào kiến thức đã biết, hoàn thành câu hỏi mục Hoạt động: Dựa vào bảng tuần hoàn các nguyên tố hóa học, hãy cho biết: 1. Các nguyên tố khối s, d, f thường là kim loại hay phi kim? 2. Kể tên các kim loại thuộc nhóm IA và IIA. 3. Các nguyên tố kim loại thường có bao nhiêu electron ở lớp ngoài cùng? - GV tổ chức cho HS vận dụng kiến thức đã học để trả lời Câu hỏi 1: Viết cấu hình electron nguyên tử của Sc (Z = 21) và Ti (Z = 22). Cho biết số electron ở lớp ngoài cùng và trên phân lớp d sát lớp ngoài cùng. Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập - HS quan sát hình, vận dụng kiến thức đã học kết hợp đọc thông tin trong SGK để trả lời câu hỏi. - GV hướng dẫn, hỗ trợ HS (nếu cần thiết). Bước 3: Báo cáo kết quả hoạt động, thảo luận - GV mời đại diện 2 – 3 HS trả lời câu hỏi. * Trả lời câu hỏi mục Hoạt động (DKSP). * Trả lời mục Câu hỏi: + Cấu hình electron: Sc (Z = 21): 1s22s22p63s23p63d14s2; Ti (Z = 22): 1s22s22p63s23p63d24s2. + Tổng số electron ở lớp ngoài cùng và trên phân lớp sát lớp ngoài cùng của Sc là 3, Ti là 4. - GV yêu cầu các HS khác lắng nghe, nhận xét, nêu ý kiến bổ sung (nếu có). Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập - GV đánh giá câu trả lời của HS, đưa ra kết luận về đặc điểm cấu tạo nguyên tử kim loại. - GV chuyển sang nội dung mới. | I. Đặc điểm cấu tạo của nguyên tử kim loại - Các nguyên tố khối s, d, f thường là kim loại. - Các kim loại thuộc nhóm IA: Li, Na, K, Rb, Cs và Fr (Fr là nguyên tố phóng xạ). - Các kim loại thuộc nhóm IIA: Be, Mg, Ca, Sr, Ba. - Nguyên tử của các nguyên tố kim loại thường có 1, 2 hoặc 3 electron ở lớp ngoài cùng. - Trong cùng một chu kì, so với các nguyên tử nguyên tố phi kim, nguyên tử kim loại có điện tích hạt nhân nhỏ hơn và bán kính lớn hơn nên dễ nhường electron hóa trị hơn, có độ âm điện nhỏ hơn.
|
------------------------- Còn tiếp -------------------------
Ngày soạn:…/…/…
Ngày dạy:…/…/…
BÀI 21. HỢP KIM
I. MỤC TIÊU
1. Về kiến thức
Sau bài học này, HS sẽ:
Trình bày được khái niệm hợp kim và việc sử dụng phổ biến hợp kim.
Trình bày được một số tính chất của hợp kim so với kim loại thành phần.
Nêu được thành phần, tính chất và ứng dụng của một số hợp kim quan trọng của sắt và nhôm (gang, thép, duralumin,…).
2. Năng lực
Năng lực chung:
Năng lực giao tiếp và hợp tác: Chủ động giao tiếp trong nhóm, trình bày rõ ý tưởng cá nhân và hỗ trợ nhau hoàn thành nhiệm vụ chung, tự tin và biết kiểm soát cảm xúc, thái độ khi nói trước nhiều người.
Năng lực giải quyết vấn đề và sáng tạo: Thu thập và làm rõ thông tin có liên quan đến vấn đề; phân tích để xây dựng được các ý tưởng phù hợp.
Năng lực đặc thù:
Năng lực vận dụng kiến thức, kĩ năng đã học: Nhận ra, giải thích được vấn đề thực tiễn dựa trên kiến thức hoá học.
Năng lực tìm hiểu tự nhiên dưới góc độ hoá học:
Sử dụng được ngôn ngữ, hình vẽ, sơ đồ, biểu bảng để biểu đạt quá trình tìm hiểu vấn đề và kết quả tìm kiếm.
Viết được báo cáo quá trình tìm hiểu.
Năng lực nhận thức hoá học:
Trình bày được khái niệm hợp kim và việc sử dụng phổ biến hợp kim.
Trình bày được một số tính chất của hợp kim so với kim loại thành phần.
Nêu được thành phần, tính chất và ứng dụng của một số hợp kim quan trọng của sắt và nhôm (gang, thép, duralumin,…).
3. Phẩm chất
Tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
Cẩn trọng, trung thực và thực hiện các yêu cầu trong bài học.
Sử dụng tiết kiệm các nguyên, vật liệu bằng hợp kim.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Đối với giáo viên
Tài liệu: SGK, SGV Hóa học 12, các hình ảnh liên quan đến bài học.
Thiết bị dạy học: Máy tính, máy chiếu.
2. Đối với học sinh
Tài liệu: SGK Hóa học 12.
Tranh ảnh, tư liệu sưu tầm liên quan đến bài học theo yêu cầu của GV.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a. Mục tiêu:
- Huy động được vốn hiểu biết, kĩ năng có sẵn của học sinh về hợp kim (đã được học trong Khoa học Tự nhiên 9, bài 20) để chuẩn bị cho bài học mới; học sinh cảm thấy vấn đề sắp học rất gần gũi với mình.
- Kích thích sự tò mò, khơi dậy hứng thú của học sinh về chủ đề sẽ học; tạo không khí lớp học sôi nổi, chờ đợi, thích thú.
- Học sinh trải nghiệm qua tình huống có vấn đề, trong đó chứa đựng những nội dung kiến thức, những kĩ năng để phát triển phẩm chất, năng lực mới.
b. Nội dung: HS quan sát hình và thực hiện yêu cầu của GV.
c. Sản phẩm: HS nêu được một số ứng dụng của hợp kim.
d. Tổ chức thực hiện
Bước 1: GV chuyển giao nhiệm vụ học tập
- GV yêu cầu HS quan sát hình ảnh một số ứng dụng của hợp kim.
 |  |  |
Khung xe đạp | Khung ô tô | Thân vỏ máy bay |
GV yêu cầu HS dựa vào hình và kiến thức đã học để trả lời câu hỏi: Em hãy cho biết các bộ phận trong hình trên được làm từ loại vật liệu nào?
Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập
- HS làm việc cá nhân, suy nghĩ trả lời câu hỏi của GV.
- GV hướng dẫn, hỗ trợ HS (nếu cần thiết).
Bước 3: Báo cáo kết quả hoạt động, thảo luận
- GV mời 2 – 3 HS trả lời câu hỏi: Các bộ phận trên được làm từ hợp kim.
- Các HS khác lắng nghe để nhận xét câu trả lời của bạn mình.
- GV khuyến khích HS có thể có nhiều ý kiến khác nhau.
Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập
- GV đánh giá, nhận xét của câu trả lời HS, dẫn dắt HS vào bài học: Khung xe đạp, xe máy, ô tô hay thân vỏ máy bay thường được làm bằng hợp kim. Trong bài học hôm nay Bài 21 – Hợp kim chúng ta sẽ cùng ôn lại khái niệm hợp kim cũng như xác định những tính chất khác biệt của hợp kim so với kim loại thành phần giúp chúng được sử dụng rộng rãi.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
Hoạt động 1. Xây dựng khái niệm hợp kim
a. Mục tiêu: HS trình bày được khái niệm hợp kim, nhận biết được một số loại hợp kim.
b. Nội dung: HS đọc thông tin trong SGK trang 99 và trả lời các câu hỏi của GV.
c. Sản phẩm: Câu trả lời của HS về khái niệm hợp kim, nhận biết được một số loại hợp kim.
d. Tổ chức hoạt động:
HOẠT ĐỘNG CỦA GV - HS | DỰ KIẾN SẢN PHẨM |
Bước 1: GV chuyển giao nhiệm vụ học tập - GV yêu cầu HS quan sát hình sau:
- GV cho biết: Gang là hợp kim của Fe với C. - GV nêu câu hỏi: Hợp kim là gì? Hợp kim được điều chế như thế nào? - GV tổ chức cho HS làm việc nhóm đôi, tìm hiểu thông tin để trả lời câu hỏi Hoạt động. - GV yêu cầu HS quan sát hình sau:
- GV yêu cầu HS dựa vào hình và thông tin trong SGK, trả lời Câu hỏi 1: Hãy nêu tên và ứng dụng của một số hợp kim thông dụng của nhôm và sắt. Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập - HS quan sát hình, đọc thông tin trong bài, thảo luận nhóm để thực hiện yêu cầu của GV. - GV hướng dẫn, hỗ trợ HS (nếu cần thiết); ghi lại những HS tích cực, những HS chưa tích cực để điều chỉnh. Bước 3: Báo cáo kết quả hoạt động, thảo luận - GV mời đại diện 2 - 3 HS xung phong trả lời: * Trả lời câu hỏi của GV (DKSP). * Trả lời mục Hoạt động: a) Hợp kim duralumin, thành phần chính là nhôm hay hợp kim titanium, thành phần chính là titanium là những hợp kim nhẹ, bền, chịu được nhiệt độ cao và áp suất cao dùng để tạo tên lửa, tàu vũ trụ, máy bay, ô tô,… b) Thép, thành phần chính là sắt và carbon là hợp kim cứng và bền dùng để xây dựng nhà cửa và cầu cống. * Trả lời Câu hỏi 1: Thép được sử dụng trong xây dựng nhà và xây cầu. Duralumin được sử dụng trong chế tạo tàu vũ trụ, tên lửa, máy bay, ô tô,… Inox hay thép không gỉ được sử dụng chế tạo dụng cụ y tế và nhà bếp. - Các HS khác lắng nghe, nhận xét, nêu ý kiến bổ sung (nếu có). Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập - GV đánh giá câu trả lời của HS, đưa ra kết luận về khái niệm và ứng dụng của hợp kim. - GV chuyển sang nội dung mới. | I. Khái niệm và ứng dụng của hợp kim 1. Khái niệm hợp kim - Là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim. - Thường được điều chế bằng cách nung chảy các thành phần rồi để nguội. 2. Ứng dụng của hợp kim - Hợp kim được sử dụng rộng rãi trong đời sống và sản xuất: + Trong lĩnh vực chế tạo máy bay, ô tô,… sử dụng hợp kim nhẹ, bền, chịu nhiệt,… + Công nghiệp hóa chất sử dụng hợp kim có tính bền hóa học và cơ học cao,… + Đồ gia dụng làm từ hợp kim không gỉ, không độc hại,… |
------------------------- Còn tiếp -------------------------
II. TRẮC NGHIỆM KÌ 2 HOÁ HỌC 12 KẾT NỐI TRI THỨC
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 15: Thế điện cực và nguồn điện hoá học
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 16: Điện phân
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 17: Ôn tập chương 5
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 18: Cấu tạo và liên kết trong tinh thể kim loại
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 19: Tính chất vật lí và tính chất hoá học của kim loại
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 21: Hợp kim
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 22: Sự ăn mòn kim loại
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 23: Ôn tập chương 6
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 24: Nguyên tố nhóm IA
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 25: Nguyên tố nhóm IIA
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 26: Ôn tập chương 7
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 27: Đại cương về kim loại chuyển tiếp dãy thứ nhất
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 28: Sơ lược về phức chất
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 29: Một số tính chất và ứng dụng của phức chất
- Phiếu trắc nghiệm Hoá học 12 kết nối Bài 30: Ôn tập chương 8
CHƯƠNG 7. NGUYÊN TỐ NHÓM IA VÀ NHÓM IIA
BÀI 24. NGUYÊN TỐ NHÓM IA
(30 CÂU)
A. TRẮC NGHIỆM NHIỀU LỰA CHỌN
1. NHẬN BIẾT (10 CÂU)
Câu 1: Cấu hình electron lớp ngoài cùng của nguyên tử kim loại nhóm IA là
A. ns2np2.
B. ns2np1.
C. ns1.
D. ns2.
Câu 2: Kim loại nào sau đây thuộc nhóm IA trong bảng tuần hoàn?
A. Al.
B. Na.
C. Fe.
D. Ba.
Câu 3: Cấu hình electron của nguyên tử Na (Z=11)
A. 1s22s22p63s2.
B. 1s22s22p6.
C. 1s22s22p63s1.
D. 1s22s22p63s23p1.
Câu 4: Cation M+ có cấu hình electron lớp ngoài cùng 2s22p6 là:
A. Na+
B. Li+
C. Rb+
D. K+
Câu 5: Công thức chung của oxide kim loại thuộc phân nhóm chính nhóm I là
A. R2O3.
B. RO2.
C. R2O.
D. RO.
Câu 6: Trong phòng thí nghiệm, kim loại Na được bảo quản bằng cách ngâm trong chất lỏng nào sau đây?
A. Nước.
B. Dầu hỏa.
C. Giấm ăn.
D. Ethanol.
Câu 7: Cho dãy các kim loại: Na, Cu, Al, Cr. Kim loại mềm nhất trong dãy là
A. Cu.
B. Al.
C. Cr.
D. Na.
Câu 8: Kim loại phản ứng với nước ở nhiệt độ thường là
A. Fe.
B. Cu.
C. Be.
D. K.
…………………….
2. THÔNG HIỂU (5 CÂU)
Câu 1: Dung dịch Na2CO3 tác dụng được với dung dịch nào sau đây?
A. Na2SO4.
B. KNO3.
C. KOH.
D. CaCl2.
Câu 2: Phát biểu nào sau đây không đúng về kim loại kiềm?
A. Nhiệt độ nóng chảy và nhiệt độ sôi thấp.
B. Khối lượng riêng nhỏ.
C. Độ cứng giảm dần từ Li đến Cs
D. Mạng tinh thể của kim loại kiềm là lập phương tâm diện.
Câu 3: Chọn phát biểu đúng:
A. Dung dịch Na2CO3 có tính kiềm mạnh.
B. Dung dịch Na2CO3 có môi trường trung tính có Na2CO3 là muối trung hòa.
C. Dung dịch chứa Na2CO3 có môi trường axit do Na2CO3 là muối của acid yếu.
D. Na2CO3 dễ bị phân hủy khi đun nóng.
……………….
B. TRẮC NGHIỆM ĐÚNG - SAI
Học sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Cho các phát biểu sau:
a) Kim loại kiềm có bán kính nguyên tử tăng dần từ Li đến Cs.
b) Kim loại kiềm có tính khử mạnh nhất trong số các kim loại.
c) Kim loại kiềm tác dụng với nước ở điều kiện thường tạo ra base mạnh và khí hydrogen.
d) Kim loại kiềm có thể tác dụng trực tiếp với nitrogen ở nhiệt độ thường.
Trả lời:
a) S
b) Đ
c) Đ
d) S
------------------------- Còn tiếp -------------------------
CHƯƠNG 8. SƠ LƯỢC VỀ DÃY KIM LOẠI CHUYỂN TIẾP THỨ NHẤT VÀ PHỨC CHẤT
BÀI 28. SƠ LƯỢC VỀ PHỨC CHẤT
(17CÂU)
A. TRẮC NGHIỆM NHIỀU LỰA CHỌN
1. NHẬN BIẾT (8 CÂU)
Câu 1: Phức chất là gì?
A. Là hỗn hợp có chứa nguyên tử trung tâm và các phối tử.
B. Là hợp kim có chứa nguyên tử trung tâm và các phối tử.
C. Là hợp chất có chứa nguyên tử trung tâm và các nguyên tử xung quanh.
D. Là hợp chất có chứa nguyên tử trung tâm và các phối tử.
Câu 2: Phối từ trong phức chất có kí hiệu là
A. L.
B. M.
C. N.
D. P.
Câu 3: Nguyên tử trung tâm trong phức chất có kí hiệu là
A. L.
B. M.
C. N.
D. P.
Câu 4: Điện tích của phức chất [Fe(CO)5] là
A. -2.
B. +5.
C. +2.
D. 0.
Câu 5: Phối từ trong phức chất [Co(NH3)6]3+ là
A. Co.
B. NH3.
C. 3+.
D. (NH3)6.
…………………..
2. THÔNG HIỂU (5 CÂU)
Câu 1: Dạng hình học của phức chất [Cu(H2O)6]2+ là
A. tứ diện đều.
B. chóp tam giác.
C. vuông phẳng.
D. bát diện
Câu 2: Dạng hình học của phức chất [Zn(CN)4]2–
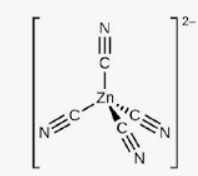
A. tứ diện.
B. chóp tam giác.
C. vuông phẳng.
D. bát diện
…………………
B. TRẮC NGHIỆM ĐÚNG - SAI
Học sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Cho các phát biểu sau:
a) Phức chất là hợp chất được tạo thành bởi ion kim loại trung tâm liên kết với các phân tử hoặc ion khác (gọi là phối tử) thông qua liên kết ion.
b) Số phối hợp (số phối trí) của ion kim loại trung tâm trong phức chất là số lượng tối đa các phối tử có thể liên kết với ion kim loại đó.
c) Hình dạng của phức chất được xác định bởi lý thuyết trường tinh thể.
d) Hình dạng của phức chất được xác định bởi lý thuyết VSEPR
Trả lời:
a) S
b) Đ
c) S
d) Đ
------------------------- Còn tiếp -------------------------

Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
=> Giáo án hoá học 12 kết nối tri thức
Từ khóa: giáo án kì 2 Hoá học 12 kết nối tri thức, bài giảng kì 2 môn Hoá học 12 kết nối tri thức, tài liệu giảng dạy Hoá học 12 kết nối tri thức