Giáo án kì 2 Hoá học 12 cánh diều
Đầy đủ giáo án kì 2, giáo án cả năm Hoá học 12 cánh diều. Bộ giáo án chất lượng, chỉn chu, được hỗ trợ tốt nhất hiện nay. Khi mua giáo án được tặng thêm: bộ phiếu trắc nghiệm, bộ đề kiểm tra theo cấu trúc mới. Giáo án được gửi ngay và luôn. Có thể xem trước bất kì bài nào phía dưới trước khi mua.
Một số tài liệu quan tâm khác
Phần trình bày nội dung giáo án
I. GIÁO ÁN WORD KÌ 2 HÓA HỌC 12 CÁNH DIỀU
- Giáo án Hóa học 12 Cánh diều bài 12: Điện phân
- Giáo án Hóa học 12 Cánh diều bài 13: Cấu tạo và tính chất vật lí của kim loại
- Giáo án Hóa học 12 Cánh diều bài 14: Tính chất hóa học của kim loại
- Giáo án Hóa học 12 Cánh diều bài 15: Tách kim loại và tái chế kim loại
- Giáo án Hóa học 12 Cánh diều bài 16: Hợp kim - Sự ăn mòn kim loại
- Giáo án Hóa học 12 Cánh diều bài 17: Nguyên tố nhóm IA
- Giáo án Hóa học 12 Cánh diều bài 18: Nguyên tố nhóm IIA
- Giáo án Hóa học 12 Cánh diều bài 19: Nước cứng và làm mềm nước cứng
- Giáo án Hóa học 12 Cánh diều bài 20: Sơ lược về kim loại chuyển tiếp dãy thứ nhất
- Giáo án Hóa học 12 Cánh diều bài 21: Sơ lược về phức chất
- Giáo án Hóa học 12 Cánh diều bài 22: Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
Ngày soạn:…/…/…
Ngày dạy:…/…/…
CHỦ ĐỀ 6: ĐẠI CƯƠNG VỀ KIM LOẠI
BÀI 13. CẤU TẠO VÀ TÍNH CHẤT VẬT LÍ CỦA KIM LOẠI
I. MỤC TIÊU
1. Về kiến thức
Sau bài học này, HS sẽ:
- Trình bày được đặc điểm cấu tạo của nguyên tử kim loại và tinh thể kim loại.
- Nêu được đặc điểm của liên kết kim loại.
- Giải thích được một số tính chất vật lí chung của kim loại (tính dẻo, tính dẫn điện, tính dẫn nhiệt, tính ánh kim).
- Trình bày được ứng dụng từ tính chất vật lí chung và riêng của kim loại.
2. Năng lực
Năng lực chung:
- Năng lực giao tiếp và hợp tác: Chủ động giao tiếp trong nhóm, trình bày rõ ý tưởng cá nhân và hỗ trợ nhau hoàn thành nhiệm vụ chung, tự tin và biết kiểm soát cảm xúc, thái độ khi nói trước nhiều người.
- Năng lực giải quyết vấn đề và sáng tạo: Thu thập và làm rõ thông tin có liên quan đến vấn đề; phân tích để xây dựng được các ý tưởng phù hợp.
Năng lực đặc thù:
- Năng lực vận dụng kiến thức, kĩ năng đã học: Nhận ra, giải thích được vấn đề thực tiễn dựa trên kiến thức hoá học.
- Năng lực tìm hiểu tự nhiên dưới góc độ hoá học:
- Sử dụng được ngôn ngữ, hình vẽ, sơ đồ, biểu bảng để biểu đạt quá trình tìm hiểu vấn đề và kết quả tìm kiếm.
- Viết được báo cáo quá trình tìm hiểu.
- Năng lực nhận thức hoá học:
- Trình bày được đặc điểm cấu tạo của nguyên tử kim loại và tinh thể kim loại.
- Nêu được đặc điểm của liên kết kim loại.
- Giải thích được một số tính chất vật lí chung của kim loại (tính dẻo, tính dẫn điện, tính dẫn nhiệt, tính ánh kim).
- Trình bày được ứng dụng từ tính chất vật lí chung và riêng của kim loại.
3. Phẩm chất
- Tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
- Cẩn trọng, trung thực và thực hiện các yêu cầu trong bài học.
- Sử dụng tiết kiệm, an toàn các sản phẩm bằng kim loại.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Đối với giáo viên
- Tài liệu: SGK, SGV Hóa học 12, các hình ảnh liên quan đến bài học.
- Thiết bị dạy học: Máy tính, máy chiếu.
2. Đối với học sinh
- Tài liệu: SGK Hóa học 12.
- Tranh ảnh, tư liệu sưu tầm liên quan đến bài học theo yêu cầu của GV.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a. Mục tiêu:
- Huy động được vốn hiểu biết, kĩ năng có sẵn của học sinh về ứng dụng của kim loại để chuẩn bị cho bài học mới; học sinh cảm thấy vấn đề sắp học rất gần gũi với mình.
- Kích thích sự tò mò, khơi dậy hứng thú của học sinh về chủ đề sẽ học; tạo không khí lớp học sôi nổi, chờ đợi, thích thú.
- Học sinh trải nghiệm qua tình huống có vấn đề, trong đó chứa đựng những nội dung kiến thức, những kĩ năng để phát triển phẩm chất, năng lực mới.
b. Nội dung: HS quan sát hình ảnh GV cung cấp và thực hiện yêu cầu của GV.
c. Sản phẩm: Câu trả lời của HS về một số ứng dụng của kim loại.
d. Tổ chức thực hiện
Bước 1: GV chuyển giao nhiệm vụ học tập
- GV yêu cầu HS quan sát các hình sau.
 |  |  |
| Thép | Đồng | Vàng |
GV nêu câu hỏi: Em hãy cho biết ứng dụng của các kim loại tương ứng với mỗi hình.
Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập
- HS làm việc cá nhân, tham gia trò chơi và suy nghĩ trả lời câu hỏi của GV.
- GV hướng dẫn, hỗ trợ HS (nếu cần thiết).
Bước 3: Báo cáo kết quả hoạt động, thảo luận
- GV mời 2 – 3 HS trả lời câu hỏi:
+ Thép: là vật liệu xây dựng.
+ Đồng: lõi dây dẫn điện.
+ Vàng: trang sức.
- Các HS khác lắng nghe để nhận xét câu trả lời của bạn mình.
- GV khuyến khích HS có thể có nhiều ý kiến khác nhau.
Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập
- GV đánh giá, nhận xét của câu trả lời HS, dẫn dắt HS vào bài học: Kim loại được sử dụng nhiều trong cuộc sống như các kết cấu bằng thép, dây dẫn điện bằng đồng, đồ trang sức bằng vàng,…. Kim loại có đặc điểm gì về cấu tạo nguyên tử và liên kết mà hữu dụng như vậy? Để đi tìm câu trả lời, chúng ta cùng vào bài học ngày hôm nay Bài 13 – Cấu tạo và tính chất vật lí của kim loại.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
Hoạt động 1. Đặc điểm cấu tạo và liên kết kim loại
a. Mục tiêu: HS trình bày được đặc điểm cấu tạo, trạng thái của các đơn chất kim loại, vị trí của các ion trong mạng tinh thể, sự hình thành liên kết kim loại.
b. Nội dung: HS đọc thông tin trong SGK trang 89-90 và thực hiện yêu cầu của GV.
c. Sản phẩm: Câu trả lời của HS về đặc điểm cấu tạo, trạng thái của các đơn chất kim loại, vị trí của các ion trong mạng tinh thể, sự hình thành liên kết kim loại.
d. Tổ chức hoạt động:
| HOẠT ĐỘNG CỦA GV - HS | DỰ KIẾN SẢN PHẨM |
Bước 1: GV chuyển giao nhiệm vụ học tập - GV tổ chức cho HS quan sát bảng tuần hoàn các nguyên tố hóa học:  - GV yêu cầu HS dựa vào kiến thức đã biết, trả lời câu hỏi: Nhận xét về số electron lớp ngoài cùng và bán kính của nguyên tử kim loại. - GV cung cấp thông tin cho HS về trạng thái tồn tại của các đơn chất kim loại ở nhiệt độ phòng, vị trí của các ion dương kim loại trong mạng tinh thể. - GV yêu cầu HS quan sát Hình 13.2. 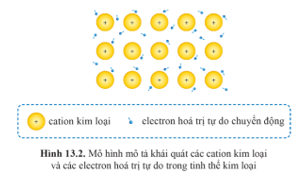 - GV yêu cầu HS dựa vào thông tin trong hình, hoàn thành câu hỏi Luyện tập 1: Trong mạng tinh thể kim loại, các electron hóa trị tự do chuyển động theo một hướng hay theo nhiều hướng? - GV hướng dẫn HS nghiên cứu thông tin mục I.3. - GV yêu cầu HS dựa vào thông tin vừa tìm hiểu, liên hệ với kiến thức đã học, thảo luận nhóm 4 và hoàn thành câu hỏi: Liên kết kim loại là gì? Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập - HS quan sát hình, vận dụng kiến thức đã học kết hợp đọc thông tin trong SGK để trả lời câu hỏi. - GV hướng dẫn, hỗ trợ HS (nếu cần thiết). Bước 3: Báo cáo kết quả hoạt động, thảo luận - GV mời đại diện 2 – 3 HS trả lời câu hỏi. * Trả lời câu hỏi của GV (DKSP). * Trả lời câu hỏi Luyện tập 1: Trong mạng tinh thể kim loại, các electron hoá trị tự do chuyển động theo nhiều hướng. * Trả lời câu hỏi của GV (DKSP). - GV yêu cầu các HS khác lắng nghe, nhận xét, nêu ý kiến bổ sung (nếu có). Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập - GV đánh giá câu trả lời của HS, đưa ra kết luận về đặc điểm cấu tạo và liên kết kim loại. - GV chuyển sang nội dung mới. | I. Đặc điểm cấu tạo và liên kết kim loại 1. Đặc điểm cấu tạo của nguyên tử kim loại - Thường có ít electron ở lớp ngoài cùng. - Bán kính của nguyên tử kim loại thường lớn hơn khá nhiều so với bán kính của nguyên tử phi kim cùng chu kì. - Các electron hóa trị ở lớp vỏ ngoài cùng của nguyên tử kim loại chịu lực hút yếu của hạt nhân. 2. Cấu tạo tinh thể kim loại - Ở điều kiện thường, các kim loại ở thể rắn, có cấu tạo tinh thể (trừ thủy ngân ở thể lỏng). - Trong tinh thể kim loại, do chịu lực hút yếu của hạt nhân nguyên tử nên các electron hóa trị dễ tách ra khỏi nguyên tử, tạo thành các electron hóa trị tự do và cation kim loại. Vì vậy, tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron hóa trị chuyển động tự do. 3. Liên kết kim loại - Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong mạng tinh thể kim loại.
|
--------------------------------------
--------------------- Còn tiếp ----------------------
Ngày soạn:…/…/…
Ngày dạy:…/…/…
BÀI 15. TÁCH KIM LOẠI VÀ TÁI CHẾ KIM LOẠI
I. MỤC TIÊU
1. Về kiến thức
Sau bài học này, HS sẽ:
- Nêu được khái quát trạng thái tự nhiên của kim loại và một số quặng, mỏ kim loại phổ biến.
- Trình bày và giải thích được phương pháp tách kim loại hoạt động mạnh như sodium, magnesium, nhôm (aluminium); phương pháp tách kim loại hoạt động trung bình như kẽm (zinc), sắt (iron); phương pháp tách kim loại kém hoạt động như đồng (copper).
- Trình bày được nhu cầu và thực tiễn tái chế kim loại phổ biến như sắt, nhôm, đồng,...
2. Năng lực
Năng lực chung:
- Năng lực giao tiếp và hợp tác: Chủ động giao tiếp trong nhóm, trình bày rõ ý tưởng cá nhân và hỗ trợ nhau hoàn thành nhiệm vụ chung, tự tin và biết kiểm soát cảm xúc, thái độ khi nói trước nhiều người.
- Năng lực giải quyết vấn đề và sáng tạo: Thu thập và làm rõ thông tin có liên quan đến vấn đề; phân tích để xây dựng được các ý tưởng phù hợp.
Năng lực đặc thù:
- Năng lực vận dụng kiến thức, kĩ năng đã học: Nhận ra, giải thích được vấn đề thực tiễn dựa trên kiến thức hoá học.
- Năng lực tìm hiểu tự nhiên dưới góc độ hoá học:
- Sử dụng được ngôn ngữ, hình vẽ, sơ đồ, biểu bảng để biểu đạt quá trình tìm hiểu vấn đề và kết quả tìm kiếm.
- Viết được báo cáo quá trình tìm hiểu.
- Năng lực nhận thức hoá học:
- Nêu được khái quát trạng thái tự nhiên của kim loại và một số quặng, mỏ kim loại phổ biến.
- Trình bày và giải thích được phương pháp tách kim loại hoạt động mạnh như sodium, magnesium, nhôm (aluminium); phương pháp tách kim loại hoạt động trung bình như kẽm (zinc), sắt (iron); phương pháp tách kim loại kém hoạt động như đồng (copper).
- Trình bày được nhu cầu và thực tiễn tái chế kim loại phổ biến như sắt, nhôm, đồng,...
3. Phẩm chất
- Tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
- Cẩn trọng, trung thực và thực hiện các yêu cầu trong bài học.
- Sử dụng tiết kiệm các nguồn tài nguyên như quặng kim loại; có ý thức bảo vệ môi trường ở những nơi có khai thác, chế biến quặng.
- Có ý thức thu gom, phân loại các đồ vật bằng kim loại đã qua sử dụng để tái chế; có ý thức bảo tồn tài nguyên thiên nhiên cho các thế hệ tương lai.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Đối với giáo viên
- Tài liệu: SGK, SGV Hóa học 12, các hình ảnh liên quan đến bài học.
- Thiết bị dạy học: Máy tính, máy chiếu.
- Bảng thế điện cực, sơ đồ quá trình tách kim loại, sơ đồ minh họa quá trình sản xuất một số kim loại (sơ đồ lò cao, bình điện phân nóng chảy,…).
2. Đối với học sinh
- Tài liệu: SGK Hóa học 12.
- Tranh ảnh, tư liệu sưu tầm liên quan đến bài học theo yêu cầu của GV.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a. Mục tiêu:
- Huy động được vốn hiểu biết, kĩ năng có sẵn của học sinh (về phản ứng oxi hóa – khử, thế điện cực chuẩn, điện phân, tính chất hóa học của kim loại,…) để chuẩn bị cho bài học mới; học sinh cảm thấy vấn đề sắp học rất gần gũi với mình.
- Kích thích sự tò mò, khơi dậy hứng thú của học sinh về chủ đề sẽ học; tạo không khí lớp học sôi nổi, chờ đợi, thích thú.
- Học sinh trải nghiệm qua tình huống có vấn đề, trong đó chứa đựng những nội dung kiến thức, những kĩ năng để phát triển phẩm chất, năng lực mới.
b. Nội dung: GV tổ chức cho HS trả lời câu hỏi để tìm các từ hàng ngang, từ đó tìm được từ khóa liên quan đến bài học.
c. Sản phẩm: HS tìm được từ khóa liên quan đến bài học.
d. Tổ chức thực hiện
Bước 1: GV chuyển giao nhiệm vụ học tập
- GV tổ chức cho HS tham gia trò chơi ô chữ, yêu cầu: Em hãy trả lời các câu hỏi sau để tìm được từ thích hợp điền vào các hàng ngang tương ứng, từ đó xác định được từ khóa.
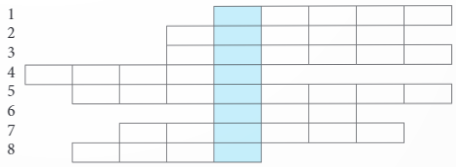
Câu 1: Tên loại lò được dùng để luyện quặng sắt thành gang.
Câu 2: Các khoáng vật trong tự nhiên dùng làm nguyên liệu để sản xuất kim loại gọi chung là gì?
Câu 3: Tên loại quặng sắt được dùng làm nguyên liệu sản xuất sulfuric acid.
Câu 4: Tên loại hợp chất giữa một nguyên tố với oxygen.
Câu 5: Tên quá trình phân hủy hợp chất dưới tác dụng của dòng điện một chiều.
Câu 6: Quá trình biến ion kim loại thành kim loại gọi là quá trình gì?
Câu 7: Tên gọi quá trình chuyển đổi các vật liệu đã qua sử dụng thành nguyên liệu mới.
Câu 8: Trong công nghiệp, kim loại nào được sản xuất từ quặng bauxite?
Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập
- HS làm việc cá nhân, tham gia trò chơi và suy nghĩ trả lời câu hỏi của GV.
- GV hướng dẫn, hỗ trợ HS (nếu cần thiết).
Bước 3: Báo cáo kết quả hoạt động, thảo luận
- GV mời 2 – 3 HS trả lời câu hỏi:
Câu 1: Lò cao.
Câu 2: Quặng.
Câu 3: Pyrite.
Câu 4: Oxide.
Câu 5: Điện phân.
Câu 6: Khử.
Câu 7: Tái chế.
Câu 8: Nhôm
Từ khóa: LUYEN KIM (luyện kim).
- Các HS khác lắng nghe để nhận xét câu trả lời của bạn mình.
- GV khuyến khích HS có thể có nhiều ý kiến khác nhau.
- GV cung cấp thêm thông tin về từ khóa: Luyện kim (metallurgy) là ngành công nghiệp điều chế các kim loại từ quặng hoặc từ các nguyên liệu khác,…
Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập
- GV đánh giá, nhận xét của câu trả lời HS, dẫn dắt HS vào bài học: Trong tự nhiên, các kim loại (trừ vàng, bạc và platinum) thường tồn tại dưới dạng hợp chất trong quặng. Vậy có các phương pháp nào dùng để tách kim loại? Cơ sở của các phương pháp đó là gì? Để đi tìm câu trả lời, chúng ta cùng vào bài học ngày hôm nay Bài 15 – Tách kim loại và tái chế kim loại.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
Hoạt động 1. Trạng thái tự nhiên của kim loại
a. Mục tiêu: HS nêu được các dạng tồn tại của kim loại trong tự nhiên.
b. Nội dung: HS đọc các thông tin trong SGK trang 100-101 và thực hiện yêu cầu của GV.
c. Sản phẩm: Câu trả lời của HS về các dạng tồn tại của kim loại trong tự nhiên.
d. Tổ chức hoạt động:
| HOẠT ĐỘNG CỦA GV - HS | DỰ KIẾN SẢN PHẨM |
Bước 1: GV chuyển giao nhiệm vụ học tập - GV yêu cầu HS quan sát hình 15.1:  - GV yêu cầu HS dựa vào hình và thông tin trong SGK, cho biết kiến thức đã học, trả lời câu hỏi: Trong tự nhiên, kim loại tồn tại ở dạng nào? - GV tổ chức cho HS vận dụng kiến thức đã học, trả lời Câu hỏi 1: Dựa vào độ hoạt động hóa học hoặc giá trị thế điện cực chuẩn, giải thích vì sao vàng, bạc có thể tồn tại ở dạng đơn chất trong tự nhiên. - GV yêu cầu HS nghiên cứu thông tin trong SGK, trả lời Câu hỏi 2: Nước tự nhiên ở khu vực có khoáng vật calcite thường chứa cation kim loại nào? - GV tổ chức cho HS làm việc nhóm 4, tìm hiểu thông tin và hoàn thành câu hỏi Vận dụng 1: Mỏ khoáng vật là nơi tập trung quặng tới mức có thể khai thác được, như mỏ vàng Bồng Miêu, Quảng Nam và mỏ sắt Thạch Khê, Hà Tĩnh. Hãy tìm hiểu và cho biết một số mỏ kim loại quan trọng ở Việt Nam. Bước 2: HS tiếp nhận, thực hiện nhiệm vụ học tập - HS lắng nghe, vận dụng kiến thức đã học kết hợp đọc thông tin trong SGK để trả lời câu hỏi. - GV hướng dẫn, hỗ trợ HS (nếu cần thiết). Bước 3: Báo cáo kết quả hoạt động, thảo luận - GV mời đại diện 2 – 3 HS trả lời câu hỏi. * Trả lời câu hỏi của GV (DKSP). * Trả lời Câu hỏi: 1. Bạc, vàng là những kim loại có giá trị thế điện cực chuẩn cao, độ hoạt động hóa học yếu. Do đó hầu như không tác dụng với các đơn chất và hợp chất có trong tự nhiên. Vì vậy, vàng, bạc có thể tồn tại ở dạng đơn chất trong tự nhiên. 2. Thành phần chính của khoáng vật calcite là CaCO3. Vì vậy, nước tự nhiên ở khu vực có khoáng vật calcite thường chứa cation kim loại Ca2+. * Trả lời Vận dụng 1: + Mỏ quặng bauxite và alumina Nhân Cơ, Đăk R’Lấp, Đắk Nông. + Mỏ đồng Sin Quyền, Bát Xát, Lào Cai. - GV yêu cầu các HS khác lắng nghe, nhận xét, nêu ý kiến bổ sung (nếu có). Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập - GV đánh giá câu trả lời của HS, đưa ra kết luận về trạng thái tự nhiên của kim loại. - GV chuyển sang nội dung mới. | I. Trạng thái tự nhiên của kim loại - Trong vỏ Trái Đất, đa số các nguyên tố kim loại tồn tại ở dạng hợp chất oxide và muối không tan, một số kim loại quý tồn tại ở dạng đơn chất hoặc hợp kim. - Trong nước mặt và nước ngầm, các nguyên tố kim loại tồn tại ở dạng cation như Na+, Mg+, Ca2+,…. - Trong cơ thể sinh vật, nguyên tố calcium có trong xương và răng; các nguyên tố như potassium, sắt, đồng,… có trong máu. - Quặng kim loại chứa các khoáng vật tạo bởi hợp chất của kim loại hoặc đơn chất kim loại và tạp chất. - Nhôm và sắt là những nguyên tố kim loại chiếm hàm lượng cao trong vỏ Trái Đất ⇒ Quặng nhôm và quặng sắt là các quặng kim loại phổ biến nhất.
|
--------------------------------------
--------------------- Còn tiếp ----------------------
II. TRẮC NGHIỆM KÌ 2 HÓA HỌC 12 CÁNH DIỀU
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 12: Điện phân
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 13: Cấu tạo và tính chất vật lí của kim loại
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 14: Tính chất hóa học của kim loại
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 15: Tách kim loại và tái chế kim loại
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 16: Hợp kim - Sự ăn mòn kim loại
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 17: Nguyên tố nhóm IA
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 18: Nguyên tố nhóm IIA
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 19: Nước cứng và làm mềm nước cứng
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 20: Sơ lược về kim loại chuyển tiếp dãy thứ nhất
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 21: Sơ lược về phức chất
- Phiếu trắc nghiệm Hóa học 12 cánh diều Bài 22: Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
CHỦ ĐỀ 6. ĐẠI CƯƠNG KIM LOẠI
BÀI 15. TÁCH KIM LOẠI VÀ TÁI CHẾ KIM LOẠI
A. TRẮC NGHIỆM
1. NHẬN BIẾT (11 câu)
Câu 1: Kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A. Fe.
B. Na.
C. Cu.
D. Ag.
Câu 2: Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
A. Fe.
B. Cu.
C. Mg.
D. Ag.
Câu 3: Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện?
A. Mg.
B. Fe.
C. Na.
D. Al.
Câu 4: Kim loại nào sau đây điều chế được bằng phương pháp nhiệt luyện với chất khử là H2?
A. K.
B. Na.
C. Cu.
D. Ca.
Câu 5: Ở nhiệt độ cao, CO khử được oxide nào sau đây?
A. CaO.
B. Fe2O3.
C. Na2O.
D. K2O.
Câu 6: Gang và thép là hợp kim của
A. nhôm (aluminium) với đồng (copper).
B. sắt (iron) với carbon và một số nguyên tố khác.
C. carbon với silicon.
D. sắt (iron) với nhôm (aluminium).
Câu 7: Gang là hợp kim của sắt (iron) với carbon và một lượng nhỏ các nguyên tố khác như: Si, Mn, S,… trong đó hàm lượng carbon chiếm:
A. Từ 2% đến 6%.
B. Dưới 2%.
C. Từ 2% đến 5%.
D. Trên 6%.
Câu 8: Thép là hợp kim của sắt (iron) với carbon và một số nguyên tố khác trong đó hàm lượng carbon chiếm:
A. Trên 2%.
B. Dưới 2%.
C. Từ 2% đến 5%.
D. Trên 5%.
Câu 9: Trong công nghiệp, Mg được điều chế bằng cách nào dưới đây?
A. Điện phân nóng chảy MgCl2.
B. Cho kim loại Fe vào dung dịch MgCl2.
C. Điện phân dung dịch MgSO4.
D. Cho kim loại K vào dung dịch Mg(NO3)2.
Câu 10: Ở nhiệt độ cao, H2 khử được oxit nào sau đây?
A. K2O.
B. CaO.
C. Na2O.
D. CuO.
……………………
2. THÔNG HIỂU (9 câu)
Câu 1: Cho luồng khí H2 dư qua hỗn hợp các oxit CuO, Fe2O3, Al2O3, MgO nung nóng ở nhiệt độ cao. Sau phản ứng, hỗn hợp chất rắn thu được gồm
A. Cu, Fe, Al, Mg.
B. Cu, FeO, Al2O3, MgO.
C. Cu, Fe, Al2O3, MgO.
D. Cu, Fe, Al, MgO.
--------------------------------------
--------------------- Còn tiếp ----------------------
CHỦ ĐỀ 6. ĐẠI CƯƠNG KIM LOẠI
BÀI 16. HỢP KIM - SỰ ĂN MÒN KIM LOẠI
A. TRẮC NGHIỆM
1. NHẬN BIẾT (13 câu)
Câu 1: Ăn mòn kim loại là
A. Sự phá hủy kim loại do tác dụng hóa học của môi trường.
B. Sự phá hủy kim loại do tác dụng lí học của môi trường.
C. Sự phá hủy kim loại do tác dụng của lực cơ học.
D. Sự phá hủy kim loại do tác quá trình phân hủy bởi nhiệt.
Câu 2: Liên kết hoá học chủ yếu trong hợp kim là
A. liên kết kim loại và liên kết cộng hoá trị.
B. liên kết cộng hoá trị và liên kết ion.
C. liên kết ion và tương tác yếu giữa các phân tử (tương tác Van der Waals).
D. tương tác yếu giữa các phân tử (tương tác Van der Waals) và liên kết kim loại.
Câu 3: Cần phải vệ sinh sạch, lau khô các vật dụng đồ dùng bằng kim loại khi sử dụng để
A. hạn chế sự ăn mòn.
B. không làm bẩn các đồ dùng khác.
C. không gây hại cho người sử dụng, không làm ảnh hưởng tới môi trường.
D. kim loại sáng, đẹp.
Câu 4: Yếu tố nào sau đây không ảnh hưởng đến sự ăn mòn kim loại
A. Môi trường.
B. Thành phần kim loại.
C. Áp suất.
D. Nhiệt độ.
Câu 5: Kim loại vừa tan được trong dung dịch HCl, vừa tan được trong dung dịch NaOH là
A. Cu.
B. Zn.
C. Mg.
D. Ag.
Câu 6: Phát biểu nào sau đây sai?
A. Hợp kim có tính dẫn điện
B. Hợp kim có tính dẫn nhiệt
C. Hợp kim có tính dẻo
D. Hợp kim có mềm hơn so với các kim loại thành phần
Câu 7: Hợp kim nào sau đây là hợp kim của sắt?
A. Đồng thau
B. Thép
C. Đuy-ra
D. Magnesite
Câu 8: Phát biểu nào sau đây đúng?
A. Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại hoặc phi kim khác
B. Không có tính dẫn điện, dẫn nhiệt, tính dẻo và ánh kim
C. Hay bị gỉ, mềm , chịu nhiệt tốt, chịu ma sát tốt
D. Hợp kim là vật liệu kim loại có chứa hai kim loại cơ bản
Câu 9: Trong hợp kim đuyra, nguyên tố chiếm hàm lượng cao nhất là
A. Mg.
B. Al.
C. Mn.
D. Cu.
Câu 10: Trong thành phần của gang, nguyên tố chiếm hàm lượng cao nhất là
A. Fe.
B. Si.
C. Mn.
D. S.
…………………
2. THÔNG HIỂU (9 câu)
Câu 1: Phát biểu nào sau đây đúng?
A. Hợp kim là vật liệu kim loại có chứa một kim loại cơ bản và một số kim loại hoặc phi kim khác
B. Không có tính dẫn điện, dẫn nhiệt, tính dẻo và ánh kim
C. Hay bị gỉ, mềm , chịu nhiệt tốt, chịu ma sát tốt
D. Hợp kim là vật liệu kim loại có chứa hai kim loại cơ bản
--------------------------------------
--------------------- Còn tiếp ----------------------

Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
=> Giáo án hoá học 12 cánh diều
Từ khóa: giáo án kì 2 Hoá học 12 cánh diều, bài giảng kì 2 môn Hoá học 12 cánh diều, tài liệu giảng dạy Hoá học 12 cánh diều