Giáo án điện tử chuyên đề Hoá học 12 cánh diều Bài 7: Liên kết và cấu tạo của phức chất
Tải giáo án điện tử Chuyên đề học tập Hoá học 12 cánh diều Bài 7: Liên kết và cấu tạo của phức chất. Bộ giáo án chuyên đề được thiết kế sinh động, đẹp mắt. Thao tác tải về đơn giản, dễ dàng sử dụng và chỉnh sửa. Thầy, cô kéo xuống để xem chi tiết.
Xem: => Giáo án hoá học 12 cánh diều
Click vào ảnh dưới đây để xem 1 phần giáo án rõ nét







Xem toàn bộ: Giáo án điện tử chuyên đề hóa học 12 cánh diều
CHÀO MỪNG CÁC EM
ĐẾN VỚI BÀI HỌC HÔM NAY!
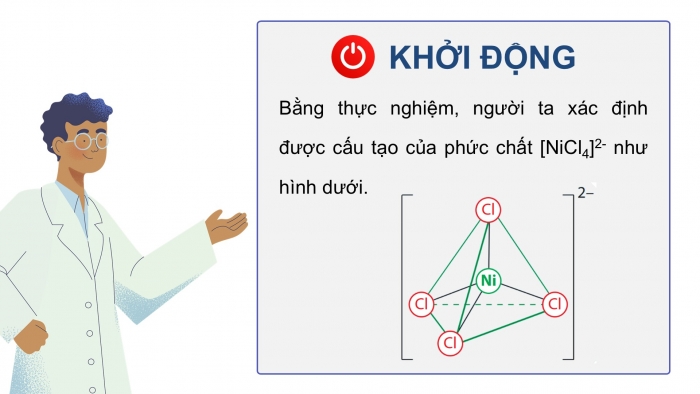
Bằng thực nghiệm, người ta xác định được cấu tạo của phức chất [NiCl4]2- như hình dưới.
KHỞI ĐỘNG
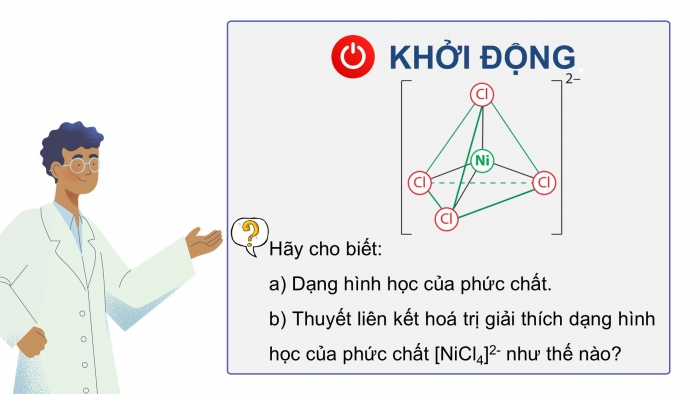
KHỞI ĐỘNG
Hãy cho biết:
a) Dạng hình học của phức chất.
b) Thuyết liên kết hoá trị giải thích dạng hình học của phức chất [NiCl4]2- như thế nào?
a) Dạng hình học của phức chất là: dạng tứ diện.
b) Thuyết liên kết hóa trị giải thích dạng hình học của phức chất [NiCl4]2- như sau:
Phức chất có điện tích là -2, mỗi ion Cl− có điện tích là -1 nên điện tích của nguyên tử trung tâm là +2.
Cấu hình electron của ion Ni2+ là: [Ar]3d84s04p0.
Cấu hình electron hoá trị dạng ô orbital của Ni2+ là:
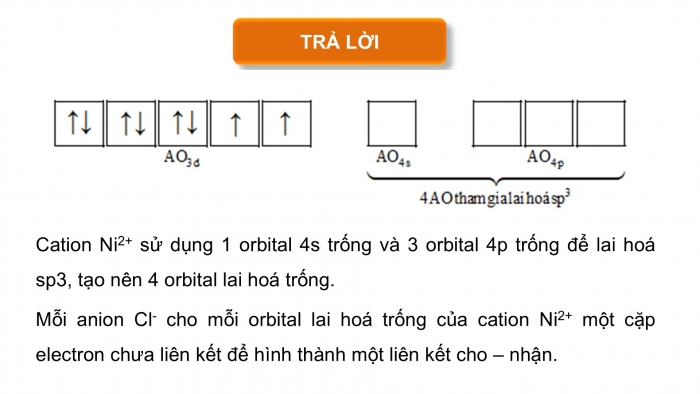
TRẢ LỜI
TRẢ LỜI
Cation Ni2+ sử dụng 1 orbital 4s trống và 3 orbital 4p trống để lai hoá sp3, tạo nên 4 orbital lai hoá trống.
Mỗi anion Cl- cho mỗi orbital lai hoá trống của cation Ni2+ một cặp electron chưa liên kết để hình thành một liên kết cho – nhận.
BÀI 7:
LIÊN KẾT VÀ CẤU TẠO CỦA PHỨC CHẤT
NỘI DUNG BÀI HỌC
Liên kết và cấu tạo phức chất theo thuyết liên kết hóa trị
Dạng hình học của phức chất
Đồng phân phức chất
I.
LIÊN KẾT VÀ CẤU TẠO PHỨC CHẤT THEO THUYẾT LIÊN KẾT HÓA TRỊ
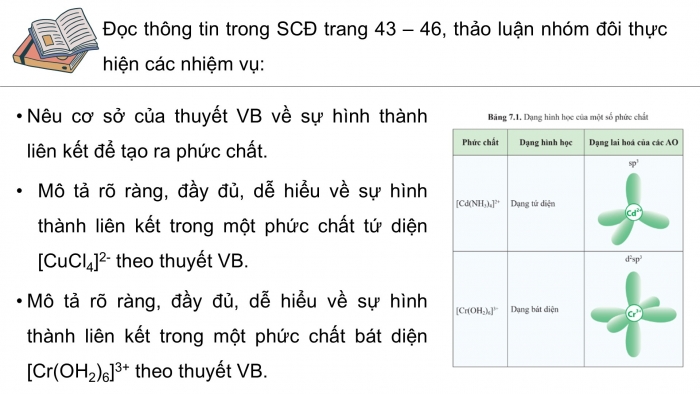
Đọc thông tin trong SCĐ trang 43 – 46, thảo luận nhóm đôi thực hiện các nhiệm vụ:
- Nêu cơ sở của thuyết VB về sự hình thành liên kết để tạo ra phức chất.
- Mô tả rõ ràng, đầy đủ, dễ hiểu về sự hình thành liên kết trong một phức chất tứ diện [CuCl4]2- theo thuyết VB.
- Mô tả rõ ràng, đầy đủ, dễ hiểu về sự hình thành liên kết trong một phức chất bát diện [Cr(OH2)6]3+ theo thuyết VB.
1. CƠ SỞ CỦA THUYẾT
Theo thuyết Liên kết hóa trị, liên kết giữa phối tử và nguyên tử trung tâm trong phức chất là liên kết cho – nhận.
Liên kết này được hình thành từ quá trình phân tử hoặc anion cho cặp electron chưa liên kết (hay electron hóa trị riêng) vào các orbital lai hóa trống của cation kim loại hoặc nguyên tử kim loại.
2. ÁP DỤNG
VÍ DỤ 1
Theo thuyết Liên kết hóa trị, liên kết và cấu tạo phức chất [CuCl4]2- được giải thích như sau:
Phức chất có điện tích là -2, mỗi anion Cl- có điện tích -1 nên điện tích của cation kim loại tạo nguyên tử trung tâm là +2.
Cấu hình electron của cation Cu2+ là: [Ar]3d94s04p0.
Cấu hình electron hóa trị ở dạng ô orbital của Cu2+ là:
2. ÁP DỤNG
VÍ DỤ 2
Theo thuyết Liên kết hóa trị, liên kết và cấu tạo phức chất [Cr(OH2)6]3+ được giải thích như sau:
Phức chất có điện tích là +3, mỗi phân tử H2O có điện tích bằng 0 nên điện tích của cation kim loại tạo nguyên tử trung tâm là +3.
Cấu hình electron của cation Cr3+ là: [Ar]3d34s04p0.
Cấu hình electron hóa trị ở dạng ô orbital của Cr3+ là:
Câu hỏi SCĐ trang 44:
Xác định điện tích của nguyên tử trung tâm trong phức chất [Cd(NH3)4]2+.
Điện tích của nguyên tử trung tâm tạo phức chất [Cd(NH3)4]2+ là +2.
Luyện tập 1, 2 SCĐ trang 45:
CÂU 1
Thực nghiệm xác nhận phức chất [Zn(NH3)4]2+ có dạng hình học tứ diện. Giải thích sự hình thành liên kết và mô tả cấu tạo của phức chất này theo thuyết Liên kết hóa trị.
CÂU 2
Thực nghiệm xác nhận phức chất [FeF6]4- có dạng hình học bát diện. Giải thích sự hình thành liên kết và mô tả cấu tạo của phức chất này theo thuyết Liên kết hóa trị.
1. Theo thuyết Liên kết hóa trị, liên kết và cấu tạo phức chất [Zn(NH3)4]2+ được giải thích như sau:
- Phức chất có điện tích là +2, mỗi phân tử NH3 có điện tích bằng 0 nên điện tích của cation kim loại tạo nguyên tử trung tâm là +2.
- Cấu hình electron của cation Zn2+ là: [Ar]3d104s04p0.
- Cấu hình electron hóa trị ở dạng ô orbital của Zn2+ là:
TRẢ LỜI
2. Theo thuyết Liên kết hóa trị, liên kết và cấu tạo phức chất [FeF6]4- được giải thích như sau:
- Phức chất có điện tích là -4, mỗi anion F- có điện tích bằng -1 nên điện tích của cation kim loại tạo nguyên tử trung tâm là +2.
- Cấu hình electron của cation Fe2+ là: [Ar]3d64s04p0.
- Cấu hình electron hóa trị ở dạng ô orbital của Fe2+ là:
TRẢ LỜI
II.
DẠNG HÌNH HỌC CỦA PHỨC CHẤT
Các phức chất [ML6], [ML4] có dạng hình học phổ biến là gì? Cho ví dụ minh họa.
1. Dạng hình học phổ biến của phức [ML6]
Các phức chất [ML6] có dạng hình học phổ biến là bát diện.
Nhiều phức chất có dạng hình học bát diện như
[Fe(CN)6]3-
[Co(NH3)6]3
[Cu(OH2)6]2+
2. Dạng hình học phổ biến của phức [ML4]
Các phức chất [ML4] có dạng hình học phổ biến là tứ diện.
Có nhiều phức chất có dạng hình học tứ diện như
[CuCl4]2-
[CoCl4]2-
[Cd(NH3)4]2+
[Ni(CO)4]
Luyện tập trong SCĐ trang 46
3. Theo thực nghiệm, phức chất [Fe(CN)6]3- có dạng hình học bát diện. Hãy vẽ dạng hình học của phức chất này.
Luyện tập trong SCĐ trang 46
4. Thực nghiệm xác nhận phức chất [Cd(NH3)4]2+ có dạng hình học tứ diện. Hãy vẽ dạng hình học của phức chất này.
III.
ĐỒNG PHÂN
PHỨC CHẤT
Nêu đặc điểm của đồng phân cis và trans ở phức chất, kèm công thức cấu tạo minh họa.
Nêu đặc điểm của đồng phân ion hóa ở phức chất, kèm công thức cấu tạo minh họa.
THẢO LUẬN CẶP ĐÔI
Nêu đặc điểm của đồng phân liên kết ở phức chất, kèm công thức cấu tạo minh họa.
--------------------------------------
--------------------- Còn tiếp ----------------------
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Giáo án điện tử chuyên đề hóa học 12 cánh diều
ĐẦY ĐỦ GIÁO ÁN CÁC BỘ SÁCH KHÁC
GIÁO ÁN WORD LỚP 12 CÁNH DIỀU
Giáo án hoạt động trải nghiệm hướng nghiệp 12 cánh diều
Giáo án Tin học 12 - Định hướng khoa học máy tính cánh diều
Giáo án Tin học 12 - Định hướng Tin học ứng dụng cánh diều
GIÁO ÁN POWERPOINT LỚP 12 CÁNH DIỀU
Giáo án Powerpoint Toán 12 Cánh diều
Giáo án powerpoint hình học 12 cánh diều
Giáo án powerpoint đại số 12 cánh diều
Giáo án powerpoint vật lí 12 cánh diều
Giáo án powerpoint sinh học 12 cánh diều
Giáo án powerpoint hoá học 12 cánh diều
Giáo án powerpoint ngữ văn 12 cánh diều
Giáo án powerpoint lịch sử 12 cánh diều
Giáo án powerpoint địa lí 12 cánh diều
Giáo án powerpoint Kinh tế pháp luật 12 cánh diều
Giáo án powerpoint Công nghệ 12 Công nghệ điện - điện tử cánh diều
Giáo án powerpoint Công nghệ 12 Lâm nghiệp - Thuỷ sản cánh diều
Giáo án powerpoint Tin học 12 - Định hướng Tin học ứng dụng cánh diều
Giáo án powerpoint Tin học 12 - Định hướng khoa học máy tính cánh diều
Giáo án powerpoint hoạt động trải nghiệm hướng nghiệp 12 cánh diều
GIÁO ÁN CHUYÊN ĐỀ LỚP 12 CÁNH DIỀU
GIÁO ÁN POWERPOINT CHUYÊN ĐỀ 12 CÁNH DIỀU
GIÁO ÁN DẠY THÊM LỚP 12 CÁNH DIỀU
Giáo án dạy thêm toán 12 cánh diều
Giáo án dạy thêm ngữ văn 12 cánh diều
Giáo án powerpoint dạy thêm ngữ văn 12 cánh diều
Giáo án powerpoint dạy thêm toán 12 cánh diều
