Giáo án và PPT Hoá học 11 kết nối Bài 4: Nitrogen
Đồng bộ giáo án word và powerpoint (ppt) Bài 4: Nitrogen. Thuộc chương trình Hoá học 11 kết nối tri thức. Giáo án được biên soạn chỉn chu, hấp dẫn. Nhằm tạo sự lôi cuốn và hứng thú học tập cho học sinh.
Click vào ảnh dưới đây để xem giáo án WORD rõ nét












Giáo án ppt đồng bộ với word









Còn nữa....
Các tài liệu bổ trợ khác
Xem toàn bộ: Trọn bộ giáo án và PPT Hoá học 11 kết nối tri thức
CHƯƠNG 2. NITROGEN - SULFUR
BÀI 4: NITROGEN - SULFUR
HOẠT ĐỘNG KHỞI ĐỘNG
GV yêu cầu HS thảo luận và trả lời:
Tìm hiểu vị trí và cấu hình electron của nguyên tử N
HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
I. TRẠNG THÁI TỰ NHIÊN
HS thảo luận trả lời câu hỏi:
Nitrogen tồn tại ở những dạng nào?
Nêu những dạng tồn tại của nitrogen?
Sản phẩm dự kiến:
Ở trạng thái tự nhiên, nitrogen tồn tại ở dạng đơn chất và hợp chất:
- Dạng đơn chất: 78% thể tích không khí; trong tự nhiên là hỗn hợp 2 đồng vị 14N (99,63%) và 15N (0,37%)
- Dạng hợp chất: trong khoáng vật sodium nitrate (diêm tiêu Chile); thành phần protein, nucleic acid.
II. CẤU TẠO NGUYÊN TỬ VÀ PHÂN TỬ
Hoạt động 1: Cấu tạo nguyên tử
HS thảo luận trả lời câu hỏi:
Em hãy cho biết cấu tạo nguyên tử của nitrogen.
Em hãy liệt kê các số oxi hoá thường gặp của nitrogen.
Sản phẩm dự kiến:
- Nguyên tố nitrogen ở ô số 7, nhóm VA, chu kì 2 trong bảng tuần hoàn, có độ âm điện lớn
- Các số oxi hóa thường gặp của nitrogen:
- 3; 0; + 1; + 2; + 3; + 4; +5
Hoạt động 2: Cấu tạo phân tử
HS thảo luận trả lời câu hỏi:
Em hãy mô tả liên kết trong phân tử nitrogen.
Trả lời CH hoạt động mục II.2 SGK trang 30:
Viết công thức electron, công thức Lewis và công thức cấu tạo của phân tử nitrogen
Từ cấu tạo phân tử, hãy cho biết tại sao phân tử N2 có năng lượng liên kết lớn. Dự đoán về khả năng hoạt động hóa học của nitrogen ở nhiệt độ thường
Sản phẩm dự kiến:
Phân tử nitrogen gồm hai nguyên tử, liên kết với nhau bằng liên kết ba (1 liên kết và 2 liên kết ); năng lượng liên kết lớn và không có cực
1. Công thức Lewis của phân tử nitrogen:
:N≡N:
Nếu coi hai nguyên tử nitrogen không ở trạng thái lai hóa sp:
- 1 liên kết tạo thành nhờ sự xen phủ dọc theo trục liên kết của cặp orbital 2pz–2pz
- 2 liên kết tạo thành nhờ sự xen phủ bên của các cặp orbital 2px–2px và 2py –2py
![]()
2. Phân tử nitrogen có liên kết ba bền vững, khó bị phá vỡ để tạo liên kết mới nên nitrogen khá trơ ở nhiệt độ thường
II. TÍNH CHẤT VẬT LÍ
HS thảo luận trả lời câu hỏi:
Em hãy nêu tính chất vật lí của nitrogen.
Trả lời CH1 SGK trang 30: Dựa vào tương tác van der Waals, hãy giải thích tại sao đơn chất N2 khó hóa lỏng và ít tan trong nước.
Sản phẩm dự kiến:
Tính chất vật lí:
- Ở điều kiện thường, nitrogen là chất khí, không màu, không mùi, không vị, khó hòa tan, tan rất ít trong nước.
- Khí nitrogen không duy trì sự cháy và sự hô hấp
Trả lời CH1 SGK trang 30:
- Phân tử nitrogen nhẹ và không phân cực, tương tác van der Waals giữa các phân tử nitrogen rất yếu nên khó hóa lỏng
- Tương tác van der Waals giữa các phân tử nitrogen với nước rất yếu nên ít tan trong nước
IV. TÍNH CHẤT HÓA HỌC
Hoạt động 1: Tác dụng với hydrogen
HS thảo luận trả lời câu hỏi:
Em hãy viết phương trình hoá học của phản ứng tổng hợp ammonia từ nitrogen và hydrogen bằng quá trình Haber.
Sản phẩm dự kiến:
![]()
Hoạt động 2: Tác dụng với oxygen
HS thảo luận trả lời câu hỏi:
Em hãy viết phương trình hoá học của phản ứng tổng hợp nitrogen monoxide từ nitrogen và oxygen.
Biểu diễn quá trình tạo và cung cấp đạm nitrate cho đất từ nước mưa.
Sản phẩm dự kiến:
![]()
Quá trình tạo và cung cấp đạm nitrate cho đất từ nước mưa được biểu diễn theo sơ đồ:

V. ỨNG DỤNG
HS thảo luận trả lời câu hỏi:
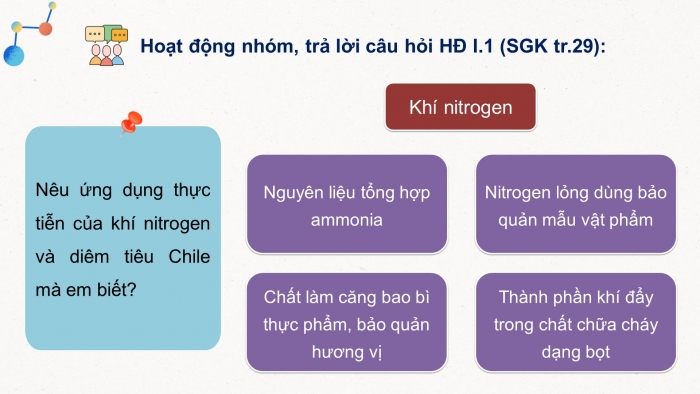
Em hãy trình bày một số ứng dụng của nitrogen.
Sản phẩm dự kiến:
Một số ứng dụng của nitrogen:
- Tác nhân làm lạnh
- Tổng hợp ammonia
- Tạo khí quyển trơ
- Bảo quản thực phẩm
- Nitrogen có nhiều ứng dụng trong sản xuất và đời sống
- Ứng dụng quan trọng nhất của khí nitrogen là để tổng hợp ammonia, mắt xích trung gian để sản xuất nitric acid, muối nitrate và nhiều hợp chất khác
- Trong nghiên cứu, khí nitrogen được dùng tạo bầu khí quyển trơ do phân tử nitrogen rất bền nhiệt
- Trong y học, nitrogen lỏng được dùng tạo môi trường lạnh sâu để bảo quản mẫu vật phẩm. Nitrogen lỏng với độ lạnh sâu cũng đóng băng mô ngay khi tiếp xúc nên được dùng điều trị mụn cóc và một số bệnh ngoài da
- Trong công nghiệp thực phẩm, nitrogen lỏng được phun vào vỏ bao bì trước khi đóng nắp nitrogen biến thành thể khí làm căng vỏ bao bì, vừa bảo vệ thực phẩm khi có va chạm, vừa bảo quản hương vị thực phẩm.
HOẠT ĐỘNG LUYỆN TẬP
Câu 1: Cấu hình electron lớp ngoài cùng của nguyên tố nitrogen là
A. 2s22p5.
B. 2s22p3.
C. 2s22p2.
D. 2s22p4.
Câu 2: Có thể thu được nitrogen từ phản ứng nào sau đây?
A. Đun nóng dung dịch bão hòa sodium nitrite với Ammonium Cloride.
B. Nhiệt phân muối Silver nitrate.
C. Cho bột Cu vào dung dịch HNO3 đặc nóng.
D. Cho muối Ammonium nitrate vào dung dịch kiềm.
Câu 3: Nung nóng 4,8 gam Mg trong bình phản ứng chứa 1 mol khí N2. Sau một thời gian, đưa bình về nhiệt độ ban đầu, thấy áp suất khí trong bình giảm 5% so với áp suất ban đầu. Thành phần phần trăm Mg đã phản ứng là
A. 37,5%.
B. 25,0%.
C. 50%.
D. 75%.
Sản phẩm dự kiến:
Câu 1: B
Câu 2: A
Câu 3: B
HOẠT ĐỘNG VẬN DỤNG
Vận dụng kiến thức, GV yêu cầu HS trả lời câu hỏi:
Câu 1: Cần bao nhiêu khí nitrogen và khí hydrogen để điều chế được 67,2 lít khí ammonia? Biết rằng thể tích của các khí đều được đo ở cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%?
Câu 2: Cho 2,64 gam kim loại tác dụng với N2 tạo nên 2,92 gam nitrite. Tìm công thức của nitrite đó
Trên chỉ là 1 phần của giáo án. Giáo án khi tải về có đầy đủ nội dung của bài. Đủ nội dung của học kì I + học kì II
Đủ kho tài liệu môn học
=> Tài liệu sẽ được gửi ngay và luôn
Cách tải:
- Bước 1: Chuyển phí vào STK: 1214136868686 - cty Fidutech - MB
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo và nhận tài liệu
Xem toàn bộ: Trọn bộ giáo án và PPT Hoá học 11 kết nối tri thức
TÀI LIỆU GIẢNG DẠY HOÁ HỌC 11 KẾT NỐI TRI THỨC
Giáo án hóa học 11 kết nối tri thức đủ cả năm
Giáo án điện tử hoá học 11 kết nối tri thức
Giáo án chuyên đề Hóa học 11 kết nối tri thức đủ cả năm
Giáo án điện tử chuyên đề hoá học 11 kết nối tri thức
Trò chơi khởi động Hoá học 11 kết nối tri thức
Video AI khởi động Hoá học 11 kết nối tri thức hấp dẫn
Giáo án tích hợp NLS Hoá học 11 kết nối tri thức
Câu hỏi và bài tập trắc nghiệm hóa học 11 kết nối tri thức
Đề thi hóa học 11 kết nối tri thức
File word đáp án hóa học 11 kết nối tri thức
Bài tập file word Hóa học 11 kết nối tri thức
Kiến thức trọng tâm hóa học 11 kết nối tri thức
Đề kiểm tra 15 phút Hoá học 11 kết nối tri thức
Đề thi, đề kiểm tra cuối kì 2 hóa học 11 kết nối tri thức
Phiếu học tập theo bài Hoá học 11 kết nối tri thức cả năm
Trắc nghiệm đúng sai Hoá học 11 kết nối tri thức cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 11 kết nối tri thức cả năm
TÀI LIỆU GIẢNG DẠY HOÁ HỌC 11 CHÂN TRỜI SÁNG TẠO
Giáo án hóa học 11 chân trời sáng tạo đủ cả năm
Giáo án điện tử hoá học 11 chân trời sáng tạo
Giáo án chuyên đề Hóa học 11 chân trời sáng tạo đủ cả năm
Giáo án điện tử chuyên đề Hoá học 11 chân trời sáng tạo
Trò chơi khởi động Hoá học 11 chân trời sáng tạo
Video AI khởi động Hoá học 11 chân trời sáng tạo hấp dẫn
Câu hỏi và bài tập trắc nghiệm hóa học 11 chân trời sáng tạo
Đề thi hóa học 11 chân trời sáng tạo
File word đáp án hóa học 11 chân trời sáng tạo
Bài tập file word hóa học 11 chân trời sáng tạo
Kiến thức trọng tâm hóa học 11 chân trời sáng tạo
Đề kiểm tra 15 phút Hoá học 11 chân trời sáng tạo
Đề thi, đề kiểm tra cuối kì 2 hóa học 11 chân trời sáng tạo
Phiếu học tập theo bài Hoá học 11 chân trời sáng tạo cả năm
Trắc nghiệm đúng sai Hoá học 11 chân trời sáng tạo cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 11 chân trời sáng tạo cả năm
TÀI LIỆU GIẢNG DẠY HOÁ HỌC 11 CÁNH DIỀU
Giáo án hoá học 11 cánh diều đủ cả năm
Giáo án điện tử hoá học 11 cánh diều
Giáo án chuyên đề Hóa học 11 cánh diều đủ cả năm
Giáo án điện tử chuyên đề hoá học 11 cánh diều
Trò chơi khởi động Hoá học 11 cánh diều
Video AI khởi động Hoá học 11 cánh diều hấp dẫn
Câu hỏi và bài tập trắc nghiệm hóa học 11 cánh diều
Đề thi hóa học 11 cánh diều
Bài tập file word Hóa học 11 cánh diều
File word đáp án hóa học 11 cánh diều
Kiến thức trọng tâm hóa học 11 cánh diều
Đề kiểm tra 15 phút Hoá học 11 cánh diều
Đề thi, đề kiểm tra cuối kì 2 hóa học 11 cánh diều
Phiếu học tập theo bài Hoá học 11 cánh diều cả năm
Trắc nghiệm đúng sai Hoá học 11 cánh diều cả năm
Trắc nghiệm dạng câu trả lời ngắn Hoá học 11 cánh diều cả năm
